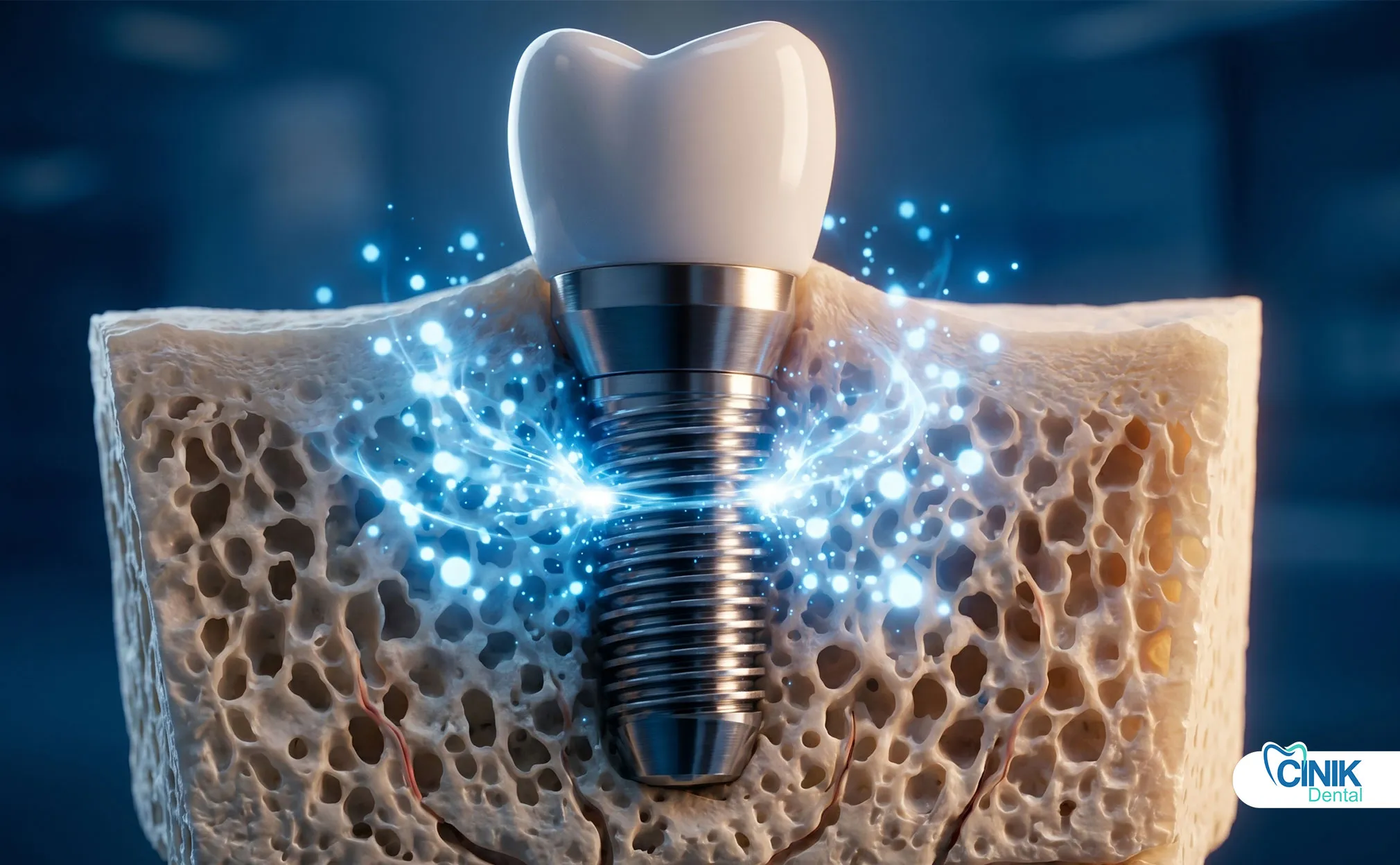
Was ist Exosom-Therapie und warum ist sie wichtig für Zahnimplantate?
Die Exosom-Therapie stellt einen Durchbruch in der regenerativen Zahnmedizin dar. Diese zellfreie Behandlung nutzt winzige Vesikel, um die Knochenheilung zu beschleunigen, Entzündungen zu reduzieren und die Erfolgsraten von Implantaten zu verbessern. Im Gegensatz zu herkömmlichen Stammzellansätzen liefert die Exosom-Therapie Wachstumsfaktoren ohne lebende Zellen, wodurch Risiken von Abstoßung oder Tumorbildung eliminiert werden.
Zahnimplantate dienen als Goldstandard für Zahnersatz. Dennoch stehen Kliniker vor anhaltenden Herausforderungen. Einige Patienten erleben verzögerte Heilung. Andere leiden unter periimplantärer Entzündung oder unzureichender Knochendichte. Diese Komplikationen beeinträchtigen die Stabilität und Langlebigkeit von Implantaten.
Die regenerative Zahnmedizin wendet sich nun Exosomen als Lösung zu. Diese nanoskaligen Partikel wirken als biologische Botenstoffe. Sie transportieren Proteine, RNA und Lipide, die natürliche Reparaturprozesse anregen. Forschung zeigt, dass sie die Osseointegration verbessern, die kritische Verbindung zwischen Implantat und Knochen (Valadi et al., 2007). Dieser Artikel untersucht, wie die Exosom-Therapie die Implantatzahnmedizin durch wissenschaftliche Mechanismen, klinische Anwendungen und zukünftiges Potenzial transformiert.
Was sind Exosomen und wie funktionieren sie bei der Gewebereparatur?
Exosomen sind extrazelluläre Vesikel mit einem Durchmesser von 30 bis 150 Nanometern. Zellen setzen diese Bläschen frei, um mit benachbarten Geweben zu kommunizieren. Sie entstehen aus dem endosomalen Weg durch einen Prozess namens multivesikuläre Körperfusion. Stellen Sie sich diese als biologische Textnachrichten vor. Eine Zelle sendet Anweisungen. Eine andere Zelle empfängt das Signal und ändert ihr Verhalten.
Tabelle 1: Kernkomponenten von Exosomen und ihre Funktionen
Komponente | Funktion | Therapeutische Wirkung |
Proteine | Zell-Signalübertragung | Reparaturwege aktivieren |
miRNA | Genregulation | Entzündung und Knochenwachstum kontrollieren |
mRNA | Proteinsynthese | Geweberegeneration direkt steuern |
Lipide | Membranstruktur | Stabilität und Zellfusion gewährleisten |
Die Zusammensetzung variiert je nach Ursprungszelle. Mesenchymale Stammzell-abgeleitete Exosomen (MSC-Exosomen) tragen über 850 Proteine, darunter Transforming Growth Factor-β und Insulinwachstumsfaktor (Zhang et al., 2020). Zahnmark-Stammzellen setzen Exosomen frei, die mit osteogenen miRNAs angereichert sind. Diese spezialisierte Fracht erklärt, warum Exosomen aus verschiedenen Quellen unterschiedliche Heilungseffekte erzeugen.
Exosomen lösen große Probleme, die mit der Stammzelltherapie verbunden sind. Stammzellen können Immunreaktionen auslösen. Sie können Tumore bilden. Sie erfordern strenge Lagerbedingungen. Exosomen umgehen diese Probleme vollständig. Sie bieten geringe Immunogenität, hohe Biokompatibilität und reduzierte Sicherheitsbedenken (Shi et al., 2021). Patienten erhalten die regenerativen Vorteile ohne die zellulären Risiken.
Wie fördern Exosomen die Knochenbildung um Zahnimplantate?
Welche Mechanismen treiben die Verbesserung der Osteogenese an?
Exosomen aktivieren mehrere Wege, um Knochen aufzubauen. Sie stimulieren die Differenzierung von Osteoblasten. Sie erhöhen die Ablagerung der Knochenmatrix. Sie fördern die Mineralisierung im gesamten Heilungsbereich.
Forschung von Furuta et al. (2016) zeigt, dass MSC-Exosomen die Frakturheilung in Mausmodellen fördern. Die Exosomen erhöhen die Aktivität der alkalischen Phosphatase (ALP). Dieses Enzym dient als früher Marker der Knochenbildung. Auch die Osteocalcin (OCN)-Spiegel steigen. Dieses Protein zeigt die Entwicklung einer reifen Knochenmatrix an.
Drei primäre Signalwege treiben diese Effekte an:
BMP/Smad-Weg: Exosomen liefern knochenmorphogenetische Proteine. Diese Proteine binden an Zelloberflächenrezeptoren. Sie aktivieren Smad-Transkriptionsfaktoren. Die Expression von Runx2 und Osterix nimmt zu. Die Knochenbildung beschleunigt sich.
Wnt/β-Catenin-Weg: Exosomen stabilisieren β-Catenin in Empfängerzellen. Dieses Molekül gelangt in den Zellkern. Es aktiviert Gene, die für Zellproliferation und -differenzierung verantwortlich sind. Zhang et al. (2020) fanden heraus, dass menschliche Nabelschnur-MSC-Exosomen den Knochenverlust durch diesen Mechanismus reduzieren.
PI3K/AKT-Weg: Exosomen lösen Überlebenssignale in Zielzellen aus. Dies verhindert Apoptose während der kritischen frühen Heilungsphase. Studien zeigen, dass die Hemmung dieses Weges die durch Exosomen induzierte Knochenbildung blockiert (Chen et al., 2019).
Wie verbessern Exosomen die Blutversorgung an Implantationsstellen?
Angiogenese erweist sich als wesentlich für eine erfolgreiche Osseointegration. Knochengewebe benötigt Sauerstoff und Nährstoffe. Ohne ausreichende Vaskularisierung scheitern Implantate.
Exosomen stimulieren die Produktion von vaskulärem endothelialem Wachstumsfaktor (VEGF). Sie fördern Endothelzellen, röhrenartige Strukturen zu bilden. Qi et al. (2016) beobachteten, dass hiPS-MSC-Exosomen in Kombination mit β-TCP-Gerüsten sowohl die Knochenregeneration als auch die Angiogenese in Rattenmodellen verbesserten. Die Gefäße drangen tiefer in das Knochentransplantatmaterial ein. Diese doppelte Wirkung, Knochenaufbau plus Gefäßbildung, schafft eine günstige Umgebung für die Implantatintegration.
Welche Rolle spielen Exosomen bei der Kontrolle von Entzündungen?
Entzündungen zerstören Implantate. Periimplantitis betrifft bis zu 20% der Patienten mit Zahnimplantaten. Traditionelle Antibiotika helfen, schaffen aber Resistenzprobleme. Exosomen bieten eine biologische Lösung.
Exosomen, die aus dentalen Pulpa-Stammzellen gewonnen werden (DPSC-EXO), unterdrücken proinflammatorische Zytokine. Sie hemmen die Produktion von IL-1β und TNF-α. Sie blockieren den IL-6/JAK2/STAT3-Signalweg (Li et al., 2023). Dieser Weg treibt destruktive Entzündungen in parodontalen Geweben an.
Makrophagen ändern ihr Verhalten nach Exosomenexposition. Proinflammatorische M1-Makrophagen verwandeln sich in antiinflammatorische M2-Makrophagen. Diese Polarisationsverschiebung reduziert Gewebeschäden. Sie schafft eine pro-heilende Umgebung um das Implantat (Shen et al., 2020).
Wo können Kliniker die Exosomentherapie in der Implantatzahnheilkunde anwenden?
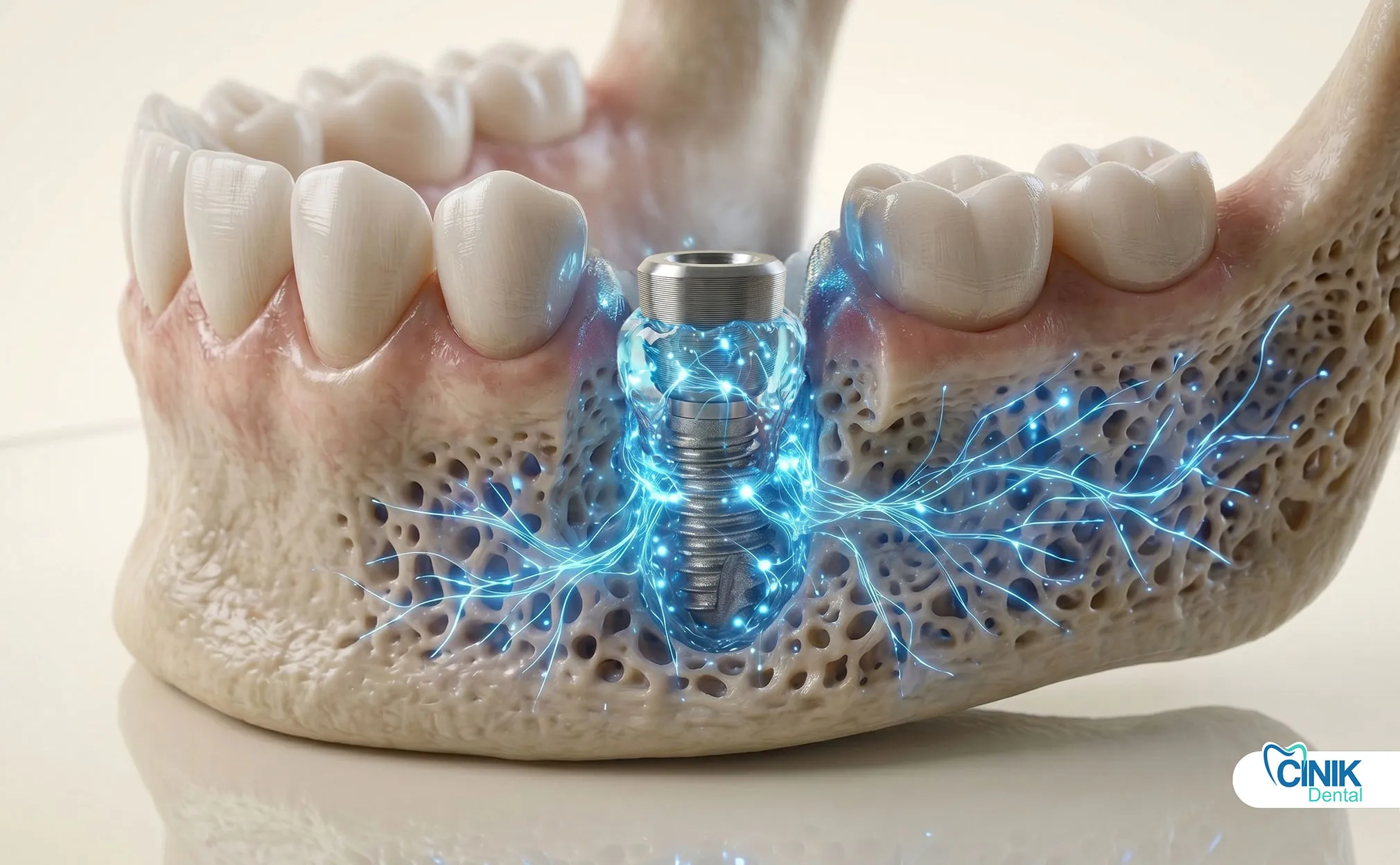
Können Exosomen die Osseointegration in Standard-Implantatfällen beschleunigen?
Ja. Exosomen verbessern den Knochen-zu-Implantat-Kontakt erheblich. Sie beschleunigen die Integrationszeitleisten. Traditionelle Osseointegration erfordert drei bis sechs Monate. Die Exosomentherapie kann diesen Zeitraum basierend auf präklinischen Daten um 30 bis 40 % verkürzen.
Wang et al. (2020) entwickelten ein selbstheilendes Hydrogel, das Nabelschnur-MSC-Exosomen enthält. Das Material förderte die Knochenregeneration bei kritischen Defekten. Der Knochenvolumenanteil stieg im Vergleich zu Kontrollgruppen. Dies deutet auf eine schnellere und robustere Implantatintegration hin, wenn Exosomen vorhanden sind.
Helfen Exosomen Patienten mit unzureichendem Knochen?
Absolut. Die Regeneration des Alveolarknochens stellt eine wichtige Anwendung dar. Viele Patienten haben nicht genügend Knochen für die sofortige Implantation. Exosomen verbessern Knochenaufbauverfahren. Sie verbessern die Ergebnisse der Kammaugmentation. Sie verhindern Knochenresorption nach der Extraktion.
Tabelle 2: Exosomenquellen und ihre regenerativen Eigenschaften
Quelle | Osteogenes Potenzial | Immunmodulatorische Stärke | Zugänglichkeit |
Knochenmark-MSCs | Hoch | Mäßig | Invasiv |
Zahnpulpa-Stammzellen | Sehr hoch | Sehr hoch | Minimalinvasiv |
Periodontales Ligament | Hoch | Hoch | Mäßig |
Gingivale MSCs | Mäßig | Sehr hoch | Einfach |
Dentale Stammzellen liefern überlegene Exosomen für orale Anwendungen. Sie exprimieren spezifische Marker wie CD24 und CD140a. Diese Zellen proliferieren schneller als Knochenmarkalternativen. Sie widerstehen der Seneszenz während der Kulturerweiterung. Am wichtigsten ist, dass sie sich natürlich an die orale Umgebung anpassen (Kotova et al., 2021).
Können Exosomen Weichgewebe um Implantate heilen?
Weichgewebedichtungen verhindern bakterielle Invasion. Sie schützen den darunterliegenden Knochen. Exosomen beschleunigen die Heilung von gingivalen Wunden. Sie stimulieren die Migration von Fibroblasten und die Kollagenproduktion.
Zhou et al. (2022) zeigten, dass exosom-funktionalisierte Gerüste die Integration von Weichgewebe verbesserten. Das gingivale Epithel heilte vollständiger. Dies reduzierte postoperative Komplikationen. Es verbesserte die ästhetischen Endergebnisse für vordere Implantatrestaurationen.
Sind Exosomen wirksam gegen periimplantäre Erkrankungen?
Forschung unterstützt diese Anwendung stark. Periimplantitis beinhaltet bakterielle Infektion und entzündlichen Knochenverlust. Exosomen bieten doppelten Schutz. Sie modulieren Immunantworten. Sie tragen auch antimikrobielle Peptide.
Lei et al. (2022) zeigten, dass aus Stammzellen gewonnene Exosomen entzündlichen Knochenverlust in Parodontitis-Modellen behandelten. Der Knochenvolumenanteil verbesserte sich signifikant. Tartrat-resistente saure Phosphatase (TRAP)-positive Osteoklasten nahmen ab. Dies weist auf eine reduzierte Knochendestruktion hin.
Welche Quellen bieten die besten Exosomen für dentale Anwendungen?
Mesenchymale Stammzellen bleiben die Hauptquelle. Allerdings bieten dentale Gewebe einzigartige Vorteile.
Dentalmark-Stammzellen (DPSCs): Diese Zellen befinden sich innerhalb der Zahnstrukturen. Sie zeigen hohe Proliferationsraten. Sie behalten ein starkes osteogenes Potenzial auch nach mehreren Passagen bei. DPSC-Exosomen enthalten spezifische miRNAs, die Angiogenese und Neuroprotektion fördern.
Parodontal-Ligament-Stammzellen (PDLSCs): Diese Zellen verbinden Zähne mit dem Knochen. Sie regulieren auf natürliche Weise die parodontale Homöostase. Ihre Exosomen sind hervorragend in der Regeneration von Weichgewebe und der Bildung der Knochen-Ligament-Schnittstelle.
Stammzellen aus menschlichen exfolierten Milchzähnen (SHEDs): Diese Zellen stammen aus Milchzähnen. Sie zeigen außergewöhnliche Plastizität. Sie exprimieren frühe Stammzellmarker länger als andere Quellen. SHED-Exosomen könnten überlegene neuroregenerative Eigenschaften bieten.
Entwickelte Exosomen: Wissenschaftler beladen nun Exosomen mit spezifischer Fracht. Sie fügen HIF-1α hinzu, um die Angiogenese zu steigern. Sie integrieren miR-375, um die Osteogenese zu verbessern (Chen et al., 2019). Diese Anpassung ermöglicht gezielte Therapien für spezifische Implantatkomplikationen.
Welche klinischen Vorteile erhalten Patienten durch die Exosomentherapie?
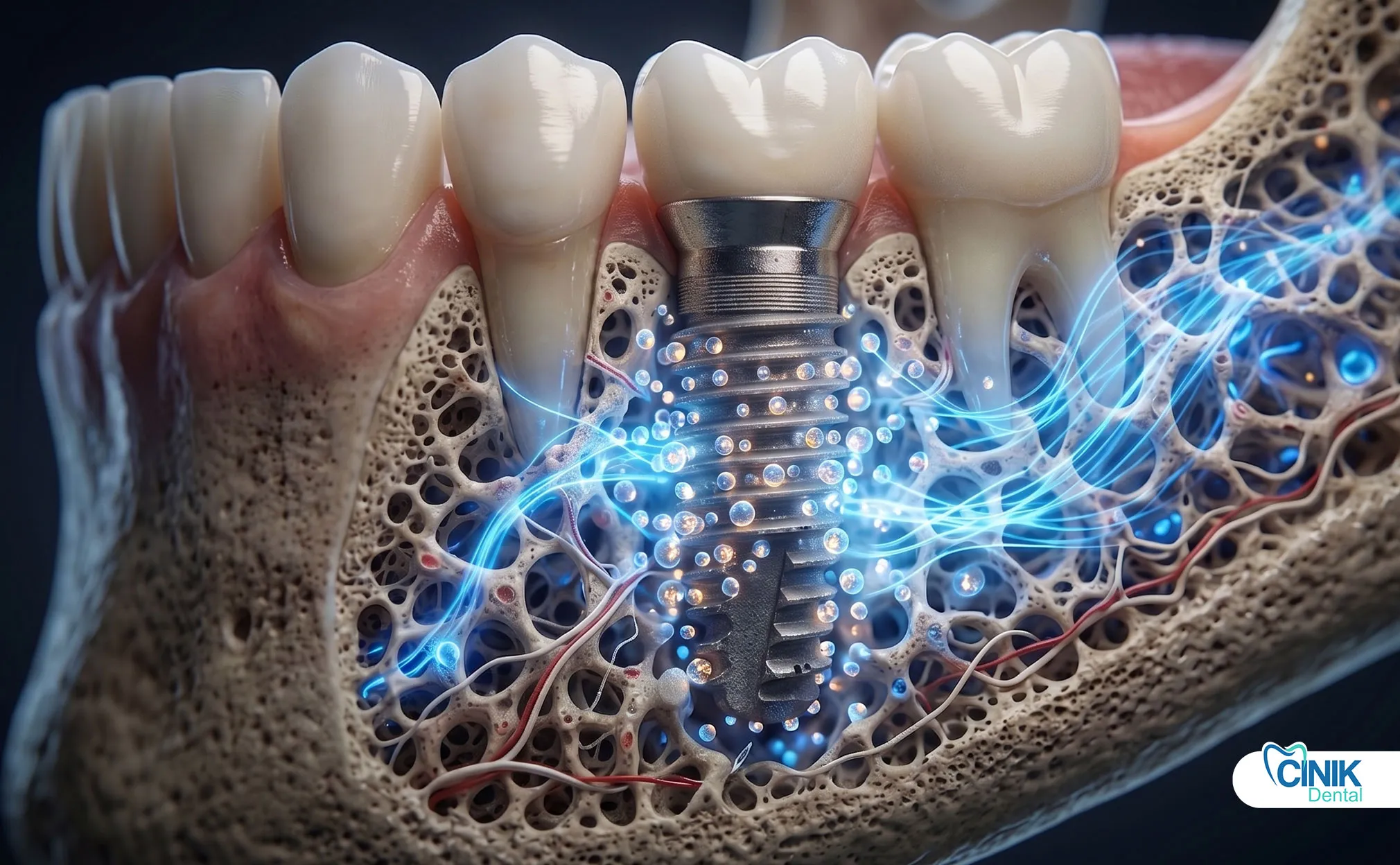
Patienten erleben messbare Verbesserungen:
Schnellere Heilung: Exosomen-behandelte Stellen zeigen frühere Knochenmineralisierung. Weichgewebe schließen sich schneller. Dies verkürzt die Zeit zwischen Implantatplatzierung und endgültiger Restauration.
Weniger Schmerzen und Schwellungen: Die entzündungshemmende Wirkung reduziert postoperative Beschwerden. Patienten berichten von geringeren Schmerzpunkten. Sie benötigen weniger Schmerzmittel.
Höhere Erfolgsraten: Frühe Integration verhindert Mikrobewegungen. Dies reduziert Implantatversagen. Exosomen könnten sich besonders wertvoll für Patienten mit Diabetes, Osteoporose oder Raucherhistorie erweisen, Gruppen, die traditionell als Hochrisiko gelten.
Minimalinvasive Verabreichung: Kliniker wenden Exosomen durch Hydrogele, Kollagenmembranen oder direkte Injektion an. Keine zusätzliche Operation ist erforderlich. Die Therapie integriert sich nahtlos in Standard-Implantatprotokolle.
Personalisierte Möglichkeiten: Zukünftige Behandlungen könnten patientenspezifische Exosomen verwenden. Ausgezogene Weisheitszähne könnten personalisierte regenerative Therapien bieten.
Welche Einschränkungen und Herausforderungen bestehen derzeit?
Warum ist die Exosomentherapie noch nicht weit verbreitet?
Beweislücken: Die meisten Studien bleiben präklinisch. Forscher haben umfangreiche Tierversuche durchgeführt. Klinische Studien am Menschen hinken hinterher. Langzeitdaten zu Überlebensraten von Implantaten mit Exosomentherapie existieren noch nicht.
Standardisierungsprobleme: Es gibt kein universelles Protokoll für die Isolierung von Exosomen. Die differentielle Ultrazentrifugation bleibt beliebt, liefert jedoch variable Ausbeuten. Fällungsmethoden erhöhen die Menge, verringern jedoch die Reinheit. Mikrofluidische Technologien versprechen Konsistenz, erfordern jedoch teure Ausrüstung (Miron et al., 2025).
Regulatorische Hürden: Regulierungsbehörden klassifizieren Exosomen als biologische Produkte. Sie erfordern umfangreiche Sicherheitstests. Die Massenproduktion muss den Standards der Guten Herstellungspraxis entsprechen. Diese Anforderungen verlangsamen die klinische Einführung.
Technische Barrieren: Exosomen degradieren während der Lagerung. Sie erfordern spezifische Temperaturbedingungen. Sie verlieren an Aktivität, wenn sie unsachgemäß behandelt werden. Liefersysteme müssen Exosomen schützen, bis sie die Zielgewebe erreichen. Aktuelle Gerüste und Hydrogele bieten teilweise Lösungen. Bessere Träger werden benötigt.
Wie vergleichen sich Exosomen mit anderen regenerativen Behandlungen?
Tabelle 3: Vergleich regenerativer Therapien
Merkmal | Exosomen | Stammzellen | PRP | Knochenersatzmaterialien |
Zellfrei | Ja | Nein | Teilweise | Ja |
Immunogenität | Sehr niedrig | Mäßig | Niedrig | Sehr niedrig |
Tumorrisiko | Keines | Niedrig | Keines | Keines |
Wachstumsfaktorkonzentration | Sehr hoch | Mäßig | Mäßig | Niedrig |
Handhabungskomplexität | Mäßig | Hoch | Niedrig | Niedrig |
Kosten | Mäßig | Hoch | Niedrig | Variabel |
Exosomen übertreffen Stammzellen in der Sicherheit. Sie vermeiden das Verpflichtungsrisiko. Sie beseitigen Bedenken hinsichtlich unvorhersehbarer Zelldifferenzierung in vivo. Sie bieten laut aktuellen Analysen die dreifache Wachstumsfaktorkonzentration von adulten Stammzellen.
Im Vergleich zu plättchenreichem Plasma (PRP) bieten Exosomen eine größere Konsistenz. Die PRP-Qualität variiert je nach Alter und Gesundheitszustand des Patienten. Exosomen aus kultivierten Stammzellen behalten eine standardisierte Potenz bei. Sie liefern vorhersehbare therapeutische Effekte.
Knochenersatzmaterialien bieten strukturelle Unterstützung. Exosomen bieten biologische Anweisungen. Die Kombination erweist sich als überlegen. Mit Exosomen beladene β-TCP-Gerüste regenerieren Knochen schneller als Gerüste allein (Ying et al., 2020).
Welche zukünftigen Entwicklungen werden die Exosomen-Therapie prägen?
Personalisierte Exosomen-Therapien: Kliniker werden Stammzellen aus den Zahngeweben der Patienten extrahieren. Sie werden diese Zellen kultivieren und Exosomen ernten. Dieser autologe Ansatz eliminiert alle Abstoßungsrisiken. Er maximiert die therapeutische Kompatibilität.
Integration intelligenter Biomaterialien: 3D-gedruckte Implantate werden Exosomen-Reservoirs enthalten. Diese Gerüste werden Vesikel allmählich freisetzen. Sie werden während der gesamten Heilungsperiode eine anhaltende Stimulation bieten.
Genbeladene Exosomen: Wissenschaftler werden Exosomen entwickeln, die spezifische genetische Anweisungen tragen. Sie werden auf Periimplantitis-Pfade abzielen. Sie werden die Nervenregeneration an Implantatstellen beschleunigen.
KI-gesteuerte Behandlungsplanung: Maschinelle Lernalgorithmen werden optimale Exosomenkonzentrationen vorhersagen. Sie werden den idealen Lieferzeitpunkt bestimmen. Sie werden Protokolle basierend auf der Genetik und Knochenqualität des Patienten personalisieren.
Wie sollten Kliniker die Exosomen-Therapie umsetzen?
Patientenauswahl: Ideale Kandidaten sind Patienten mit geringer Knochendichte. Raucher und Diabetiker profitieren besonders. Patienten, die eine sofortige Implantatplatzierung an Extraktionsstellen benötigen, zeigen verbesserte Ergebnisse.
Kontraindikationen: Patienten mit aktiven Infektionen benötigen zuerst eine Behandlung. Personen mit Blutungsstörungen benötigen eine sorgfältige Bewertung. Schwangere Patienten sollten aufgrund begrenzter Sicherheitsdaten bis nach der Geburt warten.
Integrationsprotokolle: Kliniker sollten Exosomen während der Implantatplatzierung einbeziehen. Sie können sie auf die Osteotomiestelle vor dem Einsetzen des Implantats auftragen. Sie können Kollagenmembranen in Exosomenlösungen einweichen. Sie können Exosomen mit Knochenersatzmaterialien für Sinuslift-Verfahren mischen.
Kostenüberlegungen: Derzeit erhöht die Exosomen-Therapie die Kosten für Implantatverfahren um 500 bis 2.000 $. Die Preise werden sinken, wenn die Produktion skaliert wird. Die Versicherungsdeckung bleibt begrenzt. Patienten sollten verstehen, dass dies eine Eigeninvestition in eine schnellere Heilung darstellt.
Fazit
Die Exosomtherapie für Zahnimplantate bietet ein leistungsstarkes regeneratives Werkzeug. Diese zellfreien Vesikel beschleunigen die Knochenbildung. Sie reduzieren Entzündungen. Sie verbessern die Implantatstabilität. Sie vermeiden die Risiken, die mit lebenden Zelltherapien verbunden sind.
Aktuelle Beweise unterstützen ihre Verwendung zur Verbesserung der Osseointegration. Sie zeigen besonderes Potenzial für die Knochenregeneration an defizitären Stellen. Sie bieten Lösungen für das Management von periimplantären Erkrankungen. Sie integrieren sich nahtlos in fortschrittliche Implantattechniken.
Jedoch müssen Kliniker die Einschränkungen anerkennen. Langfristige klinische Studien am Menschen bleiben notwendig. Standardisierungsbemühungen müssen fortgesetzt werden. Regulatorische Rahmenbedingungen müssen entwickelt werden.
Das Feld entwickelt sich schnell weiter. DPSC-Exosomen zeigen überlegene Potenziale für orale Anwendungen. Ingenieurtechniken verbessern Zielgenauigkeit und Wirksamkeit. Liefersysteme werden immer ausgefeilter.
Für Patienten bedeutet dies schnellere Heilung. Es bedeutet weniger Komplikationen. Es bedeutet eine breitere Kandidatur für die Implantatbehandlung. Für den Beruf bedeutet es einen Wandel hin zu biologischer statt nur mechanischer Implantatintegration.
Die Exosomtherapie steht an der Schnittstelle von Zellbiologie und klinischer Zahnmedizin. Sie überbrückt die Lücke zwischen Laborentdeckung und Patientenversorgung. Obwohl noch nicht routinemäßig, wird sie es bald sein. Kliniker, die diese Mechanismen jetzt verstehen, werden die Implantatzahnmedizin von morgen anführen.
Referenzen
Chen, Shiyi, et al. "Exosomes Derived from miR-375-Overexpressing Human Adipose Mesenchymal Stem Cells Promote Bone Regeneration." Cell Proliferation, vol. 52, no. 5, 2019, doi:10.1111/cpr.12669.
Fan, Linlin, et al. "Exosome-Functionalized Polyetheretherketone-Based Implant with Immunomodulatory Property for Enhancing Osseointegration." Bioactive Materials, vol. 6, no. 9, 2021, pp. 2754–66, doi:10.1016/j.bioactmat.2021.02.005.
Furuta, T., et al. "Mesenchymal Stem Cell-Derived Exosomes Promote Fracture Healing in a Mouse Model." Stem Cells Translational Medicine, vol. 5, no. 12, 2016, pp. 1620–30, doi:10.5966/sctm.2015-0285.
Kotova, A., et al. "Comparative Analysis of Dental Pulp and Periodontal Stem Cells: Differences in Morphology, Functionality, Osteogenic Differentiation and Proteome." Biomedicines, vol. 9, no. 11, 2021, p. 1606, doi:10.3390/biomedicines9111606.
Lei, Fengyang, et al. "Treatment of Inflammatory Bone Loss in Periodontitis by Stem Cell-Derived Exosomes." Acta Biomaterialia, vol. 141, 2022, pp. 333–43, doi:10.1016/j.actbio.2021.12.035.
Li, Mei, et al. "Dental Pulp Stem Cell-Derived Exosomes Regulate Anti-Inflammatory and Osteogenesis in Periodontal Ligament Stem Cells and Promote the Repair of Experimental Periodontitis in Rats." Frontiers in Bioengineering and Biotechnology, vol. 11, 2023, doi:10.3389/fbioe.2023.10441659.
Miron, Richard J., et al. "Isolationsmethoden von Exosomen, die aus dentalen Stammzellen gewonnen wurden." International Journal of Oral Science, 2025, doi:10.1038/s41368-025-00370-y.
Qi, X., et al. "Von menschlich induzierten pluripotenten Stammzellen abgeleitete mesenchymale Stammzellen sezernieren Exosomen, die kritische Knochendefekte durch verbesserte Angiogenese und Osteogenese bei osteoporotischen Ratten reparieren." International Journal of Biological Sciences, Bd. 12, Nr. 7, 2016, S. 836–49, doi:10.7150/ijbs.14809.
Shen, Zhenhua, et al. "Chitosan-Hydrogel, das mit aus dentalen Pulpa-Stammzellen gewonnenen Exosomen angereichert ist, lindert Parodontitis bei Mäusen über einen makrophagenabhängigen Mechanismus." Bioactive Materials, Bd. 5, Nr. 4, 2020, S. 1113–26, doi:10.1016/j.bioactmat.2020.07.002.
Shi, Qin, et al. "MSC-abgeleitete Exosomen: Eine neuartige vielversprechende Therapie für Osteoporose." Frontiers in Cell and Developmental Biology, Bd. 9, 2021, S. 723803, doi:10.3389/fcell.2021.723803.
Valadi, Hadi, et al. "Exosomen-vermittelter Transfer von mRNAs und microRNAs ist ein neuartiger Mechanismus des genetischen Austauschs zwischen Zellen." Nature Cell Biology, Bd. 9, Nr. 6, 2007, S. 654–59, doi:10.1038/ncb1596.
Wang, Ling, et al. "Ein neues selbstheilendes Hydrogel, das hucMSC-abgeleitete Exosomen enthält, fördert die Knochenregeneration." Frontiers in Bioengineering and Biotechnology, Bd. 8, 2020, S. 564731, doi:10.3389/fbioe.2020.564731.
Ying, Chang, et al. "BMSC-Exosomen tragen mutiertes HIF-1α zur Verbesserung der Angiogenese und Osteogenese bei kritischen Kalvarialdefekten." Frontiers in Bioengineering and Biotechnology, Bd. 8, 2020, S. 565561, doi:10.3389/fbioe.2020.565561.
Zhang, Shiqing, et al. "MSC-Exosomen lindern die Osteoarthritis des Kiefergelenks, indem sie Entzündungen abschwächen und die Matrix-Homöostase wiederherstellen." Biomaterials, Bd. 200, 2019, S. 35–47, doi:10.1016/j.biomaterials.2019.02.006.
Zhou, Ye, et al. "Polydopamin-beschichtete biomimetische Knochengerüste, die mit Exosomen beladen sind, fördern die osteogene Differenzierung von BMSC und die Knochenregeneration." Regenerative Therapy, Bd. 23, 2023, S. 25–36, doi:10.1016/j.reth.2023.03.005.