La extracción del nervio dental representa un procedimiento endodóntico especializado que elimina el tejido pulpar infectado o dañado del interior del diente. Los dentistas llaman a este proceso tratamiento de conducto radicular. El procedimiento salva millones de dientes naturales cada año al eliminar la fuente de infección mientras preserva la estructura externa del diente.
La odontología moderna depende en gran medida de esta intervención. Terapia endodóntica se considera uno de los procedimientos dentales más comunes a nivel mundial. Datos epidemiológicos recientes muestran que los profesionales dentales realizan millones de estos tratamientos anualmente en países desarrollados. La prevalencia refleja tanto la alta incidencia de caries dentales como las tasas de éxito que hacen que este enfoque sea preferible a la extracción para muchos pacientes.
El propósito principal de este artículo une la ciencia clínica con la comprensión práctica del paciente. Los lectores aprenderán los mecanismos biológicos detrás de la enfermedad pulpar. Entenderán por qué los dentistas recomiendan la extracción del nervio en escenarios clínicos específicos. Lo más importante es que descubrirán cómo las tecnologías modernas han transformado este procedimiento de una intervención temida a una opción de tratamiento predecible y cómoda.
El procedimiento de extracción del nervio dental aborda condiciones patológicas dentro de la cámara pulpar. Estas condiciones incluyen pulpitis irreversible, tejido pulpar necrótico e infecciones periapicales. Si no se tratan, estas condiciones conducen a la formación de abscesos, pérdida ósea y eventual pérdida del diente. La intervención temprana previene estas complicaciones y mantiene la dentición natural del paciente.
¿Qué anatomía compone el nervio dental y el complejo pulpar?
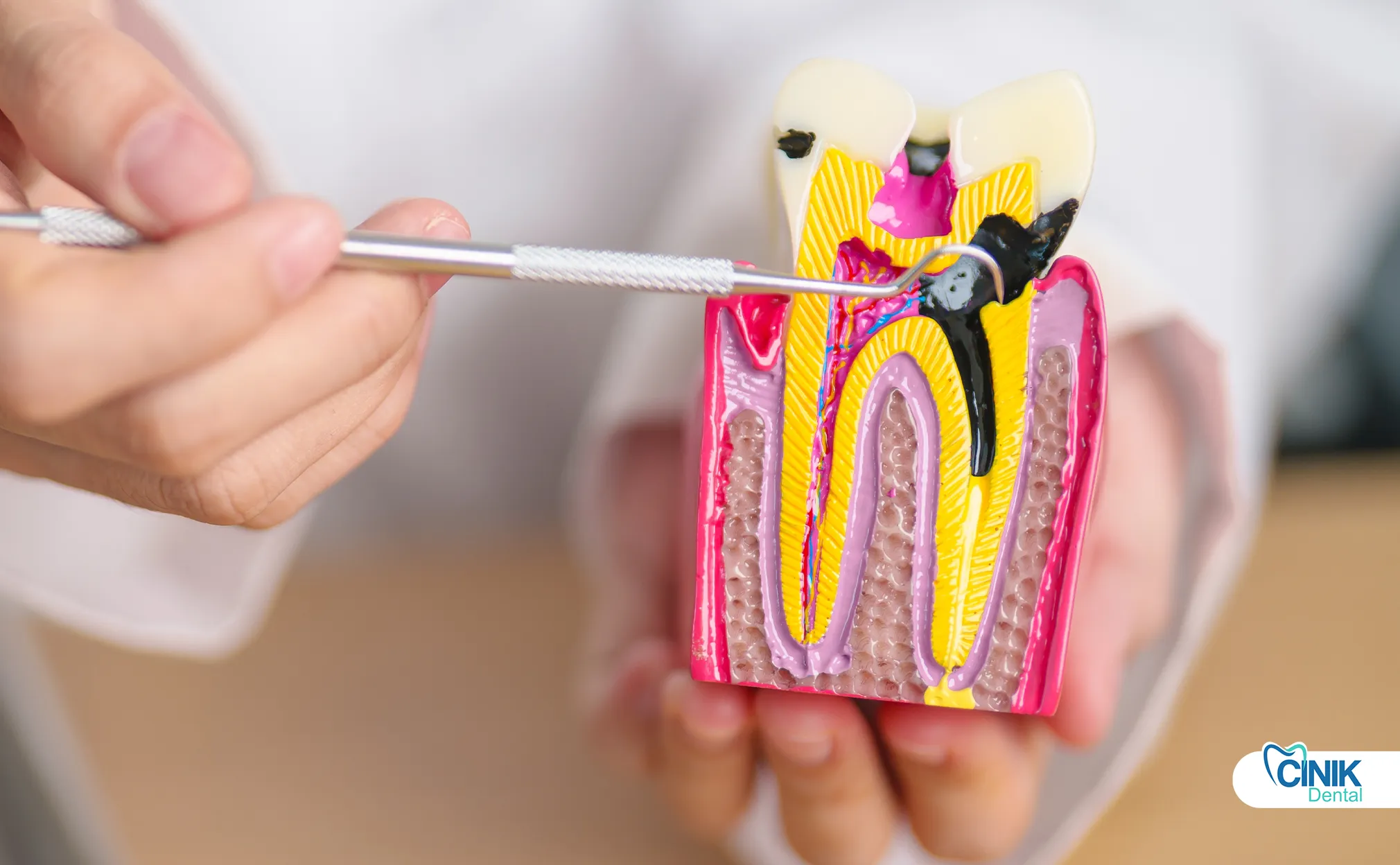
El complejo del nervio dental consiste en esmalte, dentina, cámara pulpar y conductos radiculares. La pulpa contiene nervios, vasos sanguíneos y tejido conectivo que proporcionan función sensorial y soporte de desarrollo durante la formación del diente.
Entender la anatomía del diente ayuda a los pacientes a comprender por qué la extracción del nervio se vuelve necesaria. El diente consta de varias capas distintas, cada una con funciones biológicas específicas.
La capa más externa, el esmalte, está compuesta por la sustancia más dura del cuerpo humano. Esta estructura cristalina protege el diente de daños mecánicos y erosión química. Debajo del esmalte se encuentra la dentina, un tejido calcificado que contiene túbulos microscópicos. Estos túbulos canalizan señales sensoriales desde el entorno externo hacia la cámara pulpar central.
La cámara pulpar alberga la pulpa dental, un tejido conectivo blando que contiene el haz neurovascular. Según Niki et al. (2025), la pulpa contiene dos tipos principales de nervios que inervan el tejido dental: fibras autónomas y fibras sensoriales aferentes. Las fibras autónomas simpáticas surgen del ganglio cervical superior y regulan el flujo sanguíneo a través del músculo liso arteriolar. Las fibras sensoriales aferentes se originan de las ramas maxilares y mandibulares del nervio trigémino. Estas fibras sensoriales transportan señales de dolor, temperatura y presión al cerebro.
La pulpa dental contiene odontoblastos, células especializadas que producen dentina a lo largo de la vida del diente. Estas células recubren la cámara pulpar y extienden procesos en los túbulos dentinarios. Los vasos sanguíneos dentro de la pulpa proporcionan nutrientes y oxígeno. Los vasos linfáticos drenan productos de desecho y apoyan la vigilancia inmunológica.
Durante el desarrollo dental, la pulpa juega un papel crítico. Estimula la formación de la raíz y la erupción del diente. Sin embargo, una vez que el diente madura, la importancia funcional de la pulpa disminuye. Un diente completamente desarrollado puede sobrevivir sin la pulpa porque el ligamento periodontal y los tejidos circundantes proporcionan un soporte suficiente. Esta realidad biológica permite a los dentistas eliminar la pulpa enferma sin comprometer la viabilidad a largo plazo del diente.
La edad cambia significativamente la pulpa. La investigación de Carvalho y Lussi (2017) demuestra que la densidad celular disminuye aproximadamente un 50% entre los 20 y los 70 años. La pulpa sufre fibrosis y acumula fibras de colágeno a medida que los pacientes envejecen. Los vasos sanguíneos y los nervios degeneran progresivamente. Estos cambios explican por qué los pacientes mayores a veces experimentan menos dolor por caries profundas a pesar de la extensa implicación de la pulpa.
¿Qué causa el daño y la infección del nervio dental?
Las caries dentales profundas, las fracturas dentales, los procedimientos dentales repetidos y las restauraciones defectuosas causan daño a la pulpa. Las bacterias invaden la cámara pulpar, forman biofilms y desencadenan una inflamación que lleva a pulpitis irreversible o necrosis.
Múltiples factores etiológicos contribuyen a la patología pulpar. Comprender estos factores ayuda a los pacientes a prevenir condiciones que requieren la extracción del nervio.
Las caries dentales profundas representan la causa más común de enfermedad pulpar. Cuando las caries penetran a través del esmalte y la dentina, alcanzan la cámara pulpar. Las bacterias colonizan el tejido y desencadenan respuestas inflamatorias. El cuerpo intenta combatir la infección enviando células inmunitarias al área. Este proceso inflamatorio aumenta la presión dentro de la rígida cámara pulpar, comprimiendo los nervios y causando dolor.
Las fracturas dentales y el trauma proporcionan otra vía para la invasión bacteriana. Las grietas permiten que los fluidos orales y los microorganismos entren directamente en la cámara pulpar. Incluso las fracturas microscópicas invisibles a simple vista pueden albergar bacterias. Los procedimientos dentales repetidos también estresan la pulpa. Cada episodio de perforación elimina estructura dental y genera calor, lo que puede irritar el tejido pulpar.
Las restauraciones defectuosas crean microgrietas en la interfaz diente-restauración. Estas grietas acumulan placa y permiten la fuga bacteriana. Con el tiempo, esta caries secundaria alcanza la pulpa y causa infección.
Una vez que las bacterias entran en la pulpa, forman comunidades complejas llamadas biofilms. Según la revisión del NIH sobre biofilms endodónticos (2023), la formación de biofilm implica cuatro etapas principales: formación de película de acondicionamiento, adhesión y colonización bacteriana, crecimiento y expansión, y finalmente desprendimiento. Estos biofilms resisten tanto las defensas del huésped como los tratamientos antimicrobianos.
La enfermedad progresa a través de etapas distintas. La invasión bacteriana inicial causa pulpitis reversible. En esta etapa, eliminar el irritante permite que la pulpa se cure. Sin embargo, la infección persistente conduce a pulpitis irreversible. El tejido pulpar se descompone y la inflamación se extiende a los tejidos periapicales. Eventualmente, la pulpa necrosa completamente. Las bacterias luego salen del ápice radicular e infectan el hueso circundante, formando lesiones periapicales o abscesos.
Enterococcus faecalis desempeña un papel particularmente problemático en infecciones persistentes. Este bacilo grampositivo sobrevive en condiciones adversas y resiste el hidróxido de calcio, un medicamento intracanal común. Svensäter y Bergenholtz (2004) identificaron este organismo como una de las principales causas de fracaso en el tratamiento porque penetra en los túbulos dentinarios y mantiene comunidades de biofilm que evaden la eliminación completa.
¿Qué síntomas indican que necesita la extracción del nervio dental?
El dolor dental severo y persistente, la sensibilidad a estímulos térmicos, la hinchazón, la formación de fístulas y la evidencia radiográfica de infección indican la necesidad de intervención endodóntica. Los dentistas confirman diagnósticos a través de pruebas térmicas y pruebas eléctricas de pulpa.
Los pacientes deben reconocer signos de advertencia específicos que señalan enfermedad pulpar. Estos síntomas guían las decisiones y el momento del tratamiento.
El dolor dental severo y persistente constituye el indicador más obvio. Este dolor a menudo late y empeora cuando los pacientes se acuestan. Puede despertar a los pacientes del sueño. El dolor típicamente se localiza en un diente específico, aunque puede irradiarse a áreas adyacentes. El dolor espontáneo sin estímulo sugiere fuertemente pulpitis irreversible.
La sensibilidad a la temperatura proporciona otra pista crítica. Los pacientes con enfermedad pulpar a menudo experimentan un dolor agudo y persistente al consumir bebidas calientes o frías. El dolor persiste durante minutos después de eliminar el estímulo térmico. Esta respuesta persistente difiere de la sensibilidad dental normal, que se resuelve inmediatamente al eliminar el estímulo.
La hinchazón alrededor del diente afectado indica una infección avanzada. La hinchazón puede localizarse en el tejido de las encías o extenderse a la cara y el cuello. Algunos pacientes desarrollan una fístula, una pequeña abertura de drenaje similar a un grano en el tejido de las encías. Esta fístula representa el intento del cuerpo de drenar el líquido del absceso. Los pacientes pueden sentir un sabor desagradable del líquido que sale de estas aberturas.
La imagen radiográfica revela pérdida ósea alrededor del ápice radicular. Los dentistas toman radiografías periapicales o tomografías computarizadas de haz cónico (CBCT) para visualizar estas lesiones. Las áreas oscuras alrededor de las puntas radiculares indican radiolucidez periapical, señalando destrucción ósea por infección.
Los dentistas emplean pruebas diagnósticas específicas para confirmar el estado de la pulpa. La prueba térmica aplica frío o calor a la superficie del diente. Los dientes sanos responden brevemente; los dientes enfermos responden intensamente y durante períodos prolongados. La prueba eléctrica de pulpa entrega un estímulo eléctrico leve para evaluar la viabilidad del nervio. Una lectura no receptiva sugiere pulpa necrótica.
La prueba de percusión golpea suavemente el diente para verificar la inflamación periapical. El dolor al percutir indica que la inflamación se ha extendido más allá de la pulpa hacia el ligamento periodontal que rodea el ápice radicular.
¿Cómo realizan los dentistas el procedimiento de extracción del nervio dental paso a paso?
Los dentistas siguen un protocolo sistemático: diagnóstico y planificación, anestesia y aislamiento, preparación de la cavidad de acceso, extracción de la pulpa, limpieza y conformación, llenado del canal y restauración final. Las técnicas modernas aseguran la comodidad del paciente durante el procedimiento de 60 a 90 minutos.
El tratamiento de conducto radicular sigue una secuencia precisa diseñada para eliminar la infección y sellar el sistema de conductos. Comprender estos pasos reduce la ansiedad del paciente y mejora la cooperación.
¿Cómo funciona la fase de diagnóstico y planificación del tratamiento?
Los clínicos examinan el diente clínicamente y radiográficamente. Toman radiografías o escaneos CBCT para visualizar la anatomía del canal y el estado periapical. Formulan un plan de tratamiento basado en estos hallazgos.
El dentista comienza con un examen clínico exhaustivo. Evalúan la condición del diente, verifican la movilidad y evalúan los tejidos blandos circundantes. Revisan la historia médica del paciente para identificar contraindicaciones o consideraciones especiales.
La imagen radiográfica proporciona información diagnóstica esencial. Las radiografías periapicales estándar muestran la longitud de la raíz, la curvatura y el número de conductos. Los casos complejos pueden requerir imágenes CBCT. Esta vista tridimensional revela la ramificación del canal, las calcificaciones y las lesiones periapicales que las radiografías bidimensionales no detectan.
¿Cómo garantizan la anestesia y el aislamiento la comodidad del paciente?
El anestésico local elimina la sensación de dolor. El dique de goma aísla el diente de la saliva y previene la contaminación bacteriana durante el procedimiento.
Los dentistas administran anestesia local para bloquear la conducción nerviosa. Normalmente utilizan lidocaína o articaína con epinefrina para prolongar el efecto anestésico. Los pacientes permanecen despiertos pero no sienten dolor en el área tratada.
El dique de goma proporciona una aislamiento crítico. Esta delgada hoja de látex o material no látex cubre la boca excepto por un pequeño agujero que expone el diente tratado. El dique evita que la saliva entre en el espacio del canal. También protege al paciente de tragar instrumentos o soluciones de irrigación.
¿Cómo acceden y eliminan los clínicos la pulpa?
El dentista perfora una cavidad de acceso a través de la corona para llegar a la cámara pulpar. Luego utilizan instrumentos especializados para eliminar todo el tejido pulpar de la cámara y los conductos radiculares.
La preparación de la cavidad de acceso requiere precisión. El dentista retira el techo de la cámara pulpar mientras preserva la estructura dental. Utilizan una fresa de alta velocidad para crear una apertura que proporciona acceso en línea recta a los orificios del canal.
La eliminación de la pulpa sigue inmediatamente. El dentista inserta brochas o limas con púas en los canales. Retiran estos instrumentos para extraer el tejido pulpar. Los instrumentos rotatorios con limas de níquel-titanio dominan ahora la práctica moderna. Estos instrumentos flexibles navegan por los canales curvados de manera más segura que las limas de acero inoxidable tradicionales.
¿Cómo elimina la fase de limpieza y conformación la infección?
La instrumentación mecánica combinada con la irrigación química elimina biofilms bacterianos y desechos. El hipoclorito de sodio disuelve el tejido orgánico y mata microorganismos.
La fase de limpieza y conformación constituye el paso más crítico. El dentista utiliza limas progresivamente más grandes para agrandar y dar forma a los canales. Esta acción mecánica elimina la dentina infectada y crea espacio para soluciones de irrigación.
La irrigación química sigue a cada secuencia de limado. La solución de hipoclorito de sodio sirve como el irrigante principal. Esta solución alcalina disuelve los restos de pulpa y destruye las paredes celulares bacterianas. Los dentistas utilizan concentraciones del 2-3% para tratamientos primarios. Administran la solución utilizando jeringas con agujas de ventilación lateral para evitar forzar el líquido a través del ápice.
El EDTA (ácido etilendiaminotetraacético) proporciona irrigación adyuvante. Este agente quelante elimina la capa de deslizamiento inorgánica que crean las limas. Eliminar esta capa expone los túbulos dentinarios y mejora la desinfección del canal.
Las técnicas modernas incluyen irrigación ultrasónica y sistemas de presión negativa. Estos métodos mejoran la penetración del irrigante en las ramas del canal y los túbulos dentinarios donde se ocultan las bacterias.
¿Cómo llenan y sellan los dentistas los canales?
Los dentistas llenan los canales limpios con gutapercha y sellador. Esta obturación previene la reentrada bacteriana y sella el ápice de los fluidos periapicales.
El llenado del canal ocurre después de un secado exhaustivo. El dentista selecciona puntos de gutapercha que coinciden con el tamaño final del archivo. La gutapercha, un caucho natural de árboles, proporciona un material de llenado inerte y biocompatible.
Los selladores recubren las paredes del canal antes de la inserción de la gutapercha. Estos cementos crean un efecto monobloque, uniendo el llenado a la dentina. Los selladores biocerámicos han reemplazado en gran medida a los selladores tradicionales de resina o de óxido de zinc-eugenol. Estos materiales a base de silicato de calcio sellan mejor y causan menos inflamación.
El dentista compacta la gutapercha utilizando técnicas de condensación vertical en caliente o compactación lateral. Ellos eliminan el material excedente de la cámara y colocan un sellado coronal temporal o permanente.
¿Cómo Completa la Restauración Final el Tratamiento?
El dentista coloca un empaste permanente o una corona para restaurar la función y prevenir fracturas. Los dientes posteriores requieren coronas para proteger contra fallos estructurales.
La restauración final depende de la condición y ubicación del diente. Los dientes anteriores con pérdida mínima de estructura pueden recibir empastes compuestos. Los dientes posteriores que se someten a tratamiento de conducto radicular requieren coronas de cobertura total. Estas coronas distribuyen las fuerzas de masticación y previenen fracturas verticales.
¿Qué Materiales y Tecnologías Usan los Endodoncistas Hoy en Día?
La endodoncia moderna emplea instrumentos rotatorios de níquel-titanio, localizadores electrónicos de ápice, microscopios quirúrgicos dentales, selladores biocerámicos y imágenes en 3D. Las tecnologías emergentes incluyen desinfección asistida por láser y enfoques regenerativos.
La tecnología endodóntica ha avanzado significativamente en las últimas dos décadas. Estas innovaciones mejoran las tasas de éxito, reducen el tiempo de tratamiento y aumentan la comodidad del paciente.
¿Qué Materiales Tradicionales Siguen Siendo Esenciales?
La gutapercha sigue siendo el material de llenado principal. Varios selladores aseguran sellos apicales y coronales. Los archivos de acero inoxidable aún sirven para propósitos específicos a pesar de las alternativas más nuevas.
La gutapercha ha llenado conductos radiculares durante más de un siglo. Este material termoplástico se adapta bien a las irregularidades del canal cuando se calienta. Permanece estable durante décadas sin degradarse ni causar inflamación.
Los selladores de óxido de zinc-eugenol proporcionaron el estándar durante generaciones. Estos materiales ofrecen propiedades antimicrobianas y fácil manejo. Sin embargo, se disuelven lentamente con el tiempo y pueden permitir filtraciones. Los selladores de resina modernos y los selladores biocerámicos proporcionan una capacidad de sellado superior y estabilidad dimensional.
¿Qué avances modernos mejoran los resultados del tratamiento?
Los archivos rotatorios de níquel-titanio navegan por canales curvados de manera segura. Los localizadores de ápice electrónicos determinan la longitud de trabajo con precisión. Los microscopios dentales mejoran la visibilidad. La imagenología CBCT revela anatomía compleja.
Los instrumentos rotatorios de níquel-titanio (NiTi) revolucionaron la conformación de canales. Estos archivos superelásticos se flexionan alrededor de curvas que harían que los archivos de acero inoxidable se enderecen o perforen la pared del canal. Cortan de manera eficiente y mantienen la curvatura original del canal.
Los localizadores de ápice electrónicos (EAL) determinan la longitud de trabajo del canal electrónicamente. Estos dispositivos miden la resistencia eléctrica entre un archivo en el canal y la mucosa oral. Señalan cuando el archivo alcanza la constricción apical, mejorando la precisión de la longitud en comparación con las radiografías solas.
Los microscopios quirúrgicos dentales proporcionan una magnificación de 6-25x. Los endodoncistas utilizan estos microscopios para localizar entradas de canal calcificadas, identificar canales perdidos y realizar retratamientos. La visibilidad mejorada reduce los errores de procedimiento y mejora los resultados.
La tomografía computarizada de haz cónico (CBCT) representa el estándar de imagen para casos complejos. Esta imagenología tridimensional revela istmos de canal, bifididades apicales y lesiones periapicales con una resolución de 0.1 mm. Los dentistas utilizan CBCT para la planificación preoperatoria en casos difíciles.
¿Qué tecnologías emergentes muestran promesas?
La desinfección asistida por láser, la bioprinting 3D de tejido pulpar, la terapia con células madre y los procedimientos guiados por inteligencia artificial representan la vanguardia de la investigación endodóntica.
Los láseres ahora ayudan en la desinfección de canales. Los láseres Er,Cr:YSGG y de diodo activan soluciones de irrigación y vaporizar residuos en ramas del canal. Reducen las cuentas bacterianas más allá de lo que logra la instrumentación mecánica por sí sola.
La endodoncia regenerativa ofrece una alternativa biológica al tratamiento tradicional. Los investigadores han explorado el trasplante de células madre desde que Gronthos et al. (2000) aislaron por primera vez células madre de pulpa dental. Nakashima et al. (2017) demostraron la regeneración exitosa de pulpa utilizando células madre de pulpa dental autólogas en un ensayo clínico piloto. Los pacientes recuperaron la sensibilidad pulpar, y la imagenología mostró formación de tejido similar a la dentina.
Los enfoques de bioprinting tridimensional tienen como objetivo fabricar tejido pulpar para trasplante. Los investigadores imprimen andamios utilizando hidroxiapatita y gelatina metacrilato (GelMA) cargados con células madre de pulpa dental. Estas construcciones apoyan la vascularización y la inervación cuando se implantan en los canales radiculares.
La inteligencia artificial ahora asiste en el diagnóstico y la planificación del tratamiento. Los algoritmos de aprendizaje automático analizan radiografías para detectar lesiones periapicales y predecir los resultados del tratamiento. Las aplicaciones futuras pueden incluir el modelado de conductos asistido por robots y el monitoreo en tiempo real de la ubicación del ápice.
¿Qué tasas de éxito pueden esperar los pacientes del tratamiento de conducto?
Los estudios a largo plazo muestran un 97% de supervivencia a los 10 años, un 81% a los 20 años y un 68% a los 37 años. Las tasas de éxito endodóntico oscilan entre el 89% y el 93%, dependiendo de las condiciones preoperatorias y el cuidado posterior.
La medición del éxito en endodoncia incluye dos métricas: supervivencia del diente (permanecer en la boca) y éxito endodóntico (ausencia de síntomas y curación radiográfica). Ambos son importantes para los pacientes, aunque difieren clínicamente.
¿Qué revelan los estudios de supervivencia a largo plazo?
Los tratamientos de conducto bien realizados resultan en la retención del diente durante décadas. Las principales causas de fallo tardío son la enfermedad periodontal y la fractura estructural, más que factores endodónticos.
López-Valverde et al. (2023) publicaron datos fundamentales que rastrean a los pacientes durante 5 a 37 años. Su estudio de 598 dientes tratados endodónticamente demostró tasas de supervivencia acumulativas del 97% a los 10 años, 81% a los 20 años, 76% a los 30 años y 68% a los 37 años. Estas estadísticas confirman que el tratamiento de conducto proporciona resultados duraderos.
El estudio identificó factores pronósticos específicos. Los dientes sin radiolucidez periapical preoperatoria sobrevivieron más tiempo. Los dientes restaurados con coronas mostraron mejor supervivencia que aquellos con grandes empastes. Los pacientes sin bolsas periodontales profundas mantuvieron sus dientes tratados por más tiempo.
¿Cómo se comparan los tratamientos de conducto con los implantes?
Los dientes tratados endodónticamente y los implantes de un solo diente muestran tasas de supervivencia comparables durante 5-10 años. La preservación de los dientes naturales a menudo proporciona resultados funcionales y estéticos superiores.
Las revisiones sistemáticas que comparan estas opciones muestran porcentajes de éxito similares. A los 5 años, ambos tratamientos logran aproximadamente un 95% de supervivencia. Sin embargo, las diferencias biológicas y económicas son importantes.
Los dientes naturales mantienen los ligamentos periodontales. Estos ligamentos proporcionan propriocepción, la capacidad de sentir la presión de la mordida. Los implantes carecen de este mecanismo de retroalimentación, lo que puede llevar a sobrecarga. Los dientes naturales también preservan el hueso alveolar a través de la carga funcional. Los implantes pueden causar reabsorción ósea crestal con el tiempo.
Económicamente, preservar los dientes naturales cuesta menos que la extracción y la colocación de implantes. La terapia de implantes requiere intervenciones quirúrgicas, períodos de curación y complicaciones potenciales como la periimplantitis.
¿Qué mecanismos biológicos permiten la curación?
El sistema inmunológico elimina las bacterias residuales de los tejidos periapicales. El hueso se regenera una vez que se elimina la fuente de infección. El ligamento periodontal se vuelve a unir a la superficie de la raíz.
La curación periapical comienza inmediatamente después de la desinfección del canal. Los macrófagos y los osteoclastos eliminan el tejido inflamatorio y el hueso necrótico. Luego, los osteoblastos depositan nueva matriz ósea. La curación radiográfica puede tardar de 6 a 12 meses en aparecer completamente.
El relleno del conducto radicular previene la recontaminación bacteriana. La restauración coronal sella el sistema del canal de los fluidos orales. Juntos, estos sellos permiten que los tejidos periapicales se regeneren y mantengan la salud indefinidamente.
¿Qué cuidados posteriores aseguran el éxito a largo plazo?
Los pacientes deben manejar la sensibilidad a corto plazo, mantener una excelente higiene oral, asistir a las visitas de seguimiento y obtener coronas permanentes en los dientes posteriores dentro de unas semanas después del tratamiento.
El cuidado posterior al tratamiento impacta significativamente en los resultados a largo plazo. Los pacientes deben entender tanto los requisitos inmediatos como los a largo plazo.
¿Qué síntomas a corto plazo deben esperar los pacientes?
La sensibilidad leve al masticar y a los cambios de temperatura dura de 3 a 7 días. Los medicamentos antiinflamatorios manejan el malestar de manera efectiva. El dolor severo o la hinchazón requieren contacto dental inmediato.
Después de que la anestesia desaparece, los pacientes pueden experimentar un leve malestar. Esta sensibilidad resulta de la instrumentación cerca del ápice radicular y la inflamación temporal en el ligamento periodontal. El ibuprofeno o el acetaminofén de venta libre generalmente resuelven este malestar.
Los pacientes deben evitar masticar del lado tratado hasta que se coloque la restauración permanente. El relleno temporal o la corona pueden fracturarse bajo fuerzas pesadas. Los alimentos duros arriesgan la fractura del diente antes de la colocación de la restauración de cobertura completa.
¿Qué protocolos de cuidado a largo plazo mantienen los resultados?
El cepillado y el uso de hilo dental diarios previenen fugas coronales. Los protectores nocturnos protegen contra las fuerzas de rechinamiento. Las radiografías anuales monitorean la salud periapical. El reemplazo rápido de la restauración previene la reentrada bacteriana.
La higiene oral es crítica para los dientes tratados endodónticamente. Mientras que el conducto radicular elimina la infección interna, una nueva caries en el margen de la restauración puede causar falla. Los pacientes deben cepillarse dos veces al día y usar hilo dental alrededor de todos los dientes restaurados.
El bruxismo (rechinar de dientes) pone en peligro los dientes tratados. La naturaleza quebradiza de los dientes tratados endodónticamente los hace susceptibles a fracturas verticales bajo fuerzas pesadas. Los protectores nocturnos distribuyen estas fuerzas y protegen la inversión.
Las radiografías de seguimiento a los 6-12 meses después del tratamiento confirman la curación periapical. Los dentistas comparan estas imágenes con las películas preoperatorias para evaluar la regeneración ósea. El monitoreo anual posterior captura posibles fallas temprano.
¿Qué complicaciones pueden ocurrir durante o después del tratamiento?
La limpieza incompleta del canal, las ramas del canal que se pasan por alto, las filtraciones coronales y las fracturas radiculares verticales causan la mayoría de los fracasos. El retratamiento o la cirugía apical abordan las infecciones persistentes.
A pesar de las altas tasas de éxito, ocurren complicaciones. Comprender estos riesgos ayuda a los pacientes a tomar decisiones informadas y buscar intervención oportuna.
¿Qué errores de procedimiento conducen al fracaso?
La anatomía compleja del canal radicular puede albergar infecciones no tratadas. Los dentistas pueden pasar por alto canales estrechos o calcificados. La separación de instrumentos puede bloquear el acceso al canal. Las perforaciones pueden crear nuevos caminos para las bacterias.
Los sistemas de conductos radiculares a menudo contienen más complejidad de la que sugieren los textos de anatomía estándar. Los istmos conectan canales adyacentes. Los canales accesorios se ramifican en ángulos rectos. Los canales en forma de C en los segundos molares mandibulares desafían la instrumentación convencional.
Los canales pasados por alto siguen siendo la causa más común de infección persistente. Los molares superiores típicamente tienen tres o cuatro canales; pasar por alto el segundo canal mesio-bucal (MB2) invita al fracaso. Los dientes anteriores inferiores pueden tener dos canales que aparecen como uno en las radiografías.
La separación de instrumentos ocurre cuando los archivos se fatigan dentro de los canales curvados. Los archivos de acero inoxidable se separaron con más frecuencia que los instrumentos modernos de NiTi, pero la separación aún ocurre. Los instrumentos separados bloquean el acceso al canal y pueden albergar bacterias.
¿Qué factores post-tratamiento causan fracaso?
Los sellos coronales deficientes permiten la reentrada bacteriana. La colocación tardía de la restauración permanente arriesga fracturas. Las caries secundarias invaden a través de los espacios marginales.
La calidad de la restauración final predice la supervivencia a largo plazo mejor que la técnica endodóntica. Los estudios de Gillen et al. (2011) demuestran que las restauraciones inadecuadas causan más fracasos que la recontaminación del canal. Las bacterias penetran a través de márgenes filtrantes y re-infectan el sistema de conductos.
Las fracturas estructurales representan otro modo de fallo importante. Los dientes tratados endodónticamente pierden contenido de humedad y se vuelven quebradizos. Sin coronas de cobertura total, los dientes posteriores pueden dividirse verticalmente. Estas fracturas a menudo hacen que el diente no sea restaurable.
¿Cómo manejan los clínicos los tratamientos fallidos?
El retratamiento no quirúrgico elimina las viejas obturaciones y aborda la anatomía pasada por alto. La cirugía apical elimina la punta de la raíz y coloca sellos retrógrados. La extracción sigue siendo el último recurso cuando ocurren fracturas o pérdida ósea extensa.
El retratamiento endodóntico sigue los mismos principios que el tratamiento primario con una complejidad añadida. El dentista debe eliminar las obturaciones de gutapercha, negociar alrededor de los instrumentos separados si están presentes y localizar los canales que se pasaron por alto anteriormente. Los microscopios ayudan significativamente en estos procedimientos.
La cirugía apical (apicoectomía) se vuelve necesaria cuando las lesiones persistentes resisten el retratamiento convencional. El cirujano refleja un colgajo, elimina el ápice de la raíz y coloca un relleno retrógrado. Las técnicas microquirúrgicas modernas que utilizan puntas ultrasónicas y selladores biocerámicos logran tasas de curación del 90%.
¿Qué alternativas existen además del tratamiento de conducto radicular?
La extracción dental con reemplazo a través de implantes dentales o puentes proporciona la alternativa principal. La endodoncia regenerativa ofrece una opción biológica para dientes inmaduros. La observación sola conlleva riesgos de complicaciones sistémicas.
Los pacientes que enfrentan recomendaciones de tratamiento de conducto radicular deben entender todas las opciones. Estas alternativas conllevan implicaciones distintas para la función, el costo y la longevidad.
¿Qué implica la extracción dental?
La extracción elimina todo el diente, incluida la estructura de la raíz. El procedimiento cuesta menos inicialmente que el tratamiento de conducto radicular, pero requiere reemplazo para prevenir el movimiento de los dientes adyacentes y la pérdida ósea.
La extracción proporciona una resolución inmediata del dolor y la infección. El dentista corta el ligamento periodontal y eleva el diente del alvéolo. La curación ocurre dentro de 7-10 días.
Sin embargo, la extracción crea nuevos problemas. Los dientes adyacentes se inclinan hacia el espacio. Los dientes opuestos se extruyen. El hueso alveolar se reabsorbe sin carga funcional. Estos cambios alteran la mordida y pueden causar problemas en la articulación temporomandibular.
¿Cómo se comparan las opciones de reemplazo?
Los implantes dentales reemplazan dientes individuales sin involucrar a los dientes adyacentes. Los puentes requieren la preparación de los dientes vecinos, pero proporcionan un reemplazo fijo inmediato. Las dentaduras parciales removibles son las que menos cuestan, pero ofrecen una función comprometida.
Los implantes dentales han revolucionado el reemplazo de dientes. Los fijadores de titanio se integran con el hueso a través de la oseointegración. Proporcionan soporte independiente sin preparar los dientes adyacentes. Sin embargo, los implantes requieren un volumen óseo adecuado y períodos de curación de 3-6 meses.
Los puentes tradicionales requieren coronar los dientes adyacentes al espacio. El dentista prepara estos dientes de manera similar a las preparaciones de coronas individuales. El puente conecta coronas en los dientes pilares a un pontico que reemplaza el diente faltante. Este enfoque pone en riesgo la salud a largo plazo de los dientes de soporte.
Las dentaduras parciales removibles proporcionan la opción más económica. Estos aparatos se sujetan a los dientes restantes y reemplazan múltiples unidades faltantes. Sin embargo, requieren ser removidos diariamente para su limpieza y pueden afectar el habla y el gusto.
¿Cuáles son las consideraciones funcionales y económicas?
Preservar los dientes naturales a través del tratamiento de conducto radicular generalmente cuesta menos a largo plazo que la extracción y colocación de implantes. Los dientes naturales proporcionan una propriocepción superior y resultados estéticos en comparación con los reemplazos artificiales.
El análisis económico favorece la preservación de los dientes. El tratamiento de conducto radicular más la colocación de una corona cuesta aproximadamente el 50-70% de la extracción más la terapia de implantes. Además, los dientes naturales rara vez requieren el mantenimiento que exigen los implantes.
Funcionalmente, el ligamento periodontal que rodea los dientes naturales proporciona retroalimentación sensorial que previene fuerzas de mordida excesivas. Este mecanismo protege tanto el diente como el hueso circundante. Los implantes carecen de este bucle de retroalimentación protectora.
¿Qué mitos rodean la extracción del nervio dental?
Los mitos afirman que los tratamientos de conducto radicular "matan" los dientes, causan enfermedades sistémicas o invariablemente causan dolor severo. La evidencia científica refuta estas afirmaciones de manera definitiva.
La desinformación sobre la terapia endodóntica persiste a pesar de décadas de investigación. Abordar estos mitos ayuda a los pacientes a tomar decisiones basadas en hechos en lugar de en el miedo.
¿El tratamiento de conducto radicular mata el diente?
No. El diente permanece vivo a través de los tejidos periodontales circundantes. Continúa funcionando normalmente sin la pulpa interna.
La noción de que el tratamiento de conducto radicular "mata" el diente refleja un malentendido de la biología dental. El diente consiste en más que la cámara pulpar. El ligamento periodontal sigue siendo vital después del tratamiento. Este tejido proporciona nutrición, retroalimentación sensorial y unión al hueso.
El diente continúa sintiendo presión a través del ligamento periodontal. Mantiene su posición en el arco. Soporta fuerzas de masticación. Sin la pulpa, el diente simplemente carece de sensación de temperatura y de la capacidad de formar nueva dentina internamente.
¿Este procedimiento causa dolor severo?
La anestesia moderna y las técnicas hacen que el tratamiento de conducto radicular no sea más incómodo que los empastes de rutina. La mayoría de los pacientes experimentan alivio del dolor preoperatorio inmediatamente después del procedimiento.
Históricamente, los tratamientos de conducto radicular tenían reputaciones dolorosas. Esta reputación ya no se aplica. Los anestésicos locales bloquean efectivamente la sensación de la pulpa en la mayoría de los casos. Para los dientes "calientes" con inflamación severa, técnicas de anestesia suplementarias e inyección intraósea proporcionan un entumecimiento profundo.
El malestar postoperatorio, cuando ocurre, típicamente responde a analgésicos de venta libre. El procedimiento alivia el dolor severo de la pulpitis con mucha más frecuencia de la que causa malestar.
¿Los tratamientos de conducto radicular causan enfermedades sistémicas?
No hay evidencia científica que vincule los tratamientos de conducto radicular realizados correctamente con cáncer, enfermedades cardíacas u otras condiciones sistémicas. Este mito se originó a partir de investigaciones desacreditadas hace casi un siglo.
La "teoría de la infección focal" propuso que las bacterias en la boca causan enfermedades en órganos distantes. Los primeros defensores afirmaron que los dientes tratados con conductos radiculares albergan bacterias que causan enfermedades sistémicas. Esta teoría guió miles de extracciones innecesarias a principios del siglo XX.
La investigación moderna refuta esta afirmación. Los tratamientos de conducto radicular bien realizados sellan completamente el sistema de conductos. El sistema inmunológico maneja la carga bacteriana mínima de cualquier infección residual. No hay estudios revisados por pares que vinculen los dientes tratados endodónticamente con enfermedades sistémicas.
¿Qué innovaciones futuras transformarán la endodoncia?
La terapia con células madre, la edición genética, los procedimientos guiados por IA y los materiales biomiméticos permitirán la regeneración biológica de la pulpa en lugar de su reemplazo por materiales sintéticos. Estos avances pueden eventualmente eliminar la necesidad de la extracción tradicional del nervio en muchos casos.
La endodoncia regenerativa representa la frontera más emocionante en el campo. En lugar de eliminar la pulpa y rellenar con materiales inertes, los investigadores buscan restaurar la vitalidad biológica.
¿Cómo cambiará la terapia con células madre el tratamiento?
El trasplante de células madre de pulpa dental (DPSCs) y células madre de dientes deciduos exfoliados humanos (SHED) regenerará tejido pulpar funcional, restaurará la defensa inmune y permitirá el desarrollo continuo de la raíz en dientes inmaduros.
Los ensayos clínicos demuestran la viabilidad de la regeneración de la pulpa. Nakashima et al. (2017) realizaron el primer ensayo clínico conforme a GMP utilizando células madre de pulpa dental movilizadas autólogas. Implantaron estas células en andamios de atelocolágeno con factores de crecimiento. Los pacientes recuperaron la sensibilidad pulpar en pocas semanas. La imagenología confirmó la formación de tejido similar a la dentina y la vascularización.
Xuan et al. (2018) realizaron un ensayo controlado aleatorio comparando el trasplante de células madre con la apexificación en dientes inmaduros. El grupo de células madre mostró un desarrollo radicular superior, cierre apical y formación de tejido similar a la pulpa. Huang et al. (2024) revisaron estos avances y concluyeron que las DPSCs muestran una mayor capacidad regenerativa que las células madre mesenquimatosas de médula ósea para aplicaciones dentales.
¿Qué papel jugará la terapia génica?
La edición genética utilizando la tecnología CRISPR/Cas9 puede activar genes dentinogénicos en células residentes. Este enfoque podría estimular la regeneración natural de la pulpa sin trasplante celular.
La terapia génica ofrece un enfoque sin células para la regeneración. Los investigadores proponen introducir genes que codifican proteínas morfogenéticas óseas (BMPs) y factor de crecimiento endotelial vascular (VEGF) en el espacio del conducto radicular. Estos genes estimularían a las células madre residentes a diferenciarse en odontoblastos y células endoteliales.
Los enfoques ex vivo implican la transducción de células madre recolectadas para sobreexpresar genes regenerativos antes de la implantación. Estas células modificadas producen una liberación sostenida de factores de crecimiento, mejorando la formación de tejido.
¿Cómo Mejorarán la IA y la Robótica los Resultados?
Los algoritmos de aprendizaje automático predecirán los resultados del tratamiento y optimizarán la selección de instrumentos. Los sistemas robóticos pueden realizar la conformación del canal con una precisión sobrehumana.
La inteligencia artificial ahora analiza escaneos CBCT para detectar variaciones en la anatomía del canal que los ojos humanos pasan por alto. Las aplicaciones futuras guiarán la instrumentación en tiempo real, alertando a los dentistas sobre perforaciones inminentes o riesgos de separación de instrumentos.
Las tecnologías de impresión 3D fabricarán andamios específicos para cada paciente que coincidan con las morfologías exactas de los conductos radiculares. Estos andamios apoyarán el crecimiento celular y la integración vascular.
Los materiales biocerámicos continúan avanzando. Los selladores más nuevos se unen químicamente a la dentina y proporcionan efectos antibacterianos. Estos materiales pueden eventualmente permitir la regeneración completa de la pulpa al apoyar la adhesión y diferenciación celular.
Conclusión
La extracción del nervio dental a través del tratamiento de conductos radiculares se considera una de las intervenciones más exitosas de la odontología. Este procedimiento preserva los dientes naturales que de otro modo requerirían extracción. Las técnicas modernas logran tasas de supervivencia del 97% a los 10 años y del 68% a los 37 años, según estudios longitudinales revisados por pares.
El procedimiento aborda las infecciones por biofilm bacteriano dentro de la cámara pulpar. Elimina las fuentes de dolor mientras mantiene la función dental. Los avances en instrumentación de níquel-titanio, visualización microscópica y selladores biocerámicos han transformado este tratamiento de un procedimiento temido a una terapia cómoda y predecible.
Los pacientes que enfrentan esta recomendación deben entender la base biológica del tratamiento. El papel de la pulpa disminuye después de la maduración del diente, permitiendo su extracción sin comprometer la viabilidad del diente. Existen alternativas, pero la preservación de la anatomía natural a través de la terapia endodóntica generalmente proporciona la solución más rentable y funcional a largo plazo.
Las innovaciones futuras prometen resultados aún mejores. La endodoncia regenerativa utilizando células madre puede eventualmente restaurar la vitalidad biológica en lugar de simplemente llenar conductos vacíos. La terapia génica y la ingeniería de tejidos pueden regenerar complejos pulpa-dentina indistinguibles del tejido natural.
El diagnóstico temprano sigue siendo crucial. Los pacientes que experimentan dolor dental persistente, sensibilidad a la temperatura o hinchazón deben buscar una evaluación inmediata. La demora aumenta la complejidad del tratamiento y reduce las probabilidades de éxito.
Referencias
Carvalho, Thiago Saads, y Lussi, Adrian. "Cambios Morfológicos, Histológicos y Funcionales Relacionados con la Edad en los Dientes." Journal of Oral Rehabilitation, vol. 44, no. 4, 2017, pp. 291-298.
Gillen, BM, et al. "Impacto del Tipo de Diente y del Procedimiento Endodóntico en el Resultado del Tratamiento de Conductos Radiculares: Una Revisión Sistemática." Journal of Endodontics, vol. 37, no. 4, 2011, pp. 449-457.
Gronthos, Stan, et al. "Células madre de pulpa dental humana postnatal (DPSCs) in vitro e in vivo." Actas de la Academia Nacional de Ciencias, vol. 97, no. 25, 2000, pp. 13625-13630.
Huang, Y, et al. "Células madre mesenquimatosas para la regeneración de pulpa dental: un estudio comparativo de diferentes fuentes." Células Madre Internacionales, 2024.
López-Valverde, Isabel, et al. "Supervivencia y éxito a largo plazo de los dientes tras el tratamiento de conducto radicular primario: una observación retrospectiva de 5 a 37 años." Investigaciones Clínicas Orales, vol. 27, no. 6, 2023, pp. 2545-2556.
Nakashima, Misako, et al. "Transplante de células madre de pulpa dental humana para la regeneración completa de la pulpa." Investigación y Terapia con Células Madre, vol. 8, no. 1, 2017, pp. 1-12.
Niki, Yogita, et al. "Anatomía, cabeza y cuello, pulpa dental." StatPearls, Publicación StatPearls, 2025, https://www.ncbi.nlm.nih.gov/books/NBK537112/.
Svensäter, G, y Bergenholtz, G. "Biofilms en infecciones endodónticas." Tópicos Endodónticos, vol. 9, no. 1, 2004, pp. 27-36.
Xuan, K, et al. "Células madre autólogas de dientes deciduos regeneran la pulpa dental después de la implantación en dientes lesionados." Ciencia Medicina Translacional, vol. 10, no. 455, 2018, eaaf3227.