El tratamiento de infecciones dentales requiere eliminar la fuente de la infección a través del drenaje, terapia de conducto radicular, o extracción. Los antibióticos sirven solo como terapia adyuvante para el compromiso sistémico. La intervención temprana previene complicaciones graves como sepsis y necrosis tisular.
¿Qué es una infección dental y por qué es importante?
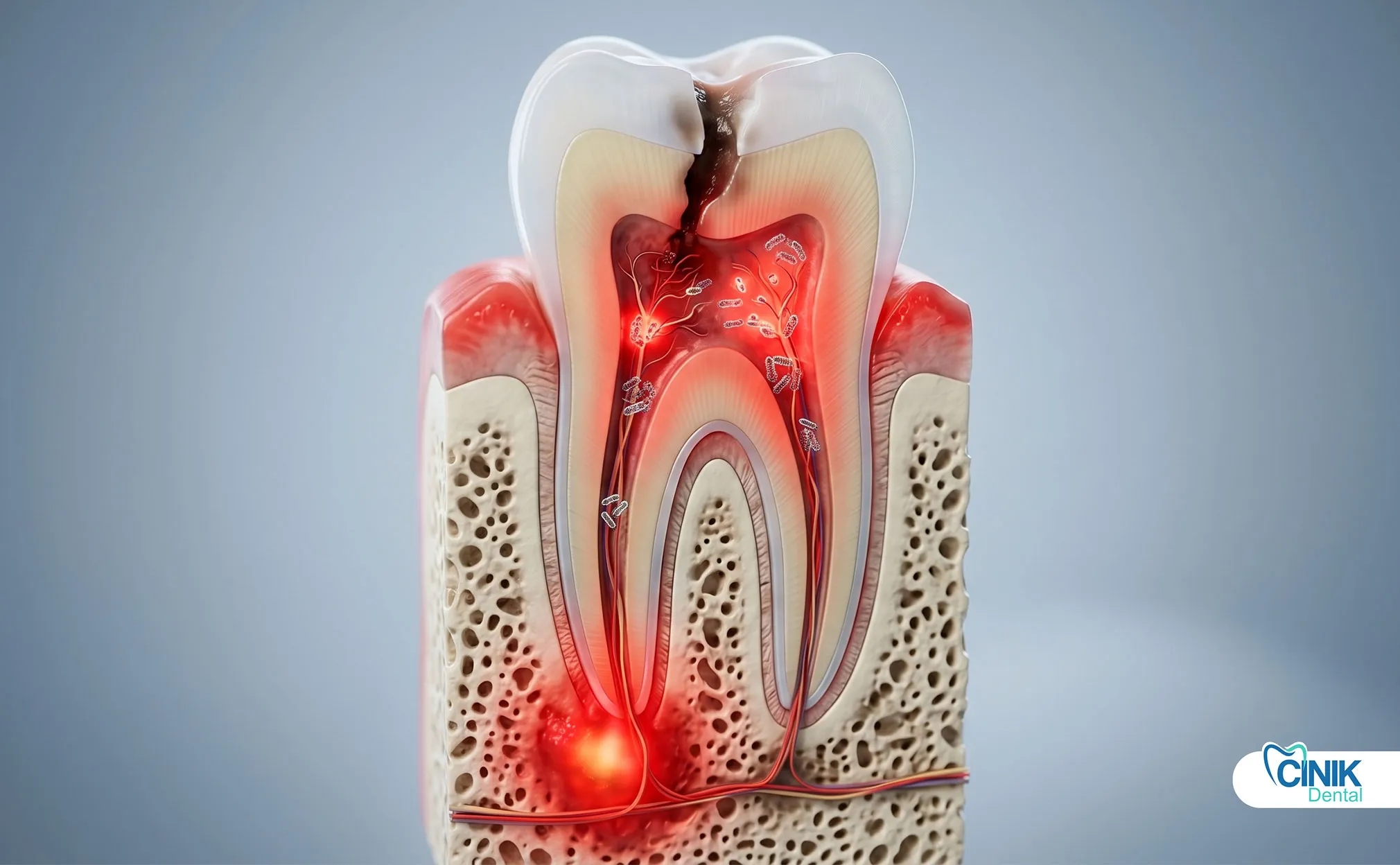
Una infección dental es una invasión bacteriana de la pulpa dental, los tejidos periodontales o el hueso circundante. Causa dolor severo, hinchazón y puede propagarse a los espacios faciales o al torrente sanguíneo sin un tratamiento rápido.
Una infección dental, clínicamente denominada infección odontogénica, se desarrolla cuando las bacterias penetran las capas protectoras de un diente o el tejido de las encías circundantes. Estas infecciones comienzan pequeñas pero pueden escalar a condiciones potencialmente mortales en cuestión de días. La Organización Mundial de la Salud reconoce las infecciones dentales como una carga significativa para la salud global, particularmente en poblaciones con acceso limitado a atención dental (Petersen, 2022).
Las infecciones dentales se dividen en tres categorías principales según la ubicación y el origen. Los abscesos periapicales se forman en la punta de la raíz cuando el tejido pulpar muere debido a caries profundas o trauma. Los abscesos periodontales se desarrollan en las estructuras de soporte de un diente afectado por enfermedad periodontal avanzada. Los abscesos gingivales permanecen confinados al margen de las encías, generalmente causados por la impactación de un cuerpo extraño.
La relevancia clínica de las infecciones dentales va más allá de la incomodidad oral. La investigación publicada en el Journal of Dental Research demuestra que las infecciones dentales no tratadas aumentan el riesgo cardiovascular, complican el manejo de la diabetes y elevan los marcadores inflamatorios sistémicos (Lockhart, 2019). En 2023, los departamentos de emergencia de los Estados Unidos trataron más de 2 millones de casos de infecciones dentales, con costos promedio de tratamiento que superan los $1,000 por visita cuando fue necesaria la hospitalización.
El diagnóstico temprano es importante porque las infecciones dentales siguen una progresión predecible. Las bacterias se multiplican en el espacio confinado de la raíz de un diente o en un bolsillo de encía. La presión aumenta. El tejido se hincha. La respuesta inmune desencadena fiebre y malestar. Sin intervención, la infección rompe las barreras locales y entra en espacios fasciales, canales linfáticos o el torrente sanguíneo.
El espectro de tratamiento abarca intervenciones locales y terapias sistémicas. Los enfoques locales, drenaje, terapia de conducto radicular, extracción, eliminan la fuente de la infección directamente. Los enfoques sistémicos, principalmente antibióticos, apoyan la defensa del cuerpo cuando la infección se propaga más allá del diente. El principio clave: el tratamiento local tiene prioridad. Los antibióticos por sí solos no pueden esterilizar un conducto radicular infectado o una cavidad de absceso.
Tipo de Infección | Ubicación | Causa Principal | Tratamiento Típico |
Absceso periapical | Ápice radicular | Necrosis pulpar | Endodoncia o extracción |
Absceso periodontal | Estructuras de soporte | Periodontitis avanzada | Drenaje + terapia periodontal |
Absceso gingival | Margen de encía | Impactación de cuerpo extraño | Drenaje + eliminación del irritante |
¿Qué causa el desarrollo de infecciones dentales?
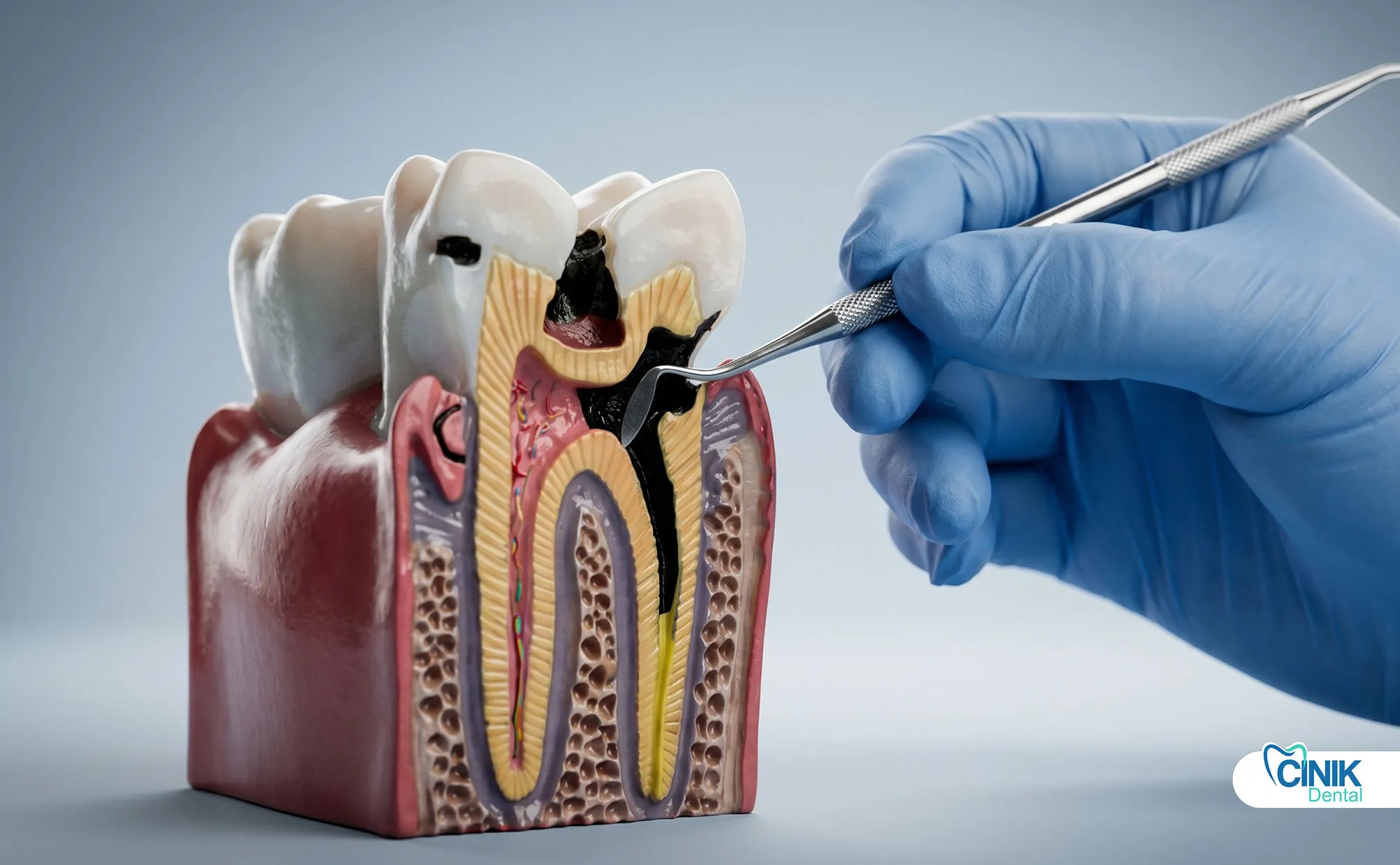
Las caries dentales, el trauma, las restauraciones fallidas y la enfermedad periodontal permiten que las bacterias invadan la pulpa dental y los tejidos circundantes. La formación de biofilm protege a las bacterias y acelera la destrucción del tejido.
¿Cómo invaden las bacterias los tejidos dentales?
Las bacterias entran a través de grietas en el esmalte, cavidades profundas o bolsas de encía. Forman biopelículas que resisten ataques inmunitarios y antibióticos, y luego destruyen la pulpa, el hueso y el tejido blando.
Las infecciones dentales comienzan con la colonización bacteriana. La cavidad oral alberga más de 700 especies bacterianas, pero solo un puñado causa infecciones invasivas. Streptococcus mutans inicia caries dental al metabolizar azúcares en ácido. Aggregatibacter actinomycetemcomitans y Porphyromonas gingivalis impulsan la destrucción periodontal. Cuando estos organismos rompen las defensas del esmalte o de las encías, acceden a la pulpa dental, una cámara estéril que contiene nervios y vasos sanguíneos.
Las caries dentales siguen siendo la principal causa de infección de la pulpa. Las cavidades no tratadas progresan a través del esmalte, la dentina y finalmente en la cámara pulpar. La pulpa responde con inflamación, pero las toxinas bacterianas y la presión eventualmente matan el tejido. La pulpa necrótica se convierte en un criadero para bacterias anaerobias.
El trauma acelera el riesgo de infección. Los dientes agrietados, incluso sin fracturas visibles, permiten la entrada de bacterias. Las restauraciones fallidas crean huecos microscópicos donde se acumulan las bacterias. Los tratamientos de conducto radicular que no alcanzan las ramas del canal dejan infección residual.
La enfermedad periodontal proporciona un camino alternativo. A medida que las bolsas de encía se profundizan, las bacterias migran por la superficie de la raíz. El sistema inmunológico ataca tanto a las bacterias como al tejido huésped, destruyendo el ligamento periodontal y el hueso alveolar. Las bolsas profundas que superan los 7 milímetros frecuentemente albergan bacterias formadoras de abscesos.
La formación de biopelículas complica el tratamiento. Las bacterias secretan polisacáridos extracelulares que forman una matriz protectora. Esta biopelícula protege a los organismos de los antibióticos, los anticuerpos de la saliva y las células inmunitarias. Dentro de una biopelícula, las bacterias se comunican a través de la detección de quorum y comparten genes de resistencia. La investigación de Seneviratne (2017) en Periodontology 2000 confirma que las bacterias incrustadas en biopelículas demuestran hasta 1,000 veces mayor resistencia a los antibióticos que las células planctónicas.
¿Cuáles son los principales tipos de infecciones dentales?
Los abscesos periapicales afectan las puntas de las raíces, los abscesos periodontales atacan las estructuras de soporte y los abscesos gingivales permanecen en los márgenes de las encías. Cada tipo requiere un momento y un enfoque de tratamiento diferentes.
Absceso Periapical: Esta infección se forma en el ápice de la raíz de un diente después de la necrosis pulpar. El pus se acumula en el hueso que rodea la punta de la raíz. Los pacientes experimentan un dolor pulsátil que empeora al acostarse. El diente se siente elevado en su alvéolo. Puede aparecer hinchazón en la piel facial si la infección perfora el hueso. Las radiografías muestran un área radiolúcida en el ápice de la raíz. La terapia de conducto radicular o la extracción resuelven la fuente de la infección.
Absceso Periodontal: Esta infección se desarrolla en un bolsillo periodontal preexistente. Causa un inicio rápido de dolor, hinchazón y secreción purulenta del margen de la encía. El diente afectado a menudo tiene movilidad debido a la pérdida ósea. Los abscesos periodontales requieren drenaje a través del bolsillo de la encía o una incisión externa. El raspado y alisado radicular siguen para reducir la profundidad del bolsillo.
Absceso Gingival: El tipo más superficial, confinado al margen de la encía. Cuerpos extraños, impacto de alimentos, cerdas de cepillo de dientes, fragmentos de hilo dental, desencadenan una infección localizada. El dolor permanece moderado. La hinchazón se mantiene limitada. El tratamiento implica la eliminación del objeto extraño y permitir el drenaje natural.
¿Cómo se Propaga una Infección Dental?
Las infecciones se propagan a través de planos de tejido local, espacios fasciales y, eventualmente, el torrente sanguíneo. La hinchazón facial, dificultad para tragar y fiebre señalan una progresión peligrosa.
La invasión del tejido local representa la primera fase. Las bacterias y los mediadores inflamatorios destruyen el hueso y el tejido blando circundantes. La cavidad del absceso se agranda. La presión comprime los nervios, causando un dolor intenso. Las enzimas como la colagenasa descomponen las barreras del tejido conectivo.
La implicación del espacio fascial marca una escalada peligrosa. La cara y el cuello contienen múltiples compartimentos de tejido conectivo separados por capas fasciales. Las bacterias siguen estos planos, creando hinchazones que amenazan la vida. La infección del espacio submandibular (angina de Ludwig) puede obstruir la vía aérea. El seno cavernoso, accesible a través del drenaje de la vena facial, corre el riesgo de trombosis e infección cerebral.
La diseminación sistémica ocurre cuando las bacterias entran en los vasos sanguíneos. La bacteriemia, la presencia de bacterias en la sangre, ocurre durante procedimientos dentales e incluso al cepillarse los dientes vigorosamente. En individuos sanos, las células inmunitarias eliminan la bacteriemia transitoria. En pacientes inmunocomprometidos o aquellos con infecciones severas, la bacteriemia progresa a sepsis. La endocarditis, infección de las válvulas cardíacas, representa un riesgo particular para los pacientes con válvulas protésicas o daño cardíaco previo.
Etapa de Propagación | Ubicación | Señales de Advertencia | Nivel de Riesgo |
Localizado | Diente y hueso inmediato | Dolor de diente, hinchazón leve | Bajo |
Regional | Espacios fasciales de la cara/cuello | Hinchazón facial, trismo, disfagia | Moderado-Alto |
Sistémico | Corriente sanguínea y órganos distantes | Fiebre, taquicardia, hipotensión, confusión | Crítico |
¿Cómo Reconocen y Diagnostican los Dentistas las Infecciones Dentales?
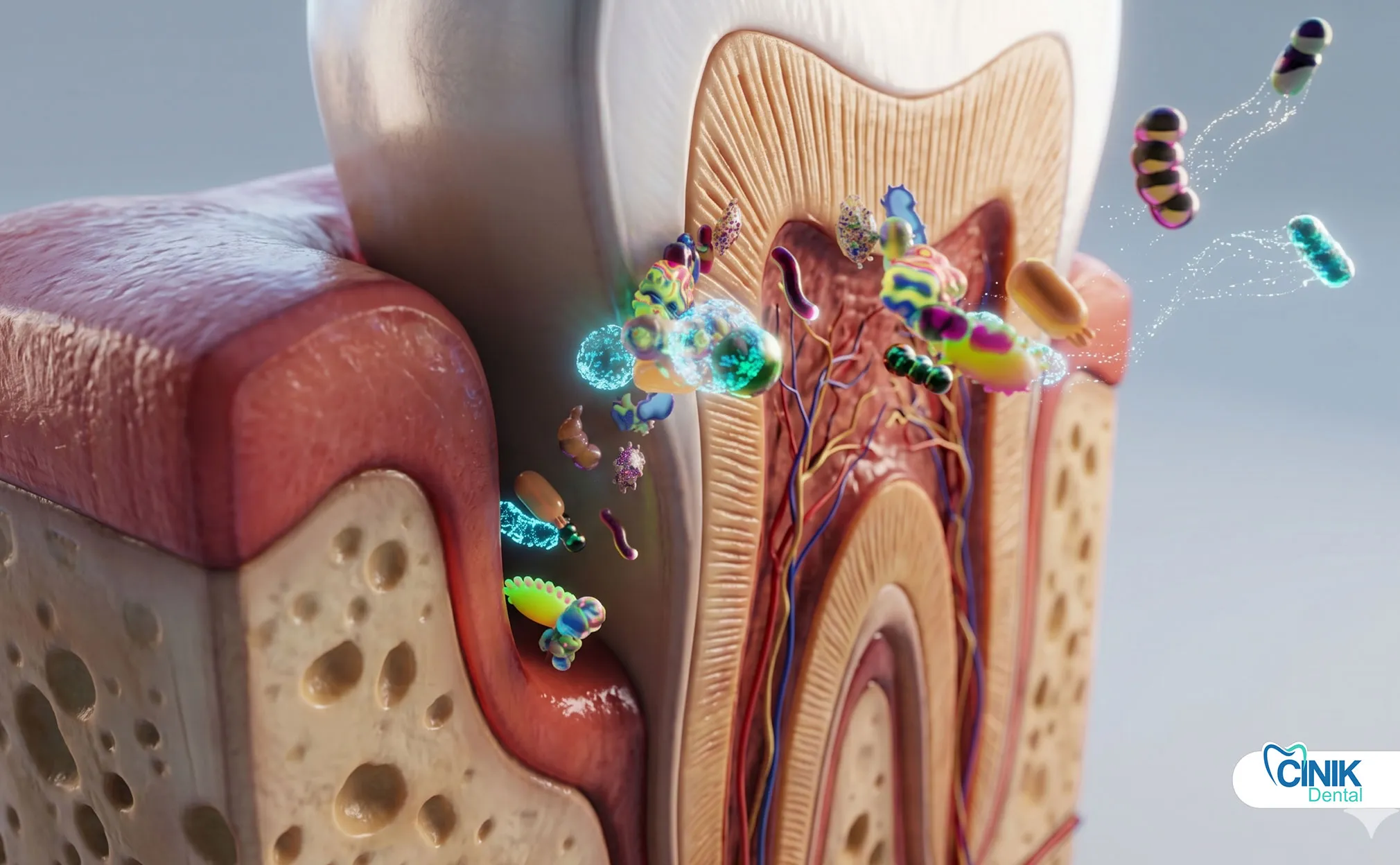
Los dentistas utilizan examen clínico, síntomas del paciente, imágenes radiográficas y pruebas de pulpa para identificar el tipo, la gravedad y la extensión de la infección.
¿Qué Síntomas Indican una Infección Dental?
Un dolor de muelas severo y pulsátil, hinchazón facial, enrojecimiento de las encías, sensibilidad a la temperatura y fiebre indican una infección activa que requiere evaluación inmediata.
El dolor sirve como el síntoma principal. Los dientes infectados producen un dolor profundo y pulsátil que los pacientes describen como implacable. El dolor se intensifica con la exposición al calor y puede disminuir brevemente con la aplicación de frío en la pulpitis temprana. Una vez que la pulpa se necrosa, la sensibilidad al frío desaparece, pero el dolor por presión aumenta a medida que se acumula pus bajo la raíz.
La hinchazón señala una infección en avance. Las infecciones tempranas causan hinchazón de las encías intraorales. A medida que aumenta la presión, la hinchazón se extiende a la piel facial. La piel se vuelve roja, caliente y tensa. Los pacientes pueden informar que la hinchazón apareció repentinamente y se expandió en horas.
Los síntomas sistémicos indican una infección en expansión. La fiebre por encima de 38°C (100.4°F) sugiere movilización inmune contra una carga bacteriana significativa. Malestar, pérdida de apetito y dificultad para abrir la boca (trismo) acompañan la implicación del espacio fascial. La dificultad para tragar (disfagia) o respirar representa un riesgo de emergencia en las vías respiratorias.
¿Qué herramientas de diagnóstico confirman infecciones dentales?
La palpación clínica, las pruebas de percusión, las radiografías, las tomografías CBCT y las pruebas eléctricas de pulpa confirman la presencia de infección, la ubicación y el estado de vitalidad del diente.
El examen clínico proporciona pistas inmediatas. Los dentistas palpan áreas hinchadas para evaluar la fluctuación; la hinchazón blanda y llena de líquido indica acumulación de pus. La prueba de percusión golpea los dientes con un instrumento romo; los dientes infectados transmiten vibraciones dolorosamente a través de los ligamentos periodontales inflamados. La prueba de movilidad identifica dientes con pérdida ósea avanzada debido a abscesos periodontales.
La imagen radiográfica visualiza la destrucción ósea. Las radiografías periapicales estándar muestran áreas radiolúcidas en las puntas de las raíces que indican pérdida ósea por abscesos periapicales. Las radiografías de aleta de mordida revelan caries profundas y niveles óseos periodontales. Sin embargo, las radiografías 2D no detectan infecciones tempranas ni anatomía compleja.
La tomografía computarizada de haz cónico (CBCT) ofrece visualización tridimensional. Esta tecnología detecta abscesos antes de que aparezcan cambios óseos visibles en las radiografías estándar. CBCT identifica canales radiculares adicionales, fracturas radiculares y patrones de propagación precisos en los espacios fasciales. La investigación de Patel (2019) en el International Endodontic Journal confirma que CBCT detecta un 40% más de lesiones periapicales que la radiografía convencional.
Las pruebas de vitalidad de la pulpa distinguen entre condiciones reversibles e irreversibles. Los medidores eléctricos de pulpa estimulan la respuesta nerviosa; los dientes no vitales no muestran sensación. La prueba de frío con spray refrigerante evalúa la función nerviosa. Una pulpa necrótica no responde al frío, mientras que una pulpa vital inflamada produce un dolor exagerado y persistente.
¿Cuáles son los principios fundamentales del tratamiento de infecciones dentales?
Elimina primero la fuente de la infección a través del drenaje, el tratamiento de conducto o la extracción. Usa antibióticos solo cuando la infección se propague sistémicamente. Nunca confíes solo en los antibióticos.
El objetivo principal del tratamiento de infecciones dentales es el control de la fuente. Los antibióticos circulan por la sangre pero no pueden penetrar en las cámaras de pulpa necrótica, las cavidades de abscesos o las colonias bacterianas protegidas por biofilm. La fuente de la infección, una pulpa muerta, pus acumulado o un bolsillo periodontal enfermo, debe ser eliminada físicamente.
El drenaje y el desbridamiento forman la base del control de la fuente. Una cavidad de absceso contiene pus, toxinas bacterianas y líquido inflamatorio. La incisión y el drenaje liberan este material, reduciendo la presión y la carga bacteriana. La terapia de conducto radicular elimina el tejido pulpar infectado del interior del diente. La extracción elimina toda la estructura infectada.
Los enfoques conservadores preservan los dientes naturales cuando es posible. La terapia de conducto radicular salva dientes con abscesos periapicales si queda suficiente estructura dental para la restauración. Los abscesos periodontales a menudo responden al drenaje combinado con limpieza profunda. La extracción se vuelve necesaria cuando los dientes tienen fracturas por debajo de la línea de las encías, pérdida ósea severa o tratamiento de conducto radicular fallido previamente.
Los enfoques quirúrgicos abordan casos complejos. La apicoectomía, la extracción quirúrgica de la punta de la raíz, salva dientes con infección periapical persistente después de la terapia de conducto radicular. La cirugía periodontal reduce los bolsillos profundos que albergan abscesos recurrentes. La cirugía en un hospital maneja infecciones del espacio fascial que requieren protección de las vías respiratorias.
Perspectiva Clínica Clave: El tratamiento local tiene prioridad sobre los antibióticos. Un paciente con un absceso dental que recibe solo antibióticos experimenta un alivio temporal de los síntomas pero enfrenta una recurrencia garantizada. La cavidad del absceso permanece. Las bacterias se repoblan. Sin drenaje o tratamiento dental, la infección regresa, a menudo con organismos resistentes a los antibióticos.
¿Qué Procedimientos Dentales Tratan Infecciones Primero?
Los dentistas priorizan la incisión y el drenaje para los abscesos, la terapia de conducto radicular para los dientes que se pueden salvar y la extracción para los dientes no restaurables. Estos procedimientos eliminan las fuentes de infección directamente.
¿Cómo Funciona el Drenaje de Abscesos?
El dentista adormece el área, hace una pequeña incisión en el absceso y permite que el pus drene. Esto reduce inmediatamente el dolor y la presión mientras elimina la carga bacteriana.
La incisión y el drenaje proporcionan el alivio del dolor más rápido para los abscesos agudos. El procedimiento requiere anestesia local. El dentista identifica el área de hinchazón más fluctuante (más blanda, más llena de líquido). Una incisión con un escalpelo, típicamente de 1-2 centímetros, penetra hasta la cavidad del absceso. El pus evacua bajo presión. El dentista puede insertar un pequeño drenaje de goma para mantener la apertura durante 24-48 horas.
Los beneficios inmediatos incluyen la reducción de la presión y el alivio del dolor. Los pacientes a menudo informan una mejora dramática en pocas horas. El drenaje también elimina el inóculo bacteriano, reduciendo la carga bacteriana sistémica. El procedimiento toma de 15 a 30 minutos en un consultorio dental.
El cuidado posterior al drenaje implica enjuagues de solución salina tibia para mantener la permeabilidad del drenaje. Los pacientes continúan con antibióticos si existen síntomas sistémicos. El tratamiento dental definitivo, conducto radicular o extracción, sigue una vez que la hinchazón aguda disminuye, generalmente dentro de 3-7 días.
¿Cuándo Salva la Terapia de Conducto Radicular un Diente Infectado?
La terapia de conducto radicular elimina la pulpa infectada, desinfecta los conductos radiculares y sella el diente. Preserva los dientes naturales cuando queda suficiente estructura para la restauración de coronas.
La terapia de conducto radicular aborda los abscesos periapicales al eliminar el contenido de la cámara pulpar infectada. El dentista crea una abertura de acceso a través de la corona del diente. Los instrumentos eliminan el tejido pulpar, los desechos necróticos y el biofilm bacteriano del sistema de conductos. Los irrigantes químicos, hipoclorito de sodio y clorhexidina, desinfectan las paredes del conducto.
El procedimiento requiere de 1 a 3 citas dependiendo de la gravedad de la infección. La primera visita se centra en la eliminación de la pulpa y el drenaje del absceso a través del diente. El dentista coloca un medicamento antibacteriano dentro del conducto y sella con un empaste temporal. La segunda visita confirma el control de la infección antes de llenar los conductos con gutapercha, un material similar al caucho. Una corona permanente restaura la resistencia del diente.
Las tasas de éxito superan el 90% para los tratamientos de conducto radicular primarios. La investigación de Ng (2011) en el International Endodontic Journal informa un 94% de supervivencia a los 4 años para dientes con abscesos periapicales tratados con terapia de conducto radicular y restauración de coronas. El fracaso generalmente proviene de ramas de conducto no detectadas, biofilm bacteriano persistente o filtración coronal.
¿Cuándo debe extraerse un diente infectado?
La extracción se vuelve necesaria cuando los dientes tienen fracturas por debajo de la línea de las encías, pérdida ósea severa, fracaso en el retratamiento del conducto radicular o estructura insuficiente para la restauración.
La extracción dental proporciona eliminación definitiva de la infección cuando la preservación es imposible. Las fracturas radiculares verticales, que se extienden por debajo de la línea de las encías, impiden el sellado bacteriano independientemente del tratamiento. La enfermedad periodontal severa que destruye más del 50% del hueso de soporte hace que los dientes no sean restaurables. El fracaso en el retratamiento del conducto radicular, particularmente con lesiones periapicales persistentes, puede justificar la extracción y el reemplazo por implante.
El procedimiento de extracción para dientes infectados requiere cuidado para prevenir la propagación bacteriana. El dentista puede prescribir antibióticos preoperatorios para pacientes inmunocomprometidos o infecciones severas. La anestesia local con vasoconstrictor controla el sangrado. El dentista eleva el diente de su alvéolo, elimina el tejido de granulación de la base del alvéolo y asegura una completa desbridación.
La curación post-extracción toma de 1 a 2 semanas para el cierre de tejidos blandos. La remodelación ósea continúa durante 3-6 meses. La colocación inmediata de implantes, realizada en casos selectos, reduce el tiempo de tratamiento pero requiere sitios de extracción libres de infección.
Nota basada en evidencia: Los procedimientos dentales definitivos siguen siendo esenciales porque los antibióticos no pueden eliminar las fuentes de infección. Una revisión sistemática de Cope (2014) en el British Dental Journal analizó 22 ensayos clínicos y concluyó que los antibióticos sin control de la fuente no proporcionan ningún beneficio sostenido para los abscesos dentales. La recurrencia de síntomas ocurre en el 100% de los casos dentro de semanas.
Procedimiento | Indicación | Tasa de Éxito | Tiempo de Recuperación |
Incisión y drenaje | Absceso agudo con hinchazón fluctuante | Alivio inmediato; requiere seguimiento | 2-3 días |
Tratamiento de conducto radicular | Absceso periapical, diente restaurable | 90-95% a 5 años | 1-2 semanas |
Extracción dental | Diente no restaurable, tratamiento fallido | 100% eliminación de infección | 1-2 semanas de tejido blando |
¿Cómo apoyan los antibióticos el tratamiento de infecciones dentales?
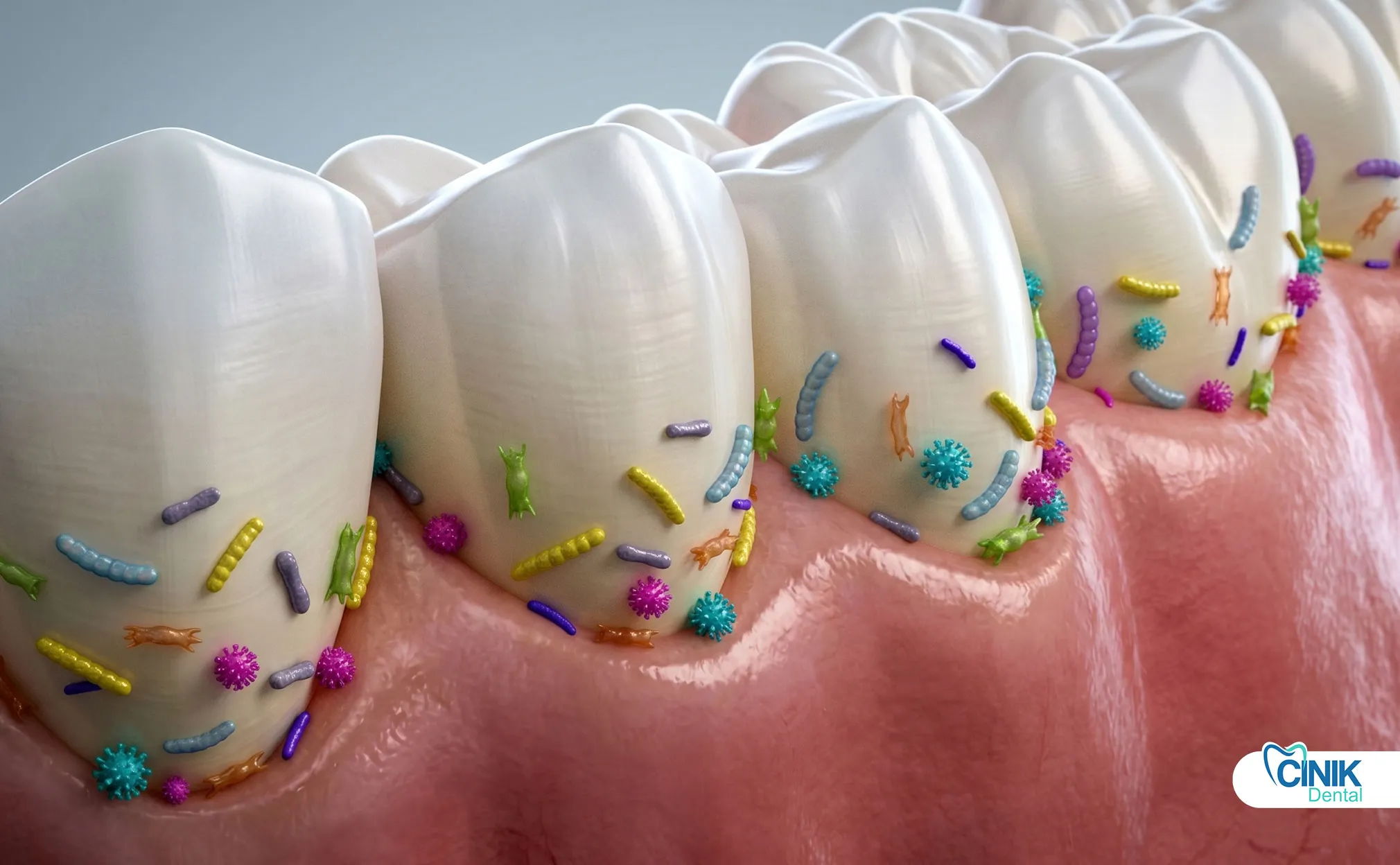
Los antibióticos tratan infecciones en expansión con fiebre, celulitis facial o inmunocompromiso. Nunca reemplazan el drenaje o el tratamiento dental. La amoxicilina sigue siendo la primera opción.
¿Cuándo prescriben los dentistas antibióticos?
Los dentistas prescriben antibióticos para síntomas sistémicos, celulitis en expansión, pacientes inmunocomprometidos o cuando los procedimientos dentales inmediatos son imposibles.
Los antibióticos sirven como un papel adjunto en el manejo de infecciones dentales. No curan los abscesos dentales. Controlan la propagación bacteriana cuando la infección excede el contención local. Las indicaciones específicas incluyen:
Involucramiento sistémico: Fiebre por encima de 38°C, malestar o linfadenopatía indican una carga bacteriana que excede la capacidad inmune local. Los antibióticos reducen el riesgo de bacteriemia y apoyan la recuperación sistémica.
Infección en expansión: Celulitis, enrojecimiento difuso de la piel sin absceso localizado, requiere antibióticos porque el drenaje no es posible. Infecciones que se extienden a espacios fasciales necesitan una cobertura antibiótica agresiva mientras se espera la intervención quirúrgica.
Estados inmunocomprometidos: Pacientes con diabetes, VIH, quimioterapia o trasplantes de órganos enfrentan un mayor riesgo de sepsis. La intervención temprana con antibióticos protege a estas poblaciones vulnerables.
Profilaxis de procedimientos: Ciertas condiciones médicas requieren cobertura antibiótica antes de procedimientos dentales para prevenir infecciones en sitios distantes. Válvulas cardíacas protésicas, endocarditis infecciosa previa y algunos implantes ortopédicos caen en esta categoría.
Principio Importante: Los antibióticos son adjuntos, no terapia primaria. Un paciente con un absceso dental localizado y sin síntomas sistémicos no necesita antibióticos. El dentista realiza el drenaje y el tratamiento del diente. Agregar antibióticos no proporciona beneficio y contribuye a la resistencia.
¿Qué Antibióticos Funcionan Mejor para Infecciones Dentales?
La amoxicilina sigue siendo el antibiótico de primera línea debido a su efectividad contra patógenos orales típicos y excelente tolerabilidad. La penicilina V sirve como alternativa.
La amoxicilina domina la prescripción de antibióticos dentales de primera línea. Esta aminopenicilina cubre los cocos gram positivos (Especies de Streptococcus) y anaerobios gram negativos (Prevotella, Fusobacterium) que causan la mayoría de las infecciones dentales. La absorción oral alcanza el 90%, produciendo niveles sanguíneos confiables. La dosis estándar para adultos es de 500 mg tres veces al día durante 5-7 días.
Evidencia Clínica: Un ensayo controlado aleatorio de Matthews (2016) en el Journal of Antimicrobial Chemotherapy comparó amoxicilina con placebo para abscesos dentales. Ambos grupos recibieron incisión y drenaje. La amoxicilina redujo la hinchazón post-procedimiento en un 35% y acortó la recuperación en 2 días. Sin embargo, las tasas de curación a los 30 días fueron idénticas, confirmando que el control de la fuente, no los antibióticos, determina los resultados.
La penicilina V proporciona una alternativa con un espectro más estrecho. Esta fenoximetilpenicilina resiste la degradación por ácido gástrico, lo que la hace adecuada para uso oral. La dosis típica es de 500 mg cuatro veces al día. La penicilina V cubre la mayoría de los patógenos odontogénicos, pero carece de cobertura para anaerobios gram negativos en comparación con la amoxicilina.
¿Qué Antibióticos Ayudan Cuando Fallan los Medicamentos de Primera Línea?
El metronidazol tiene como objetivo los anaerobios y se combina con amoxicilina para infecciones severas. La clindamicina reemplaza a la penicilina en pacientes alérgicos. La azitromicina ofrece otra alternativa.
El metronidazol tiene como objetivo específico las bacterias anaerobias obligadas. Estos organismos dominan la pulpa necrótica y los bolsillos periodontales profundos. El metronidazol solo no cubre los estreptococos aerobios, por lo que los dentistas a menudo lo combinan con amoxicilina para infecciones severas y mixtas. La dosis es de 400 mg tres veces al día. Los pacientes deben evitar el alcohol durante el tratamiento y durante 48 horas después de la finalización debido a reacciones similares al disulfiram.
La clindamicina sirve a los pacientes alérgicos a la penicilina. Este antibiótico lincosamida cubre organismos gram positivos y anaerobios de manera efectiva. La dosis es de 300 mg cuatro veces al día. Los dentistas reservan la clindamicina para verdaderas alergias a la penicilina porque conlleva un mayor riesgo de Clostridioides difficile colitis, una infección intestinal grave.
La azitromicina proporciona otra alternativa para pacientes alérgicos a la penicilina. Este antibiótico macrólido ofrece una dosificación conveniente, 500 mg diarios durante 3 días, debido a su larga vida media en los tejidos. Sin embargo, el aumento de la resistencia entre los estreptococos orales limita su fiabilidad. Los dentistas utilizan azitromicina cuando la clindamicina está contraindicada.
¿Por qué la resistencia a los antibióticos amenaza el tratamiento dental?
La sobreprescripción de antibióticos dentales acelera la resistencia bacteriana. Las directrices ahora desaconsejan el uso rutinario de antibióticos para infecciones localizadas sin diseminación sistémica.
La resistencia a los antibióticos socava la gestión de infecciones dentales. Los Centros para el Control y la Prevención de Enfermedades identifican la prescripción dental como un contribuyente significativo al uso innecesario de antibióticos. Los estudios estiman que el 30-50% de las recetas de antibióticos dentales son innecesarias, dadas para condiciones donde el control de la fuente por sí solo es suficiente.
Las consecuencias se extienden más allá de los pacientes individuales. Las bacterias resistentes colonizan la cavidad oral y se propagan a los miembros de la familia, instalaciones de salud y comunidades. Las cepas de Streptococcus pneumoniae y Staphylococcus aureus resistentes a la penicilina y la clindamicina aparecen cada vez más en infecciones dentales.
Los programas de administración de antibióticos tienen como objetivo la sobreprescripción dental. La Asociación Dental Americana actualizó las directrices en 2019, afirmando explícitamente que los antibióticos no están indicados para hinchazones intraorales localizadas sin involucramiento sistémico. Las directrices enfatizan: "El método principal para tratar una infección dental debe ser el control de la fuente."
La terapia dirigida reemplaza la prescripción empírica en casos recurrentes o complejos. El cultivo y las pruebas de sensibilidad identifican bacterias específicas y sus patrones de resistencia. Este enfoque, estándar en entornos hospitalarios, se está volviendo más común en la práctica dental para pacientes inmunocomprometidos o fracasos en el tratamiento.
Antibiótico | Espectro | Dosis típica | Mejor para |
Amoxicilina | Amplio (aerobios + anaerobios) | 500 mg TID x 5-7 días | Primera línea, la mayoría de las infecciones |
Penicilina V | Estrecho (aerobios) | 500 mg QID x 5-7 días | Infecciones leves, preferencia por penicilina |
Metronidazol | Solo anaerobios | 400 mg TID x 5-7 días | Combinado con amoxicilina para casos severos |
Clindamicina | Aerobios + anaerobios | 300 mg QID x 5-7 días | Alergia a la penicilina |
Azitromicina | Amplio | 500 mg diarios x 3 días | Alergia a la penicilina, contraindicación de clindamicina |
¿Cómo manejan los dentistas el dolor durante el tratamiento de infecciones?
Los AINE como el ibuprofeno proporcionan un alivio del dolor dental superior en comparación con los opioides. El paracetamol ofrece una alternativa para los pacientes que no pueden tomar AINE.
El manejo del dolor en infecciones dentales sigue un enfoque multimodal. Los medicamentos antiinflamatorios no esteroides (AINE) son la piedra angular. Ibuprofeno, 400-600 mg cada 6-8 horas, reduce la inflamación en el sitio de la infección mientras proporciona analgesia. La investigación de Moore (2015) en la Base de Datos Cochrane de Revisiones Sistemáticas confirma que el ibuprofeno 400 mg proporciona un mejor alivio del dolor que la codeína 60 mg para el dolor dental, con menos efectos secundarios.
El paracetamol sirve a los pacientes con contraindicaciones a los AINE, enfermedad ulcerosa péptica, terapia anticoagulante o insuficiencia renal. La dosis es de 500-1000 mg cada 6 horas, sin exceder 3000 mg diarios. El paracetamol carece de acción antiinflamatoria pero proporciona analgesia efectiva.
La terapia combinada mejora el control del dolor. Alternar ibuprofeno y paracetamol mantiene niveles estables de medicamentos. Algunos estudios sugieren que la administración concurrente proporciona un alivio superior al de cualquiera de los medicamentos por separado, aunque los pacientes deben seguir cuidadosamente los intervalos de dosificación para evitar sobredosis.
La prescripción de opioides ha disminuido drásticamente en la práctica dental. La epidemia de opioides provocó una reevaluación de los protocolos de dolor dental. Las pautas actuales reservan los opioides para el dolor postquirúrgico severo que no responde a los AINE. Cuando se prescriben, los dentistas limitan las cantidades a 3-5 días y combinan con AINE para reducir los requerimientos de opioides.
Las medidas de cuidado de apoyo complementan la medicación. La hidratación mantiene el flujo de saliva y apoya la función inmunológica. Los enjuagues con solución salina tibia (media cucharadita de sal en agua tibia, enjuagado durante 30 segundos) reducen la carga bacteriana y promueven el drenaje de los bolsillos de las encías. Los alimentos blandos previenen la irritación mecánica de los tejidos infectados. Elevar la cabeza durante el sueño reduce el flujo sanguíneo a los tejidos faciales hinchados, disminuyendo el dolor pulsátil.
¿Qué sucede cuando las infecciones dentales no se tratan?
Las infecciones dentales no tratadas causan destrucción ósea local, necrosis tisular y complicaciones sistémicas potencialmente fatales, incluyendo sepsis, obstrucción de las vías respiratorias y absceso cerebral.
¿Qué daño local causan las infecciones no tratadas?
Las infecciones no tratadas destruyen el hueso de la mandíbula (osteomielitis), matan el tejido blando (necrosis) y se propagan a través de los espacios faciales causando desfiguración y pérdida funcional.
La osteomielitis representa una infección ósea por siembra bacteriana. El hueso de la mandíbula desarrolla áreas de hueso muerto (secuestros) rodeadas de tejido inflamado. La osteomielitis crónica causa dolor persistente, fístulas drenantes y fracturas patológicas. El tratamiento requiere antibióticos prolongados (4-6 semanas) y la extracción quirúrgica del hueso muerto. La terapia de oxígeno hiperbárico apoya la curación en casos refractarios.
La necrosis del tejido ocurre cuando la infección compromete el suministro de sangre. El paladar, la lengua o la piel facial pueden desarrollar áreas negras y desvitalizadas que requieren desbridamiento quirúrgico. La fascitis necrotizante, aunque rara en infecciones dentales, destruye rápidamente los planos de tejido y exige intervención quirúrgica de emergencia.
Las infecciones de los espacios faciales distorsionan la anatomía. Los espacios submandibulares, pterigomandibulares y caninos se hinchan dramáticamente. Los pacientes desarrollan una apariencia de "cuello de toro" debido a la participación bilateral submandibular. El trismo, bloqueo de la mandíbula por inflamación muscular, impide comer y hablar.
¿Qué riesgos sistémicos crean las infecciones dentales?
Las bacterias de las infecciones dentales entran en el torrente sanguíneo, causando sepsis, infección de válvulas cardíacas y abscesos distales. La obstrucción de las vías respiratorias por la hinchazón del cuello puede causar asfixia.
La sepsis representa la complicación sistémica más temida. Las toxinas bacterianas desencadenan una activación inmune masiva. Fiebre, ritmo cardíaco rápido, respiración rápida y confusión son señales de sepsis. La presión arterial cae. Los órganos fallan. El shock séptico conlleva una mortalidad del 40% incluso con tratamiento en cuidados intensivos. Las infecciones dentales causan el 10-15% de todos los casos de sepsis facial.
La obstrucción de las vías respiratorias amenaza la vida en cuestión de horas. La angina de Ludwig, una infección del espacio submandibular bilateral, empuja la lengua hacia arriba y hacia atrás. El suelo de la boca se vuelve rígido. Los pacientes babean, no pueden tragar saliva y desarrollan estridor (respiración ruidosa). La traqueostomía de emergencia o la intubación aseguran la vía aérea antes del drenaje quirúrgico.
El absceso cerebral, aunque raro, sigue a la propagación hematógena o la extensión directa a través de los huesos del cráneo. Las infecciones de los dientes frontales acceden al lóbulo frontal. Las infecciones maxilares alcanzan el lóbulo temporal. Los abscesos cerebrales causan dolor de cabeza, convulsiones, debilidad focal y alteración del estado mental. El drenaje neuroquirúrgico y los antibióticos prolongados (6-8 semanas) tratan esta complicación.
La endocarditis afecta las válvulas cardíacas, particularmente en pacientes con enfermedad valvular preexistente o válvulas protésicas. Estreptococos viridans de infecciones dentales se adhieren al endocardio dañado, formando vegetaciones que embolizan al cerebro, riñones y extremidades. Los antibióticos profilácticos antes de los procedimientos dentales previenen esta complicación en pacientes de alto riesgo.
Complicación | Mecanismo | Riesgo de mortalidad | Tratamiento requerido |
Osteomielitis | Infección y necrosis ósea | Bajo | Cirugía + 4-6 semanas de antibióticos |
Sepsis | Propagación bacteriana en el torrente sanguíneo | 15-40% | Cuidado en UCI, antibióticos IV, control de la fuente |
Angina de Ludwig | Infección submandibular bilateral | 10-20% | Vía aérea de emergencia + drenaje quirúrgico |
Absceso cerebral | Propagación hematógena o directa | 10-30% | Neurocirugía + 6-8 semanas de antibióticos |
¿Cómo deben recibir atención las poblaciones especiales para infecciones dentales?
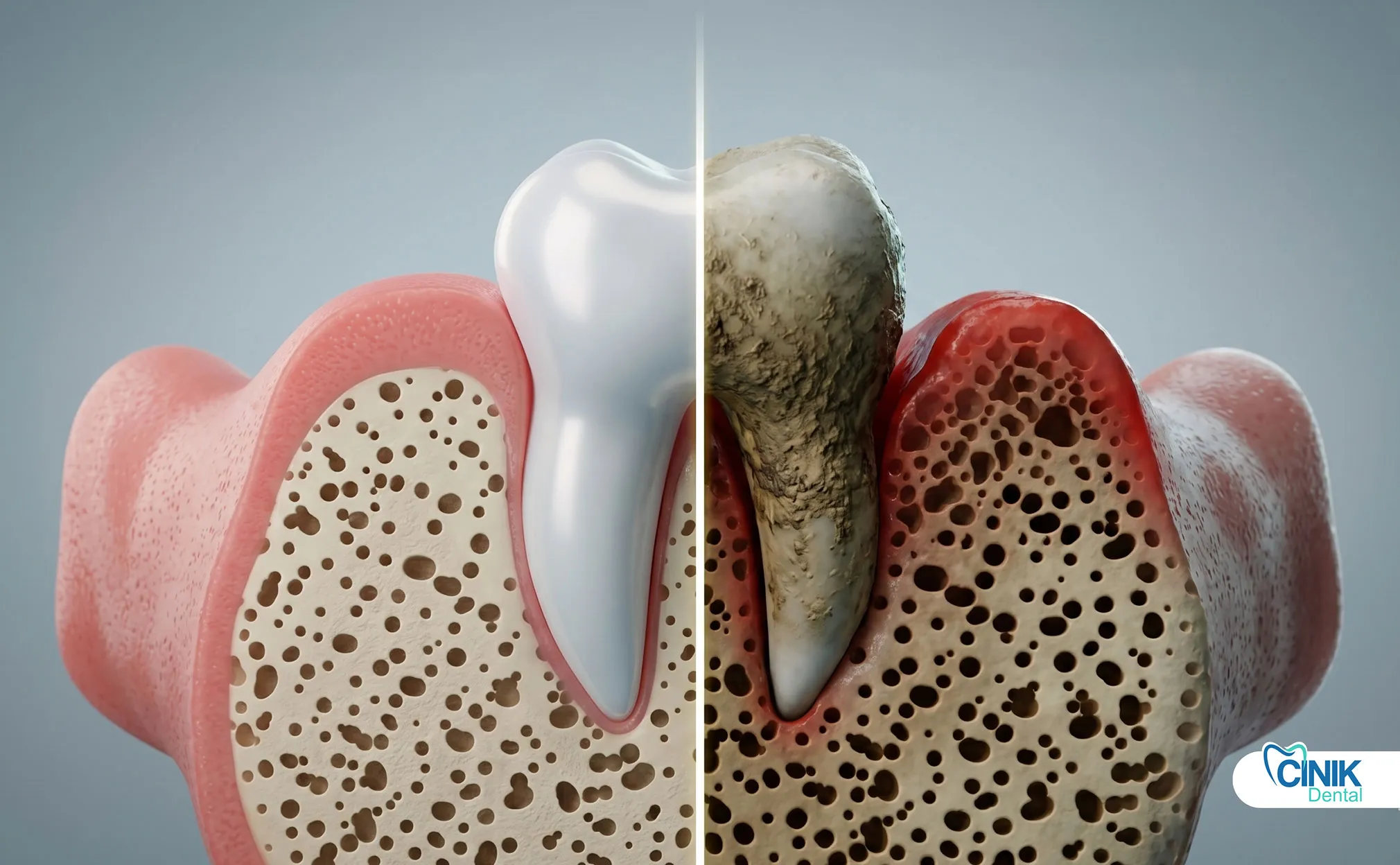
Los pacientes inmunocomprometidos, pediátricos y ancianos necesitan enfoques de tratamiento modificados, intervención antibiótica temprana, ajuste de dosis de medicamentos y monitoreo más cercano.
¿Qué cuidado adicional necesitan los pacientes inmunocomprometidos?
Los pacientes inmunocomprometidos enfrentan un mayor riesgo de propagación sistémica. Necesitan iniciar antibióticos más temprano, cobertura más amplia, tratamiento en hospital para infecciones moderadas y monitoreo de recuperación más prolongado.
Los estados inmunocomprometidos incluyen diabetes mellitus, VIH/SIDA, quimioterapia, trasplante de órganos, uso crónico de corticosteroides y deficiencias inmunitarias heredadas. Estas condiciones afectan la función de los neutrófilos, la producción de anticuerpos o la inmunidad mediada por células, defensas críticas contra patógenos dentales.
El mayor riesgo de propagación de infecciones exige un manejo agresivo. Un absceso localizado en un paciente sano puede permanecer confinado durante días. El mismo absceso en un paciente con quimioterapia neutropénico puede progresar a sepsis en cuestión de horas. Los dentistas bajan los umbrales para la iniciación de antibióticos y la derivación al hospital.
La intervención antibiótica temprana utiliza cobertura de espectro más amplio. Mientras que los pacientes sanos reciben solo amoxicilina, los pacientes inmunocomprometidos pueden necesitar amoxicilina-clavulonato (Augmentin) para una mejor cobertura de anaerobios, o incluso antibióticos intravenosos para la admisión hospitalaria.
El tratamiento en hospital se vuelve necesario para infecciones que serían manejadas en consultorio en pacientes sanos. El acceso IV proporciona una entrega confiable de medicamentos. El monitoreo sigue la temperatura, los recuentos de glóbulos blancos y los marcadores inflamatorios. Los equipos quirúrgicos están listos para el manejo de la vía aérea si se desarrolla la implicación del espacio fascial.
¿Cómo ajustan los dentistas el tratamiento para niños y pacientes ancianos?
Los niños requieren dosificación basada en el peso y manejo del comportamiento. Los pacientes ancianos necesitan evaluación de la función renal, revisión de interacciones medicamentosas y consideración de comorbilidades.
Las infecciones dentales pediátricas presentan desafíos únicos. Los dientes primarios con abscesos periapicales a menudo requieren extracción en lugar de terapia de conducto radicular debido a la anatomía compleja de las raíces y la línea de tiempo de exfoliación que se aproxima. Los mantenedores de espacio previenen complicaciones ortodónticas después de la pérdida prematura de dientes. La dosificación de antibióticos sigue cálculos basados en el peso, amoxicilina 50 mg/kg/día dividida en 3 dosis.
El manejo del comportamiento permite el tratamiento en pacientes jóvenes. La anestesia local requiere una técnica cuidadosa para evitar la inyección intravascular en pacientes pequeños. La sedación o anestesia general puede ser necesaria para procedimientos extensos. Los padres juegan roles cruciales en el cuidado post-tratamiento, asegurando la adherencia a la medicación y modificaciones dietéticas.
Los pacientes geriátricos presentan diferentes complejidades. La polifarmacia aumenta los riesgos de interacciones medicamentosas. Los antibióticos pueden interactuar con la warfarina (la clindamicina y el metronidazol potencian los efectos), las estatinas o los medicamentos cardíacos. El deterioro de la función renal requiere ajustes de dosis para los medicamentos eliminados por los riñones, como la amoxicilina y el metronidazol.
El deterioro cognitivo complica la comunicación de los síntomas. Los pacientes ancianos con demencia pueden no comunicar el dolor de manera efectiva. Los cuidadores deben observar cambios de comportamiento, rechazo de alimentos, contacto facial o agitación, como indicadores de infección. La planificación del tratamiento prioriza la simplicidad y durabilidad sobre enfoques idealistas.
Población | Consideración clave | Ajuste de antibióticos | Necesidades especiales |
Inmunocomprometidos | Alto riesgo de propagación | Espectro más amplio, inicio más temprano | Umbral de referencia hospitalaria reducido |
Pediátrico | Crecimiento y desarrollo | Dosis basada en el peso | Manejo del comportamiento, mantenimiento del espacio |
Geriátrico | Comorbilidades, polifarmacia | Ajuste de dosis renal | Revisión de interacciones medicamentosas, evaluación cognitiva |
¿Cómo pueden las personas prevenir infecciones dentales?
El cepillado y el uso de hilo dental diarios, chequeos dentales regulares cada 6 meses, tratamiento inmediato de caries y manejo de enfermedades de las encías previenen las condiciones que conducen a infecciones dentales.
La prevención de infecciones dentales se dirige a las causas raíz: caries y enfermedad periodontal. Las prácticas de higiene oral interrumpen la formación de biofilm bacteriano antes de que cause daño a los tejidos. La Asociación Dental Americana recomienda cepillarse dos veces al día con pasta de dientes con flúor durante 2 minutos, utilizando un cepillo de cerdas suaves en movimientos circulares suaves en la línea de las encías.
El uso de hilo dental alcanza áreas que los cepillos no pueden, entre los dientes y debajo de los márgenes de las encías donde se colonizan los patógenos periodontales. Los irrigadores dentales y los cepillos interdentales ayudan a los pacientes con destreza manual limitada. Los enjuagues bucales que contienen clorhexidina o aceites esenciales reducen la carga bacteriana, pero no reemplazan la limpieza mecánica.
Los chequeos dentales regulares permiten una intervención temprana. Las limpiezas profesionales eliminan el cálculo (sarro) que alberga bacterias. Los exámenes detectan caries antes de que lleguen a la pulpa. Las radiografías de aleta identifican caries interproximales invisibles a la inspección visual. El intervalo de recordatorio de 6 meses es adecuado para la mayoría de los pacientes, aunque aquellos con alto riesgo de caries o enfermedad periodontal activa pueden necesitar intervalos de 3-4 meses.
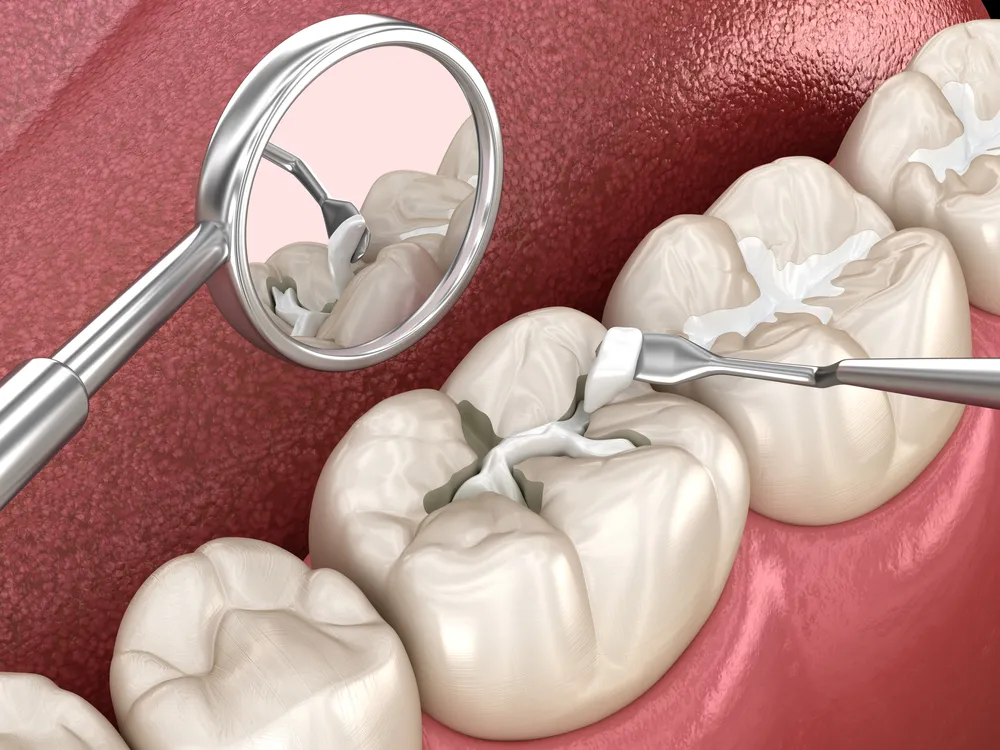
El tratamiento temprano de las caries previene la infección de la pulpa. Las caries pequeñas requieren empastes simples. La demora permite que la caries se profundice, lo que eventualmente requiere terapia de conducto radicular o extracción. Los sellantes dentales en los dientes posteriores protegen a los niños y adolescentes de la caries en las superficies oclusales.
El manejo de la enfermedad periodontal previene abscesos periodontales. El raspado y alisado radicular (limpieza profunda) elimina el cálculo de las superficies radiculares. El mantenimiento periodontal cada 3 meses controla la progresión de la enfermedad. La reducción quirúrgica de bolsas elimina espacios profundos donde se forman abscesos.
Las modificaciones dietéticas apoyan la prevención. Limitar la exposición al azúcar, particularmente el picoteo frecuente y las bebidas azucaradas, reduce la producción de ácido de Streptococcus mutans. Masticar chicle sin azúcar estimula el flujo de saliva, que neutraliza el ácido y remineraliza el esmalte. El agua fluorada fortalece la estructura dental contra el ataque ácido.
¿Cuál es la recuperación esperada después del tratamiento de infecciones dentales?
El dolor mejora dentro de 24-48 horas después del control de la fuente. Los tejidos blandos sanan en 1-2 semanas. La curación ósea toma de 3 a 6 meses. La intervención temprana produce una recuperación más rápida y completa.
Los plazos de curación esperados varían según el procedimiento y la gravedad de la infección. El drenaje de un absceso agudo produce un alivio inmediato del dolor. La hinchazón disminuye en 2-3 días. La pequeña incisión sana en una semana. Sin embargo, el diente subyacente aún requiere tratamiento definitivo para prevenir la recurrencia.
La recuperación de la terapia de conducto radicular sigue un patrón predecible. El dolor postoperatorio dura de 2 a 3 días, manejable con AINEs. El hueso periapical comienza a sanar en semanas, aunque el llenado óseo radiográfico completo requiere de 6 a 12 meses. La colocación de la corona final, de 2 a 4 semanas después de completar el conducto radicular, restaura la función y previene fracturas.
Los sitios de extracción sanan en etapas. La formación de coágulos de sangre ocurre inmediatamente. El tejido blando se cierra en 1-2 semanas. El hueso llena el alvéolo en 3-6 meses. La colocación del implante, cuando está planificada, generalmente ocurre de 3 a 4 meses después de la extracción para permitir la sanación ósea inicial.
La intervención temprana mejora drásticamente los resultados. Un absceso periapical tratado dentro de los días posteriores al inicio de los síntomas responde a una terapia de conducto radicular simple. La demora de semanas permite que la destrucción ósea se expanda, complicando el tratamiento y reduciendo la probabilidad de supervivencia del diente. Los abscesos periodontales tratados de manera oportuna preservan los dientes; el tratamiento retrasado a menudo resulta en un pronóstico desesperanzador que requiere extracción.
Los factores que afectan los resultados incluyen la adherencia del paciente, el estado inmunológico y el seguimiento con el cuidado definitivo. Los pacientes que completan los cursos de antibióticos prescritos y regresan para los procedimientos definitivos programados experimentan mejores resultados. Fumar perjudica la sanación al reducir el flujo sanguíneo y la función inmunológica. La diabetes requiere control glucémico para una recuperación óptima.
¿Qué avances están moldeando el tratamiento futuro de las infecciones dentales?
Nuevos péptidos antimicrobianos atacan los biofilms sin resistencia. La desinfección asistida por láser mejora la esterilización del conducto radicular. La medicina personalizada utiliza pruebas genéticas para predecir el riesgo de infección y la respuesta al tratamiento.
Los avances en la terapia antimicrobiana abordan la resistencia de los biofilms. Los antibióticos tradicionales fallan contra las bacterias protegidas por biofilms. Los investigadores desarrollan péptidos antimicrobianos, fragmentos de proteínas cortas que interrumpen las membranas bacterianas sin desarrollo de resistencia. Estos péptidos, derivados de moléculas inmunitarias naturales, muestran promesa como irrigantes de conducto radicular y tratamientos tópicos.
La terapia fotodinámica utiliza colorantes activados por luz para matar bacterias. El dentista aplica un agente fotosensibilizante en el área infectada y luego la expone a longitudes de onda de luz específicas. Las especies reactivas de oxígeno destruyen las membranas y el ADN bacteriano. Esta técnica esteriliza los sistemas de conducto radicular y los bolsillos periodontales sin antibióticos.
Las técnicas mínimamente invasivas preservan la estructura dental. La tecnología GentleWave utiliza energía multisonica y dinámica de fluidos avanzada para desinfectar la anatomía compleja del conducto radicular con mínima instrumentación. El tratamiento de conducto radicular asistido por láser vaporiza el tejido infectado y esteriliza las paredes del canal simultáneamente.
El cuidado dental personalizado aprovecha el análisis genético y del microbioma. Las pruebas genéticas identifican a los pacientes con deficiencias inmunitarias innatas que predisponen a infecciones severas. El perfilado del microbioma oral predice el riesgo de enfermedad periodontal y guía la terapia probiótica dirigida. La farmacogenómica determina la selección óptima de antibióticos según el metabolismo individual.
La endodoncia regenerativa representa un cambio de paradigma. En lugar de eliminar la pulpa y llenar los conductos con material inerte, este enfoque fomenta la regeneración del tejido pulpar utilizando células madre y factores de crecimiento. Los dientes inmaduros con pulpas infectadas pueden continuar el desarrollo radicular, produciendo dientes más fuertes y duraderos. La investigación de Galler (2021) en el Journal of Endodontics demuestra la maduración continua de la raíz en el 80% de los dientes permanentes inmaduros tratados.
Preguntas Frecuentes Sobre el Tratamiento de Infecciones Dentales
¿Todas las Infecciones Dentales Requieren Antibióticos?
No. Los abscesos dentales localizados sin fiebre o hinchazón facial solo necesitan control de la fuente, drenaje, tratamiento de conducto o extracción. Los antibióticos solo ayudan cuando la infección se propaga sistémicamente.
La idea errónea de que cada infección dental necesita antibióticos impulsa la sobreprescripción. Las guías clínicas de la Asociación Dental Americana y el Instituto Nacional de Salud y Atención de Gran Bretaña afirman explícitamente que los antibióticos son innecesarios para la mayoría de las infecciones dentales localizadas. Los procedimientos de control de la fuente eliminan la infección directamente. Agregar antibióticos no proporciona ningún beneficio y contribuye a la resistencia.
Los antibióticos se vuelven necesarios cuando los pacientes muestran involucramiento sistémico. Fiebre, malestar, linfadenopatía o celulitis en expansión indican una carga bacteriana que excede el control local. Los pacientes inmunocomprometidos pueden necesitar iniciar antibióticos antes. Cuando los dentistas no pueden realizar un control de la fuente inmediato debido a problemas de acceso del paciente, los antibióticos sirven como puentes temporales hacia la atención definitiva.
¿Cuánto Tiempo Toma el Tratamiento de Infecciones Dentales?
El drenaje de un absceso agudo proporciona alivio inmediato. La terapia de conducto radicular requiere de 1 a 3 citas en un período de 1 a 2 semanas. La extracción sana en 1-2 semanas. Los cursos de antibióticos duran de 5 a 7 días.
La duración del tratamiento depende de la gravedad de la infección y del enfoque elegido. El drenaje simple de un absceso toma 30 minutos en la consulta dental. El dolor mejora en unas pocas horas. Sin embargo, el paciente debe regresar para el tratamiento definitivo del diente dentro de unos días para prevenir la recurrencia.
La terapia de conducto radicular generalmente abarca dos citas. La primera visita elimina la pulpa infectada y coloca medicación antibacteriana. La segunda visita, 1-2 semanas después, llena y sella los conductos. Una tercera cita coloca la corona permanente 2-4 semanas después. Tiempo total de tratamiento: 4-8 semanas para una restauración completa.
La extracción proporciona la solución definitiva más rápida. El procedimiento toma de 20 a 40 minutos. El tejido blando sana en 1-2 semanas. Si se planea un reemplazo por implante, el cronograma se extiende de 3 a 6 meses para la cicatrización ósea antes de la colocación del implante.
Los cursos de antibióticos permanecen cortos. De cinco a siete días son suficientes para infecciones dentales, a diferencia de los cursos prolongados necesarios para infecciones de tejido profundo o óseo. Los pacientes deben completar el curso completo incluso si los síntomas mejoran antes para prevenir la recurrencia y la resistencia.
¿Pueden las infecciones dentales sanar por sí solas?
No. Las infecciones dentales requieren intervención profesional. El cuerpo no puede eliminar las fuentes de infección dentro de los dientes o cavidades de abscesos. El tratamiento tardío aumenta el riesgo de complicaciones.
Ocasionalmente, un absceso se rompe espontáneamente, drenando pus y aliviando temporalmente la presión. Los pacientes pueden interpretar esto como "sanación". Sin embargo, la fuente de infección, la pulpa necrótica, la caries profunda o el bolsillo periodontal, permanece. Las bacterias se repoblan. El absceso recurre, a menudo con organismos más resistentes.
El entorno cerrado de la raíz de un diente o la cavidad del absceso impide el acceso inmunológico. Los neutrófilos y los anticuerpos no pueden penetrar eficazmente en el tejido necrótico o en el pus espeso. Los antibióticos que circulan en la sangre no pueden alcanzar las bacterias en estos espacios avasculares. Solo la eliminación mecánica, el drenaje, el tratamiento de conducto o la extracción eliminan la infección.
Rara vez, las infecciones crónicas de bajo grado persisten durante meses sin síntomas agudos. Estas infecciones "silenciosas" aún destruyen hueso y liberan mediadores inflamatorios en el torrente sanguíneo. Contribuyen a problemas de salud sistémicos sin causar dolor notable. Las radiografías dentales regulares detectan estas infecciones ocultas.
¿Cuándo debe alguien buscar atención de emergencia por una infección dental?
Busque atención de emergencia si tiene dificultad para respirar o tragar, hinchazón facial que se expande rápidamente, fiebre superior a 39°C (102°F), confusión o afectación ocular por infecciones de dientes superiores.
Las señales de advertencia de emergencia indican una progresión que amenaza la vida. El compromiso de la vía aérea por hinchazón submandibular o del suelo de la boca requiere evaluación inmediata en el departamento de emergencias. Los pacientes que no pueden tragar su propia saliva, que desarrollan respiración ruidosa (estridor) o que sienten que su garganta se cierra necesitan manejo de la vía aérea de emergencia.
La celulitis que se expande rápidamente, la hinchazón que se expande visiblemente en horas, sugiere una cepa bacteriana agresiva o inmunidad comprometida. Se vuelven necesarios antibióticos intravenosos y posible drenaje quirúrgico. La hinchazón facial que cruza la línea media o que involucra ambos lados indica propagación bilateral.
La toxicidad sistémica señala sepsis. Fiebre alta, frecuencia cardíaca rápida (más de 100 latidos por minuto), respiración rápida (más de 20 respiraciones por minuto) y estado mental alterado exigen atención de emergencia. Estos pacientes necesitan cultivos de sangre, líquidos intravenosos y antibióticos de amplio espectro en un entorno de cuidados intensivos.
La afectación ocular por infecciones de dientes superiores amenaza la visión. La hinchazón alrededor del ojo, la visión doble o la incapacidad para mover el ojo indican celulitis orbital. Esta complicación, que surge de infecciones de dientes maxilares que se propagan a través de hueso delgado hacia la órbita, requiere consulta de emergencia con oftalmología y otorrinolaringología.
Síntoma | Acción Requerida | Plazo |
Dolor de muelas con leve hinchazón | Cita dental | Dentro de 24-48 horas |
Hinchazón facial, fiebre | Atención dental o médica urgente | Mismo día |
Dificultad para respirar/tragar | Departamento de emergencias | Inmediatamente |
Hinchazón en el ojo, cambios en la visión | Departamento de emergencias | Inmediatamente |
Confusión, fiebre alta, ritmo cardíaco rápido | Departamento de emergencias/911 | Inmediatamente |
Conclusión: Por qué la acción temprana salva dientes y vidas
Las infecciones dentales exigen un control de fuente inmediato a través de drenaje, tratamiento de conducto o extracción. Los antibióticos juegan un papel de apoyo para la propagación sistémica. La prevención a través de cuidados regulares evita el dolor, el costo y el peligro de infecciones avanzadas.
El tratamiento de infecciones dentales se basa en principios claros. Eliminar la fuente de la infección. Drenar pus y tejido necrótico. Preservar los dientes naturales cuando sea posible. Extraer cuando sea necesario. Usar antibióticos de manera juiciosa, solo para involucramiento sistémico o cuando los procedimientos deben ser retrasados.
La evidencia apoya abrumadoramente este enfoque. Los antibióticos por sí solos fallan porque no pueden alcanzar las bacterias en las cámaras pulpares necróticas y en las cavidades de abscesos. Los organismos protegidos por biofilm resisten la penetración de medicamentos. Solo la eliminación mecánica del tejido infectado produce curación.
El diagnóstico temprano previene complicaciones. Una pequeña lesión periapical en la radiografía advierte sobre un absceso inminente. Un bolsillo periodontal profundo señala riesgo de absceso. Tratar estas condiciones antes de que se desarrollen síntomas agudos ahorra dientes, dinero y salud.
El uso equilibrado de antibióticos protege a los pacientes individuales y la salud pública. Cada receta innecesaria contribuye a la resistencia. Los dentistas que siguen las pautas de gestión, prescribiendo solo para casos indicados, eligiendo medicamentos de primera línea de espectro estrecho y limitando la duración, preservan la efectividad de los antibióticos para las generaciones futuras.
La integración del tratamiento clínico y la prevención ofrece los mejores resultados. Los pacientes que combinan visitas dentales regulares con cuidado diario en casa rara vez desarrollan infecciones. Cuando ocurren infecciones, buscan atención de inmediato en lugar de soportar el dolor o esperar una resolución espontánea.
El futuro del tratamiento de infecciones dentales parece prometedor. Las terapias dirigidas al biofilm, las técnicas regenerativas y los enfoques de medicina personalizada mejorarán los resultados mientras reducen la dependencia de antibióticos. Sin embargo, el principio fundamental permanece sin cambios: identificar la fuente, eliminar la infección y restaurar la salud.
Referencias
Cope, Anwen L., et al. "Uso de antibióticos en la práctica dental: una revisión sistemática." British Dental Journal, vol. 216, no. 9, 2014, pp. 523-30.
Galler, Kerstin M., et al. "Procedimientos endodónticos regenerativos para el tratamiento de la necrosis pulpar en dientes permanentes inmaduros: una revisión sistemática." Journal of Endodontics, vol. 47, no. 8, 2021, pp. 1193-202.
Lockhart, Peter B., et al. "Mala salud oral como una condición crónica, potencialmente infecciosa e inflamatoria." Journal of Dental Research, vol. 98, no. 10, 2019, pp. 1073-80.
Matthews, David C., et al. "Antibióticos para abscesos dentales agudos: una revisión sistemática." Journal of Antimicrobial Chemotherapy, vol. 71, no. 3, 2016, pp. 564-71.
Moore, R. Andrew, et al. "Medicamentos antiinflamatorios no esteroides para el dolor dental agudo." Cochrane Database of Systematic Reviews, no. 12, 2015, CD004978.
Ng, Yuan-Ling, et al. "Resultado del tratamiento de conducto radicular primario: revisión sistemática de la literatura." International Endodontic Journal, vol. 44, no. 7, 2011, pp. 597-612.
Patel, Shanon, et al. "Tomografía Computarizada de Haz Cónico en Endodoncia." Revista Internacional de Endodoncia, vol. 52, no. 9, 2019, pp. 1248-64.
Petersen, Poul Erik. "Política Global de la Organización Mundial de la Salud para la Mejora de la Salud Oral." Revista Internacional de Odontología, vol. 72, no. 4, 2022, pp. 302-07.
Seneviratne, Chaminda J., et al. "Biofilm de Placa Dental: Un Biofilm Arquetípico." Periodontología 2000, vol. 75, no. 1, 2017, pp. 34-44.