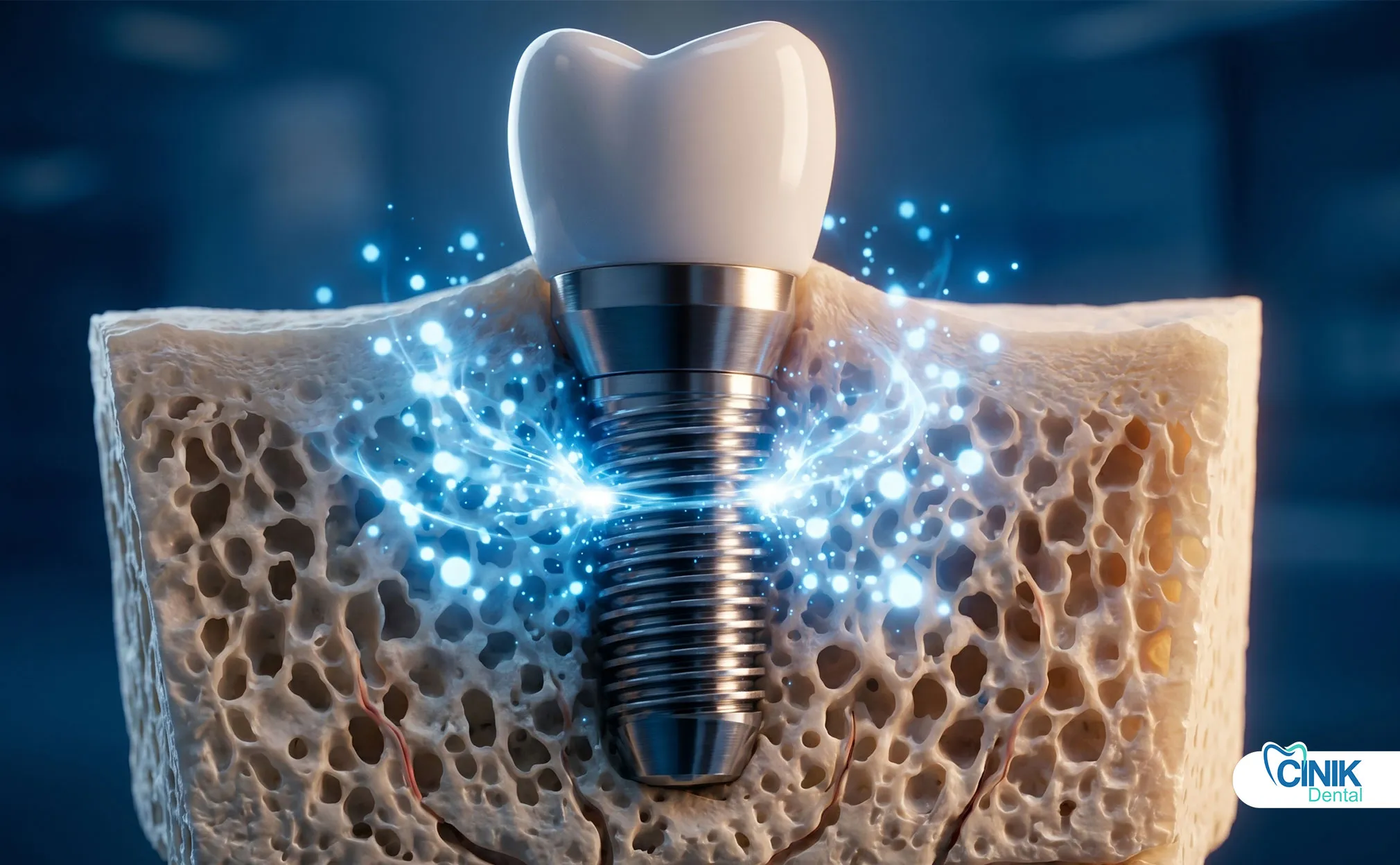
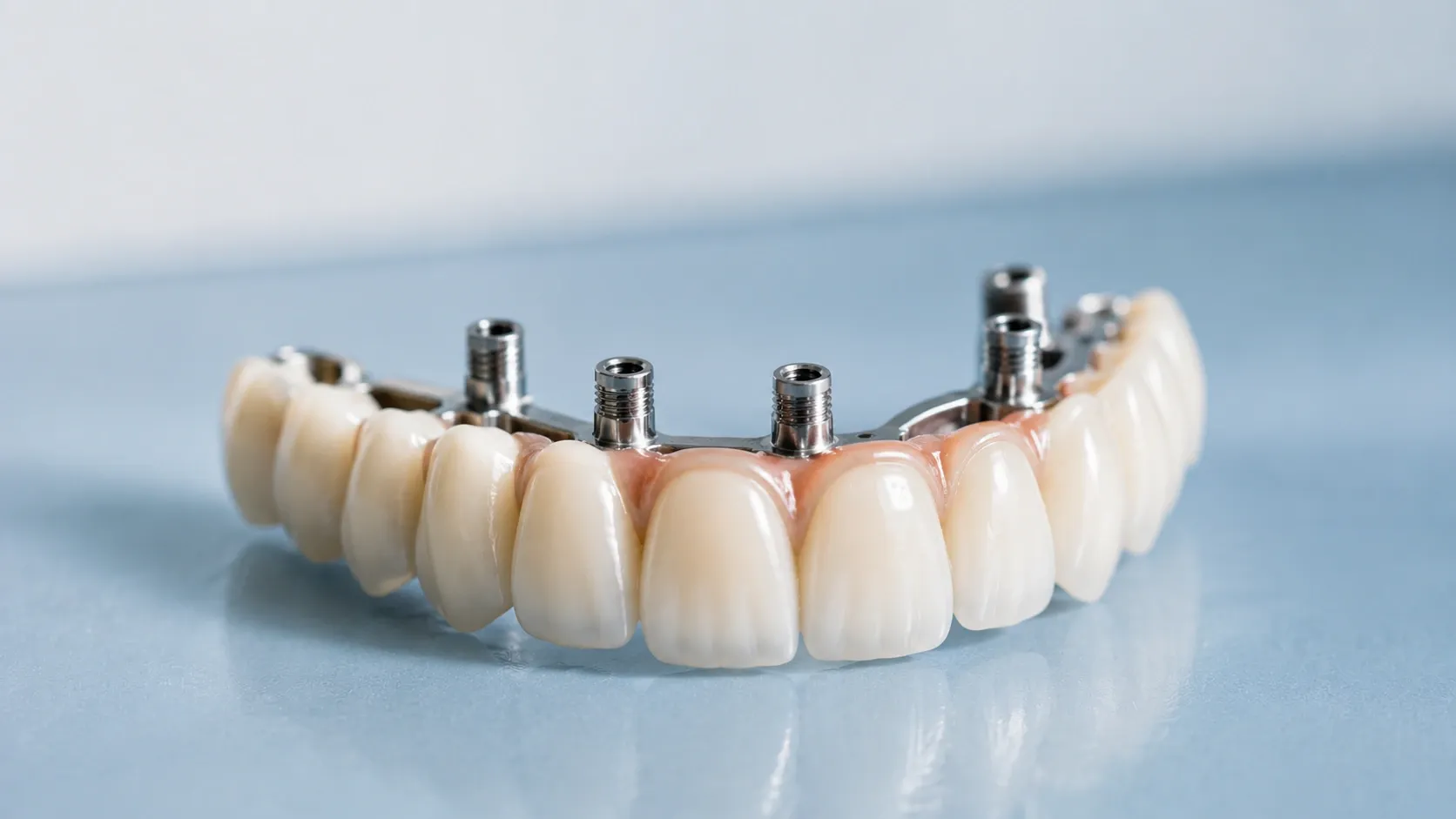
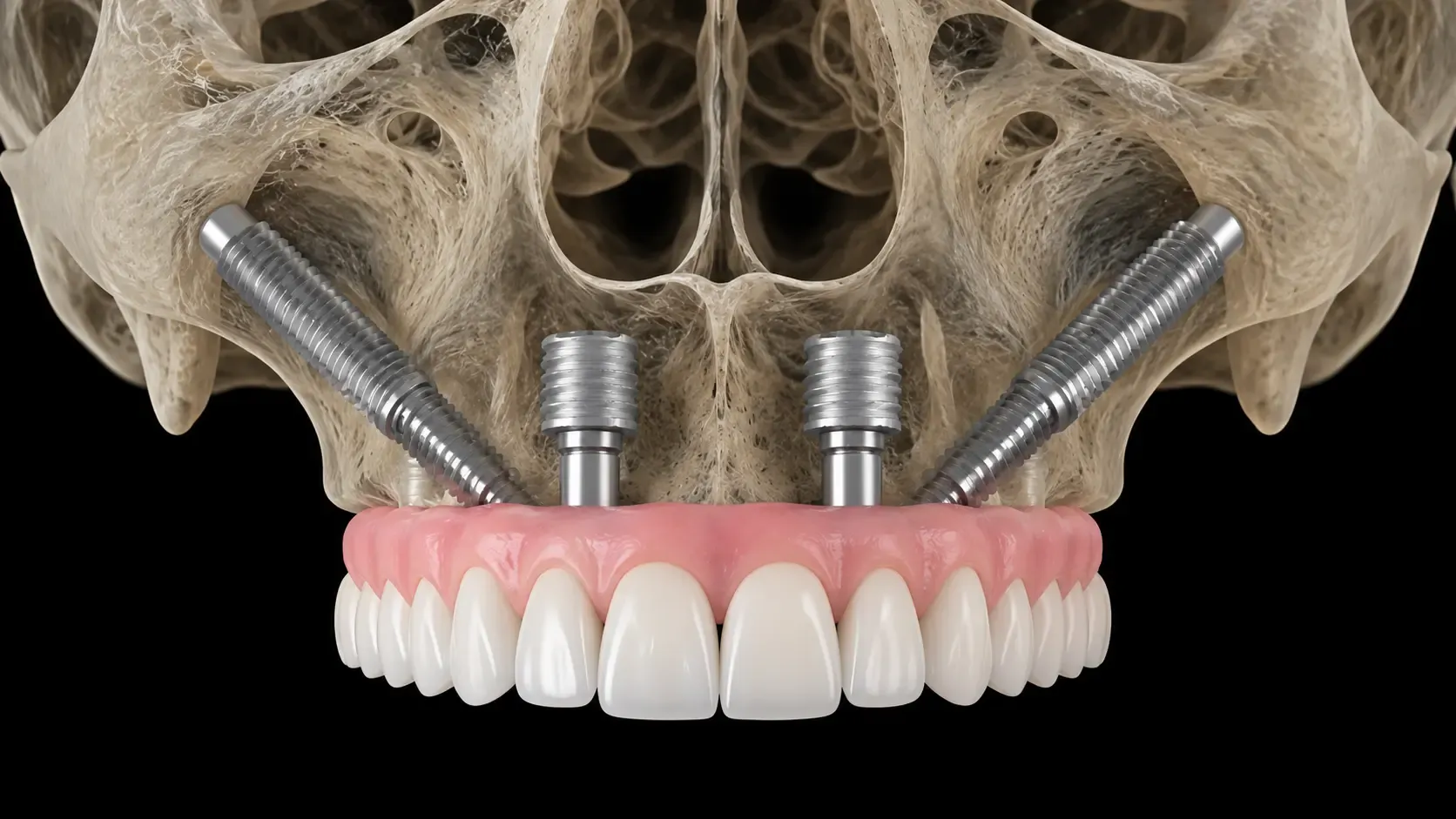
Qu'est-ce que la thérapie par exosomes et pourquoi est-elle importante pour les implants dentaires ?
La thérapie par exosomes représente une avancée dans la dentisterie régénérative. Ce traitement sans cellules utilise de minuscules vésicules pour accélérer la guérison osseuse, réduire l'inflammation et améliorer les taux de réussite des implants. Contrairement aux approches traditionnelles par cellules souches, la thérapie par exosomes délivre des facteurs de croissance sans cellules vivantes, éliminant les risques de rejet ou de formation de tumeurs.
Les implants dentaires servent de référence pour le remplacement des dents. Cependant, les cliniciens font face à des défis persistants. Certains patients connaissent une guérison retardée. D'autres souffrent d'inflammation péri-implantaire ou d'une densité osseuse insuffisante. Ces complications compromettent la stabilité et la longévité des implants.
La dentisterie régénérative se tourne maintenant vers les exosomes comme solution. Ces particules à l'échelle nanométrique agissent comme des messagers biologiques. Elles transportent des protéines, de l'ARN et des lipides qui stimulent les processus de réparation naturelle. La recherche montre qu'elles améliorent l'ostéointégration, la fusion critique entre l'implant et l'os (Valadi et al., 2007). Cet article examine comment la thérapie par exosomes transforme la dentisterie implantaire à travers des mécanismes scientifiques, des applications cliniques et un potentiel futur.
Que sont les exosomes et comment fonctionnent-ils dans la réparation des tissus ?
Les exosomes sont des vésicules extracellulaires mesurant de 30 à 150 nanomètres de diamètre. Les cellules libèrent ces bulles pour communiquer avec les tissus voisins. Ils proviennent de la voie endosomale par un processus appelé fusion du corps multivésiculaire. Pensez à eux comme des messages texte biologiques. Une cellule envoie des instructions. Une autre cellule reçoit le signal et modifie son comportement.
Tableau 1 : Composants principaux des exosomes et leurs fonctions
Composant | Fonction | Impact thérapeutique |
Protéines | Signalisation cellulaire | Activer les voies de réparation |
miARN | Régulation des gènes | Contrôler l'inflammation et la croissance osseuse |
ARNm | Synthèse des protéines | Diriger la régénération des tissus |
Lipides | Structure membranaire | Assurer la stabilité et la fusion cellulaire |
La composition varie selon la cellule source. Les exosomes dérivés de cellules souches mésenchymateuses (exosomes-CSM) transportent plus de 850 protéines, y compris le facteur de croissance transformant-β et le facteur de croissance insulinique (Zhang et al., 2020). Les cellules souches de la pulpe dentaire libèrent des exosomes enrichis en miARN ostéogéniques. Ce chargement spécialisé explique pourquoi les exosomes de différentes sources produisent des effets de guérison distincts.
Les exosomes résolvent les principaux problèmes associés à la thérapie par cellules souches. Les cellules souches peuvent déclencher des réactions immunitaires. Elles peuvent former des tumeurs. Elles nécessitent des conditions de stockage strictes. Les exosomes contournent entièrement ces problèmes. Ils offrent une faible immunogénicité, une haute biocompatibilité et des préoccupations de sécurité réduites (Shi et al., 2021). Les patients reçoivent les bénéfices régénératifs sans les risques cellulaires.
Comment les exosomes favorisent-ils la formation osseuse autour des implants dentaires ?
Quels mécanismes stimulent l'amélioration de l'ostéogenèse ?
Les exosomes activent plusieurs voies pour construire l'os. Ils stimulent la différenciation des ostéoblastes. Ils augmentent le dépôt de matrice osseuse. Ils renforcent la minéralisation sur l'ensemble du site de guérison.
La recherche de Furuta et al. (2016) démontre que les exosomes MSC favorisent la guérison des fractures dans les modèles murins. Les exosomes augmentent l'activité de la phosphatase alcaline (ALP). Cette enzyme sert de marqueur précoce de la formation osseuse. Les niveaux d'ostéocalcine (OCN) augmentent également. Cette protéine indique le développement d'une matrice osseuse mature.
Trois voies de signalisation principales conduisent ces effets :
Voie BMP/Smad : Les exosomes délivrent des protéines morphogénétiques osseuses. Ces protéines se lient aux récepteurs de surface cellulaire. Elles activent les facteurs de transcription Smad. L'expression de Runx2 et Osterix augmente. La formation osseuse s'accélère.
Voie Wnt/β-caténine : Les exosomes stabilisent la β-caténine dans les cellules réceptrices. Cette molécule entre dans le noyau. Elle active les gènes responsables de la prolifération et de la différenciation cellulaires. Zhang et al. (2020) ont découvert que les exosomes MSC de cordon ombilical humain réduisent la perte osseuse par ce mécanisme.
Voie PI3K/AKT : Les exosomes déclenchent des signaux de survie dans les cellules cibles. Cela empêche l'apoptose pendant la phase critique de guérison précoce. Des études montrent que l'inhibition de cette voie bloque la formation osseuse induite par les exosomes (Chen et al., 2019).
Comment les exosomes améliorent-ils l'apport sanguin aux sites d'implantation ?
L'angiogenèse s'avère essentielle pour une ostéointégration réussie. Le tissu osseux a besoin d'oxygène et de nutriments. Sans vascularisation adéquate, les implants échouent.
Les exosomes stimulent la production du facteur de croissance endothélial vasculaire (VEGF). Ils encouragent les cellules endothéliales à former des structures tubulaires. Qi et al. (2016) ont observé que les exosomes hiPS-MSC combinés avec des échafaudages β-TCP ont amélioré à la fois la régénération osseuse et l'angiogenèse dans les modèles de rat. Les vaisseaux ont pénétré plus profondément dans le matériau de greffe osseuse. Cette double action, construction osseuse plus création de vaisseaux, crée un environnement favorable à l'intégration de l'implant.
Quel rôle jouent les exosomes dans le contrôle de l'inflammation ?
L'inflammation détruit les implants. La péri-implantite affecte jusqu'à 20 % des patients avec des implants dentaires. Les antibiotiques traditionnels aident mais créent des problèmes de résistance. Les exosomes offrent une solution biologique.
Les exosomes dérivés de cellules souches de pulpe dentaire (DPSC-EXO) suppriment les cytokines pro-inflammatoires. Ils inhibent la production d'IL-1β et de TNF-α. Ils bloquent la voie de signalisation IL-6/JAK2/STAT3 (Li et al., 2023). Cette voie conduit à une inflammation destructive dans les tissus parodontaux.
Les macrophages changent de comportement après exposition aux exosomes. Les macrophages M1 pro-inflammatoires se transforment en macrophages M2 anti-inflammatoires. Ce changement de polarisation réduit les dommages tissulaires. Il crée un environnement pro-guérison autour de l'implant (Shen et al., 2020).
Où les cliniciens peuvent-ils appliquer la thérapie par exosomes en implantologie dentaire ?
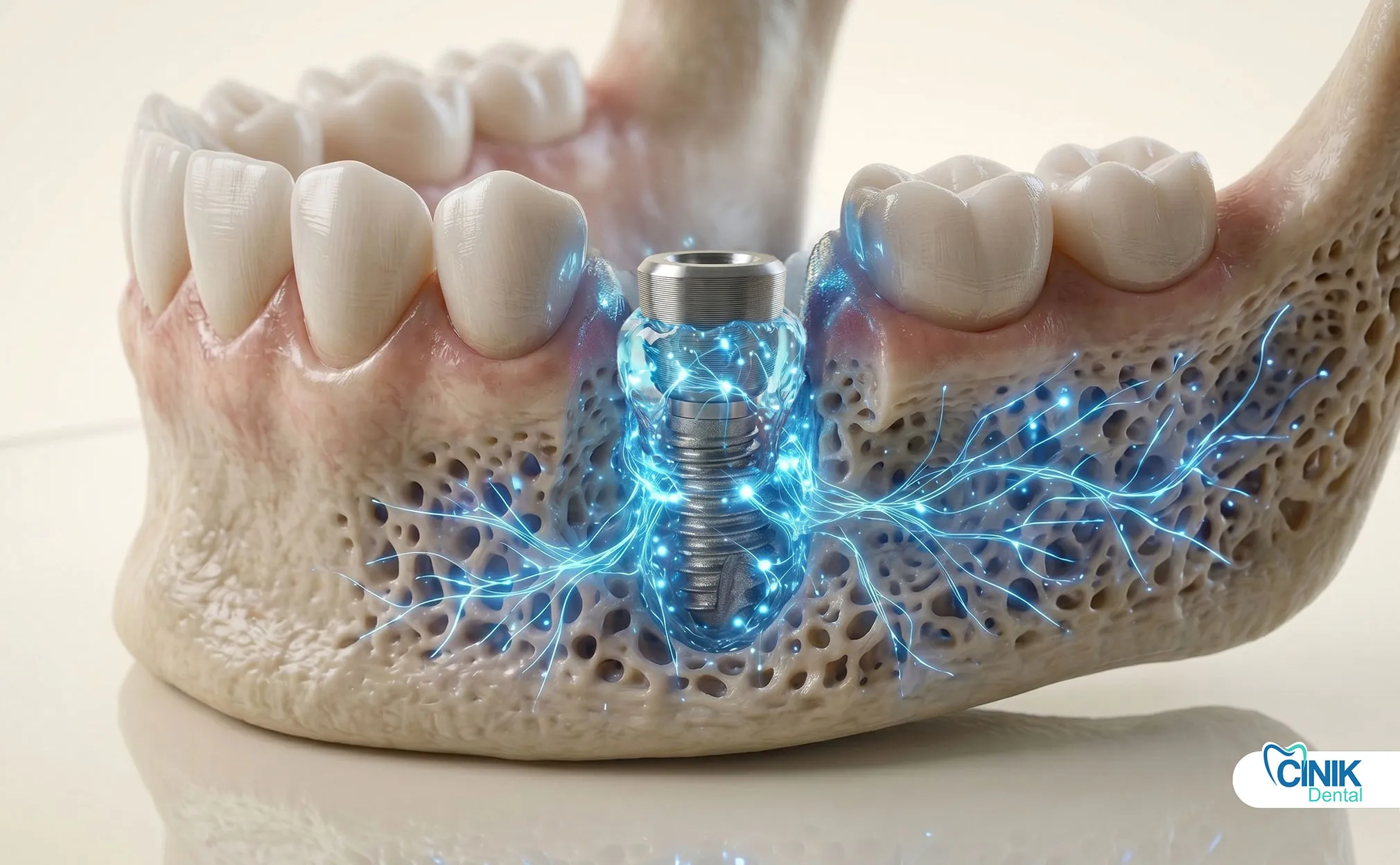
Les exosomes peuvent-ils accélérer l'ostéointégration dans les cas d'implants standard ?
Oui. Les exosomes améliorent significativement le contact os-implant. Ils accélèrent les délais d'intégration. L'ostéointégration traditionnelle nécessite de trois à six mois. La thérapie par exosomes peut réduire cette période de 30 à 40 % selon les données précliniques.
Wang et al. (2020) ont développé un hydrogel auto-cicatrisant contenant des exosomes de CSM de cordon ombilical. Le matériau a favorisé la régénération osseuse dans des défauts de taille critique. La fraction de volume osseux a augmenté par rapport aux groupes témoins. Cela suggère une intégration de l'implant plus rapide et plus robuste en présence d'exosomes.
Les exosomes aident-ils les patients avec une insuffisance osseuse ?
Absolument. La régénération de l'os alvéolaire représente une application majeure. De nombreux patients n'ont pas suffisamment d'os pour la pose immédiate d'implants. Les exosomes améliorent les procédures de greffe osseuse. Ils améliorent les résultats de l'augmentation de la crête. Ils préviennent la résorption osseuse après extraction.
Tableau 2 : Sources d'exosomes et leurs propriétés régénératrices
Source | Potentiel ostéogénique | Force immunomodulatrice | Accessibilité |
CSM de moelle osseuse | Élevé | Modéré | Invasif |
Cellules souches de pulpe dentaire | Très élevé | Très élevé | Minimement invasif |
Ligament parodontal | Élevé | Élevé | Modéré |
MSCs gingivaux | Modéré | Très élevé | Facile |
Les cellules souches dentaires fournissent des exosomes supérieurs pour les applications orales. Elles expriment des marqueurs spécifiques comme CD24 et CD140a. Ces cellules prolifèrent plus rapidement que les alternatives de moelle osseuse. Elles résistent à la sénescence lors de l'expansion en culture. Plus important encore, elles s'adaptent naturellement à l'environnement oral (Kotova et al., 2021).
Les exosomes peuvent-ils guérir les tissus mous autour des implants ?
Les joints de tissus mous empêchent l'invasion bactérienne. Ils protègent l'os sous-jacent. Les exosomes accélèrent la cicatrisation des plaies gingivales. Ils stimulent la migration des fibroblastes et la production de collagène.
Zhou et al. (2022) ont démontré que les échafaudages fonctionnalisés avec des exosomes amélioraient l'intégration des tissus mous. L'épithélium gingival guérissait plus complètement. Cela réduisait les complications post-chirurgicales. Cela améliorait les résultats esthétiques finaux pour les restaurations d'implants antérieurs.
Les exosomes sont-ils efficaces contre les maladies péri-implantaires ?
La recherche soutient fortement cette application. La péri-implantite implique une infection bactérienne et une perte osseuse inflammatoire. Les exosomes offrent une double protection. Ils modulent les réponses immunitaires. Ils transportent également des peptides antimicrobiens.
Lei et al. (2022) ont montré que les exosomes dérivés de cellules souches traitaient la perte osseuse inflammatoire dans les modèles de parodontite. La fraction volumique osseuse s'est améliorée de manière significative. Les ostéoclastes positifs à la phosphatase acide résistante au tartrate (TRAP) ont diminué. Cela indique une réduction de la destruction osseuse.
Quelles sources fournissent les meilleurs exosomes pour les applications dentaires ?
Les cellules souches mésenchymateuses restent la source principale. Cependant, les tissus dentaires offrent des avantages uniques.
Cellules souches de la pulpe dentaire (DPSCs) : Ces cellules résident à l'intérieur des structures dentaires. Elles démontrent des taux de prolifération élevés. Elles conservent un fort potentiel ostéogénique même après plusieurs passages. Les exosomes des DPSCs contiennent des miARN spécifiques qui favorisent l'angiogenèse et la neuroprotection.
Cellules souches du ligament parodontal (PDLSCs) : Ces cellules relient les dents à l'os. Elles régulent naturellement l'homéostasie parodontale. Leurs exosomes excellent dans la régénération des tissus mous et la formation de l'interface os-ligament.
Cellules souches des dents déciduales exfoliées humaines (SHEDs) : Ces cellules proviennent des dents de lait. Elles montrent une plasticité exceptionnelle. Elles expriment les marqueurs précoces des cellules souches plus longtemps que d'autres sources. Les exosomes des SHEDs peuvent offrir des propriétés neuro-régénératives supérieures.
Exosomes modifiés : Les scientifiques chargent maintenant les exosomes avec des cargaisons spécifiques. Ils ajoutent HIF-1α pour stimuler l'angiogenèse. Ils incorporent miR-375 pour améliorer l'ostéogenèse (Chen et al., 2019). Cette personnalisation permet une thérapie ciblée pour des complications spécifiques des implants.
Quels bénéfices cliniques les patients reçoivent-ils de la thérapie par exosomes ?
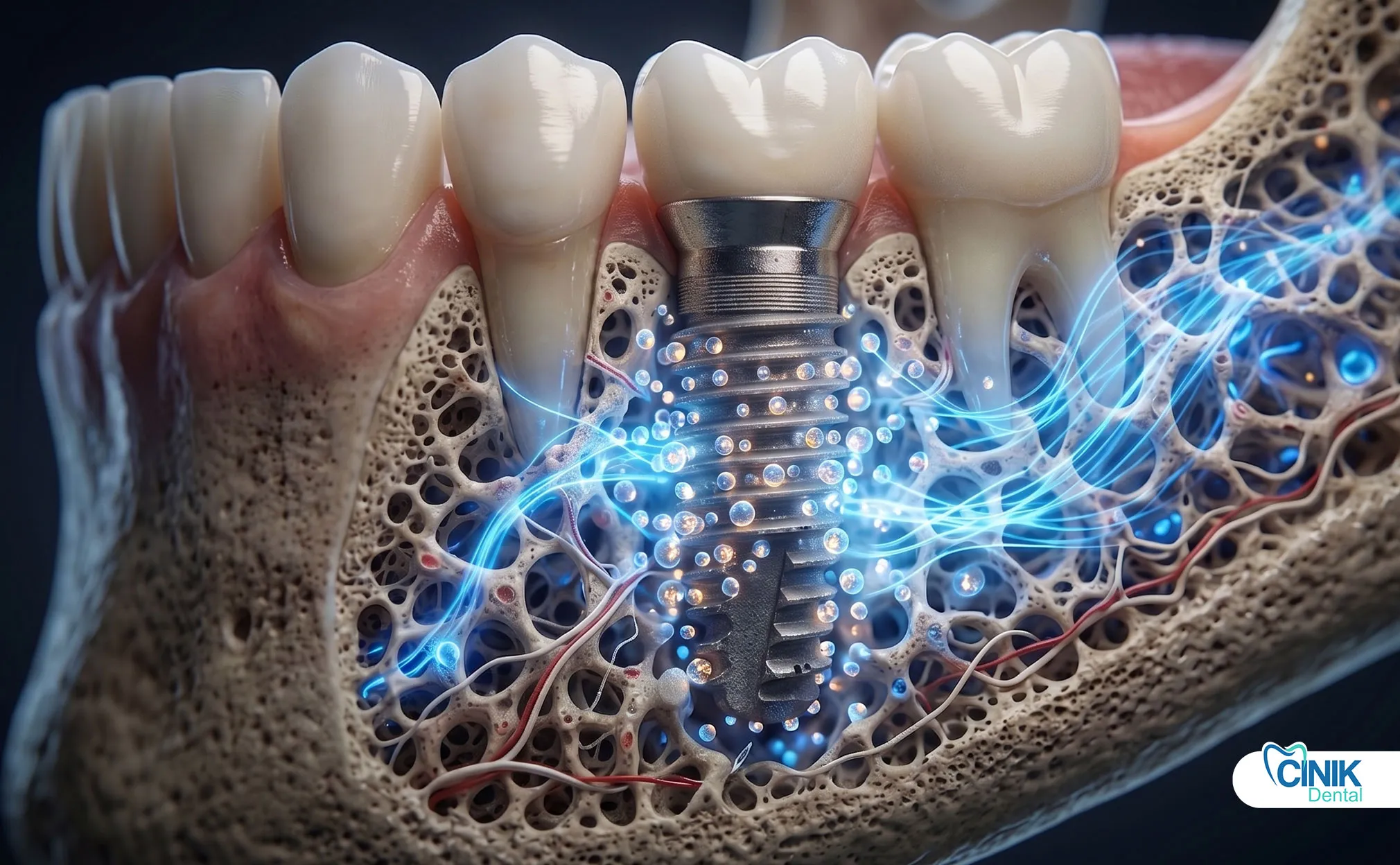
Les patients constatent des améliorations mesurables :
Guérison plus rapide : Les sites traités par exosomes montrent une minéralisation osseuse plus précoce. Les tissus mous se referment plus rapidement. Cela réduit le temps entre la pose de l'implant et la restauration finale.
Moins de douleur et de gonflement : L'action anti-inflammatoire réduit l'inconfort post-opératoire. Les patients rapportent des scores de douleur plus bas. Ils nécessitent moins de médicaments analgésiques.
Taux de réussite plus élevés : L'intégration précoce prévient la micromotion. Cela réduit l'échec de l'implant. Les exosomes peuvent s'avérer particulièrement précieux pour les patients atteints de diabète, d'ostéoporose ou ayant des antécédents de tabagisme, des groupes traditionnellement considérés à haut risque.
Administration minimalement invasive : Les cliniciens appliquent les exosomes par des hydrogels, des membranes de collagène ou une injection directe. Aucune chirurgie supplémentaire n'est requise. La thérapie s'intègre parfaitement dans les protocoles standard d'implantation.
Possibilités personnalisées : Les traitements futurs pourraient utiliser des exosomes spécifiques au patient. Les cellules prélevées sur les dents de sagesse extraites pourraient fournir des thérapies régénératives personnalisées.
Quelles limitations et défis existent actuellement ?
Pourquoi la thérapie par exosomes n'est-elle pas encore largement disponible ?
Lacunes dans les preuves : La plupart des études restent précliniques. Les chercheurs ont mené de nombreux essais sur les animaux. Les essais cliniques humains sont en retard. Les données à long terme sur les taux de survie des implants avec la thérapie par exosomes n'existent pas encore.
Problèmes de standardisation : Aucun protocole universel n'existe pour l'isolement des exosomes. L'ultracentrifugation différentielle reste populaire mais produit des rendements variables. Les méthodes de précipitation augmentent la quantité mais réduisent la pureté. Les technologies microfluidiques promettent de la cohérence mais nécessitent un équipement coûteux (Miron et al., 2025).
Obstacles réglementaires : Les agences réglementaires classent les exosomes comme des produits biologiques. Elles exigent des tests de sécurité approfondis. La production de masse doit respecter les normes de Bonnes Pratiques de Fabrication. Ces exigences ralentissent l'adoption clinique.
Barrières techniques : Les exosomes se dégradent pendant le stockage. Ils nécessitent des conditions de température spécifiques. Ils perdent de l'activité s'ils sont mal manipulés. Les systèmes de livraison doivent protéger les exosomes jusqu'à ce qu'ils atteignent les tissus cibles. Les échafaudages et hydrogels actuels offrent des solutions partielles. De meilleurs transporteurs sont nécessaires.
Comment les exosomes se comparent-ils à d'autres traitements régénératifs ?
Tableau 3 : Comparaison des thérapies régénératives
Caractéristique | Exosomes | Cellules souches | PRP | Matériaux de greffe osseuse |
Sans cellules | Oui | Non | Partiel | Oui |
Immunogénicité | Très faible | Modérée | Faible | Très faible |
Risque de tumeur | Aucun | Faible | Aucun | Aucun |
Concentration de facteur de croissance | Très élevée | Modérée | Modérée | Faible |
Complexité de manipulation | Modérée | Élevée | Faible | Faible |
Coût | Modéré | Élevé | Faible | Variable |
Les exosomes surpassent les cellules souches en termes de sécurité. Ils évitent le risque d'engagement. Ils éliminent les préoccupations concernant la différenciation cellulaire imprévisible in vivo. Ils fournissent trois fois la concentration de facteur de croissance des cellules souches adultes selon des analyses récentes.
Comparé au plasma riche en plaquettes (PRP), les exosomes offrent une plus grande cohérence. La qualité du PRP varie selon l'âge et l'état de santé du patient. Les exosomes issus de cellules souches cultivées maintiennent une puissance standardisée. Ils délivrent des effets thérapeutiques prévisibles.
Les matériaux de greffe osseuse fournissent un support structurel. Les exosomes fournissent des instructions biologiques. La combinaison s'avère supérieure. Les échafaudages en β-TCP chargés d'exosomes régénèrent l'os plus rapidement que les échafaudages seuls (Ying et al., 2020).
Quels développements futurs façonneront la thérapie par exosomes ?
Thérapies personnalisées par exosomes : Les cliniciens extrairont des cellules souches des tissus dentaires du patient. Ils cultiveront ces cellules et récolteront des exosomes. Cette approche autologue élimine tous les risques de rejet. Elle maximise la compatibilité thérapeutique.
Intégration de biomatériaux intelligents : Les implants imprimés en 3D incorporeront des réservoirs d'exosomes. Ces échafaudages libéreront des vésicules progressivement. Ils fourniront une stimulation soutenue tout au long de la période de guérison.
Exosomes chargés de gènes : Les scientifiques concevront des exosomes transportant des instructions génétiques spécifiques. Ils cibleront les voies de la péri-implantite. Ils accéléreront la régénération nerveuse sur les sites d'implantation.
Planification de traitement pilotée par l'IA : Les algorithmes d'apprentissage automatique prédiront les concentrations optimales d'exosomes. Ils détermineront le moment idéal de la délivrance. Ils personnaliseront les protocoles en fonction de la génétique du patient et de la qualité osseuse.
Comment les cliniciens devraient-ils mettre en œuvre la thérapie par exosomes ?
Sélection des patients : Les candidats idéaux incluent les patients avec une faible densité osseuse. Les fumeurs et les diabétiques en bénéficient particulièrement. Les patients nécessitant une pose immédiate d'implant sur les sites d'extraction montrent des résultats améliorés.
Contre-indications : Les patients avec des infections actives nécessitent un traitement préalable. Ceux avec des troubles de la coagulation nécessitent une évaluation attentive. Les patientes enceintes devraient attendre le postpartum en raison de données de sécurité limitées.
Protocoles d'intégration : Les cliniciens devraient incorporer des exosomes lors de la pose d'implant. Ils peuvent les appliquer sur le site de l'ostéotomie avant l'insertion de l'implant. Ils peuvent imbiber des membranes de collagène dans des solutions d'exosomes. Ils peuvent mélanger des exosomes avec des matériaux de greffe osseuse pour les procédures de sinus lift.
Considérations de coût : Actuellement, la thérapie par exosomes ajoute de 500 à 2 000 $ aux procédures d'implantation. Les prix diminueront à mesure que la production augmentera. La couverture d'assurance reste limitée. Les patients doivent comprendre qu'il s'agit d'un investissement personnel pour une guérison plus rapide.
Conclusion
La thérapie par exosomes pour les implants dentaires offre un outil régénératif puissant. Ces vésicules sans cellules accélèrent la formation osseuse. Elles réduisent l'inflammation. Elles améliorent la stabilité de l'implant. Elles évitent les risques associés aux thérapies cellulaires vivantes.
Les preuves actuelles soutiennent leur utilisation pour améliorer l'ostéo-intégration. Elles montrent un potentiel particulier pour la régénération osseuse dans les sites déficients. Elles offrent des solutions pour la gestion des maladies péri-implantaires. Elles s'intègrent harmonieusement avec les techniques d'implant avancées.
Cependant, les cliniciens doivent reconnaître les limitations. Des essais cliniques humains à long terme restent nécessaires. Les efforts de standardisation doivent se poursuivre. Les cadres réglementaires doivent être développés.
Le domaine progresse rapidement. Les exosomes DPSC démontrent un potentiel supérieur pour les applications orales. Les techniques d'ingénierie améliorent le ciblage et la puissance. Les systèmes de délivrance deviennent plus sophistiqués.
Pour les patients, cela signifie une guérison plus rapide. Cela signifie des complications réduites. Cela signifie une candidature plus large pour le traitement par implant. Pour la profession, cela représente un passage vers une intégration biologique plutôt que simplement mécanique des implants.
La thérapie par exosomes se situe à l'intersection de la biologie cellulaire et de la dentisterie clinique. Elle relie la découverte en laboratoire et les soins aux patients. Bien qu'elle ne soit pas encore courante, elle le sera bientôt. Les cliniciens qui comprennent ces mécanismes maintenant dirigeront la dentisterie implantaire de demain.
Références
Chen, Shiyi, et al. "Exosomes Derived from miR-375-Overexpressing Human Adipose Mesenchymal Stem Cells Promote Bone Regeneration." Cell Proliferation, vol. 52, no. 5, 2019, doi:10.1111/cpr.12669.
Fan, Linlin, et al. "Exosome-Functionalized Polyetheretherketone-Based Implant with Immunomodulatory Property for Enhancing Osseointegration." Bioactive Materials, vol. 6, no. 9, 2021, pp. 2754–66, doi:10.1016/j.bioactmat.2021.02.005.
Furuta, T., et al. "Mesenchymal Stem Cell-Derived Exosomes Promote Fracture Healing in a Mouse Model." Stem Cells Translational Medicine, vol. 5, no. 12, 2016, pp. 1620–30, doi:10.5966/sctm.2015-0285.
Kotova, A., et al. "Comparative Analysis of Dental Pulp and Periodontal Stem Cells: Differences in Morphology, Functionality, Osteogenic Differentiation and Proteome." Biomedicines, vol. 9, no. 11, 2021, p. 1606, doi:10.3390/biomedicines9111606.
Lei, Fengyang, et al. "Treatment of Inflammatory Bone Loss in Periodontitis by Stem Cell-Derived Exosomes." Acta Biomaterialia, vol. 141, 2022, pp. 333–43, doi:10.1016/j.actbio.2021.12.035.
Li, Mei, et al. "Dental Pulp Stem Cell-Derived Exosomes Regulate Anti-Inflammatory and Osteogenesis in Periodontal Ligament Stem Cells and Promote the Repair of Experimental Periodontitis in Rats." Frontiers in Bioengineering and Biotechnology, vol. 11, 2023, doi:10.3389/fbioe.2023.10441659.
Miron, Richard J., et al. "Méthodes d'isolement des exosomes dérivés des cellules souches dentaires." International Journal of Oral Science, 2025, doi:10.1038/s41368-025-00370-y.
Qi, X., et al. "Les exosomes sécrétés par des cellules souches mésenchymateuses dérivées de cellules souches pluripotentes humaines induites réparent des défauts osseux de taille critique grâce à une angiogenèse et une ostéogenèse améliorées chez les rats ostéoporotiques." International Journal of Biological Sciences, vol. 12, no. 7, 2016, pp. 836–49, doi:10.7150/ijbs.14809.
Shen, Zhenhua, et al. "L'hydrogel de chitosane incorporé avec des exosomes dérivés de cellules souches de pulpe dentaire atténue la parodontite chez les souris via un mécanisme dépendant des macrophages." Bioactive Materials, vol. 5, no. 4, 2020, pp. 1113–26, doi:10.1016/j.bioactmat.2020.07.002.
Shi, Qin, et al. "Exosomes dérivés de MSC : une nouvelle thérapie prometteuse pour l'ostéoporose." Frontiers in Cell and Developmental Biology, vol. 9, 2021, p. 723803, doi:10.3389/fcell.2021.723803.
Valadi, Hadi, et al. "Le transfert médié par les exosomes d'ARNm et de microARN est un nouveau mécanisme d'échange génétique entre les cellules." Nature Cell Biology, vol. 9, no. 6, 2007, pp. 654–59, doi:10.1038/ncb1596.
Wang, Ling, et al. "Un nouvel hydrogel auto-cicatrisant contenant des exosomes dérivés de hucMSC favorise la régénération osseuse." Frontiers in Bioengineering and Biotechnology, vol. 8, 2020, p. 564731, doi:10.3389/fbioe.2020.564731.
Ying, Chang, et al. "Les exosomes de BMSC transportent un HIF-1α mutant pour améliorer l'angiogenèse et l'ostéogenèse dans les défauts calvariaux de taille critique." Frontiers in Bioengineering and Biotechnology, vol. 8, 2020, p. 565561, doi:10.3389/fbioe.2020.565561.
Zhang, Shiqing, et al. "Les exosomes de MSC atténuent l'arthrose de l'articulation temporo-mandibulaire en réduisant l'inflammation et en restaurant l'homéostasie de la matrice." Biomaterials, vol. 200, 2019, pp. 35–47, doi:10.1016/j.biomaterials.2019.02.006.
Zhou, Ye, et al. "Les échafaudages osseux biomimétiques revêtus de polydopamine chargés d'exosomes favorisent la différenciation ostéogénique des BMSC et la régénération osseuse." Regenerative Therapy, vol. 23, 2023, pp. 25–36, doi:10.1016/j.reth.2023.03.005.