Die Behandlung von Zahninfektionen erfordert die Beseitigung der Infektionsquelle durch Drainage, Wurzelkanaltherapie oder Extraktion. Antibiotika dienen nur als unterstützende Therapie bei systemischer Beteiligung. Eine frühzeitige Intervention verhindert schwerwiegende Komplikationen wie Sepsis und Gewebsnekrose.
Was ist eine Zahninfektion und warum ist sie wichtig?
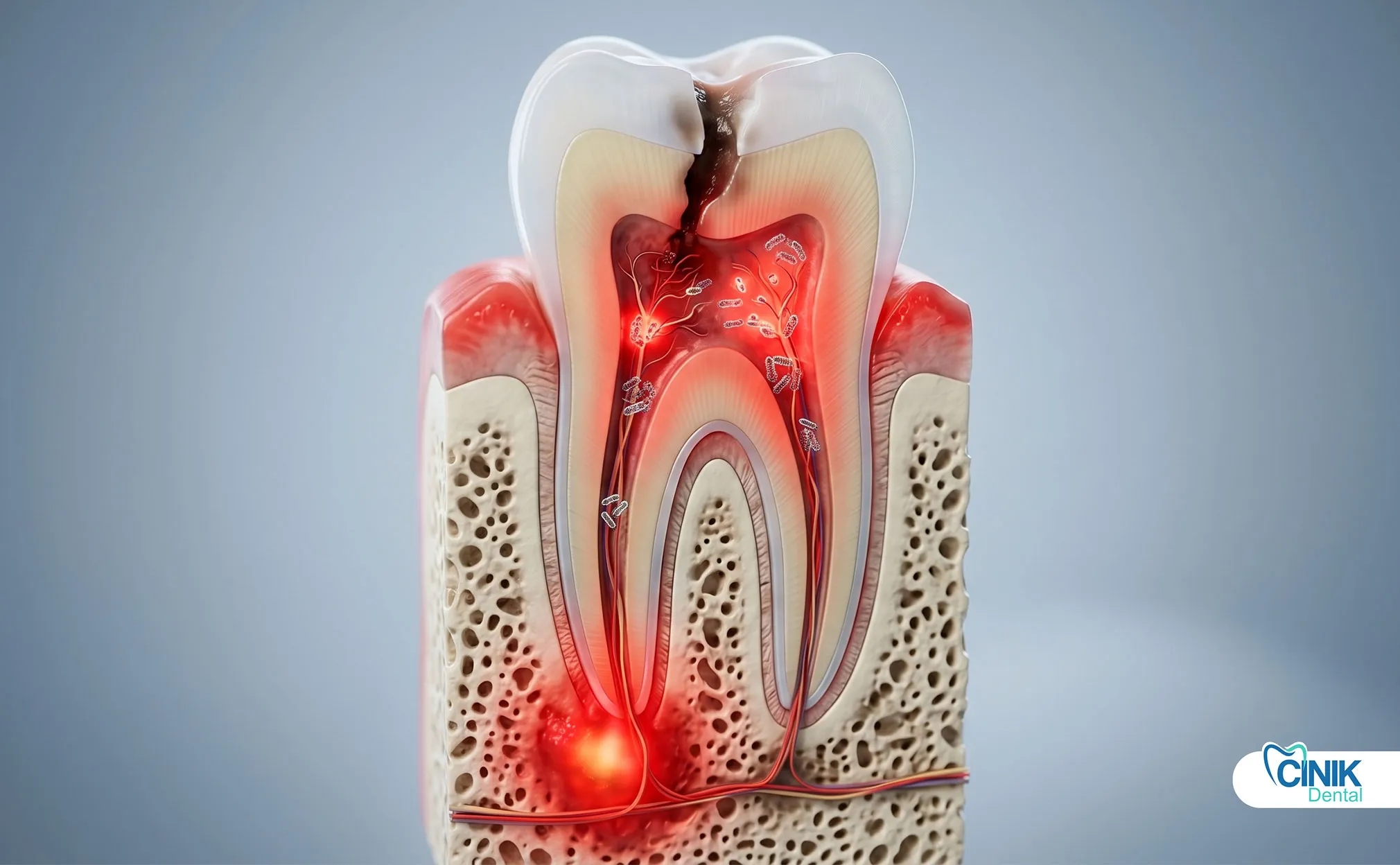
Eine Zahninfektion ist eine bakterielle Invasion der Zahnpulpa, des parodontalen Gewebes oder des umgebenden Knochens. Sie verursacht starke Schmerzen, Schwellungen und kann sich ohne sofortige Behandlung auf Gesichtsbereiche oder den Blutkreislauf ausbreiten.
Eine Zahninfektion, klinisch als odontogene Infektion bezeichnet, entwickelt sich, wenn Bakterien in die schützenden Schichten eines Zahns oder des umgebenden Zahnfleischgewebes eindringen. Diese Infektionen beginnen klein, können sich jedoch innerhalb von Tagen zu lebensbedrohlichen Zuständen entwickeln. Die Weltgesundheitsorganisation erkennt Zahninfektionen als eine bedeutende globale Gesundheitsbelastung an, insbesondere in Bevölkerungsgruppen mit eingeschränktem Zugang zur zahnärztlichen Versorgung (Petersen, 2022).
Zahninfektionen fallen in drei Hauptkategorien basierend auf Standort und Ursprung. Periapikale Abszesse bilden sich an der Wurzelspitze, wenn das Pulpagewebe durch tiefe Karies oder Trauma abstirbt. Parodontalabszesse entwickeln sich in den unterstützenden Strukturen eines Zahns, der von fortgeschrittener Zahnfleischerkrankung betroffen ist. Gingivalabszesse bleiben auf den Zahnfleischrand beschränkt und werden normalerweise durch das Eindringen eines Fremdkörpers verursacht.
Die klinische Relevanz von Zahninfektionen geht über orale Beschwerden hinaus. Forschungen, die im Journal of Dental Research veröffentlicht wurden, zeigen, dass unbehandelte Zahninfektionen das kardiovaskuläre Risiko erhöhen, das Diabetesmanagement komplizieren und systemische Entzündungsmarker erhöhen (Lockhart, 2019). Im Jahr 2023 behandelten Notaufnahmen in den Vereinigten Staaten über 2 Millionen Fälle von Zahninfektionen, wobei die durchschnittlichen Behandlungskosten über 1.000 USD pro Besuch lagen, wenn eine Hospitalisierung notwendig wurde.
Eine frühzeitige Diagnose ist wichtig, da Zahninfektionen einem vorhersehbaren Verlauf folgen. Bakterien vermehren sich im begrenzten Raum eines Zahnwurzel- oder Zahnfleischtaschen. Der Druck steigt. Das Gewebe schwillt an. Die Immunreaktion löst Fieber und Unwohlsein aus. Ohne Intervention durchbricht die Infektion lokale Barrieren und gelangt in fasziale Räume, lymphatische Kanäle oder den Blutkreislauf.
Das Behandlungsspektrum reicht von lokalen Interventionen bis zu systemischen Therapien. Lokale Ansätze, Drainage, Wurzelkanaltherapie, Extraktion, beseitigen die Infektionsquelle direkt. Systemische Ansätze, hauptsächlich Antibiotika, unterstützen die Abwehr des Körpers, wenn sich die Infektion über den Zahn hinaus ausbreitet. Das Schlüsselprinzip: Lokale Behandlung hat Vorrang. Antibiotika allein können einen infizierten Wurzelkanal oder Abszesshöhle nicht sterilisieren.
Infektionstyp | Standort | Hauptursache | Typische Behandlung |
Periapikales Abszess | Wurzelspitze | Pulpanekrose | Wurzelkanal oder Extraktion |
Parodontalabszess | Stützgewebe | Fortgeschrittene Parodontitis | Drainage + parodontaltherapie |
Zahnfleischabszess | Zahnfleischrand | Fremdkörperimpaktion | Drainage + Entfernung des Reizstoffs |
Was verursacht die Entwicklung von Zahninfektionen?
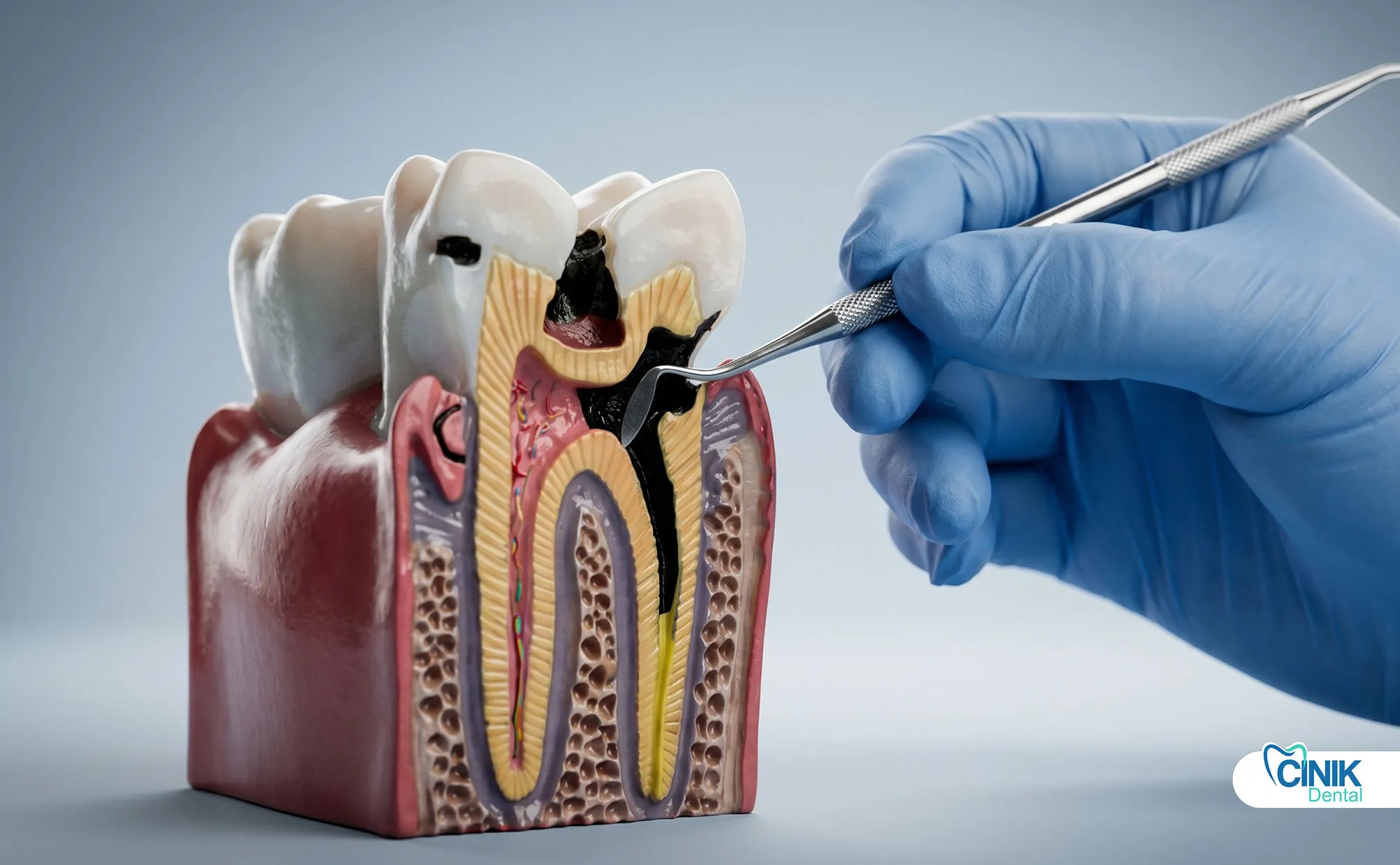
Zahnkaries, Trauma, fehlgeschlagene Restaurationen und parodontalerkrankungen ermöglichen es Bakterien, in das Zahnmark und das umliegende Gewebe einzudringen. Die Biofilmbildung schützt die Bakterien und beschleunigt die Gewebezerstörung.
Wie dringen Bakterien in Zahngewebe ein?
Bakterien dringen durch Zahnschmelz-Risse, tiefe Kavitäten oder Zahnfleischtaschen ein. Sie bilden Biofilme, die immunologischen Angriffen und Antibiotika widerstehen, und zerstören dann das Zahnmark, den Knochen und das Weichgewebe.
Zahninfektionen beginnen mit der bakteriellen Besiedlung. Die Mundhöhle beherbergt über 700 Bakterienarten, aber nur eine Handvoll verursacht invasive Infektionen. Streptococcus mutans initiiert Zahnverfall, indem es Zucker in Säure umwandelt. Aggregatibacter actinomycetemcomitans und Porphyromonas gingivalis treiben die parodontalen Zerstörungen voran. Wenn diese Organismen den Zahnschmelz oder die Zahnfleischabwehr durchbrechen, gelangen sie in das Zahnmark, eine sterile Kammer, die Nerven und Blutgefäße enthält.
Zahnkaries bleibt die Hauptursache für Zahnmarkinfektionen. Unbehandelte Kavitäten schreiten durch den Zahnschmelz, das Dentin und schließlich in die Zahnmarkkammer voran. Das Zahnmark reagiert mit Entzündungen, aber bakterielle Toxine und Druck töten schließlich das Gewebe. Nekrotisches Zahnmark wird zu einem Nährboden für anaerobe Bakterien.
Trauma beschleunigt das Infektionsrisiko. Rissige Zähne, selbst ohne sichtbare Brüche, ermöglichen das Eindringen von Bakterien. Fehlgeschlagene Restaurationen schaffen mikroskopisch kleine Lücken, in denen Bakterien sich ansammeln. Wurzelkanalbehandlungen, die Kanaläste übersehen, hinterlassen eine verbleibende Infektion.
Parodontalerkrankungen bieten einen alternativen Weg. Wenn sich die Zahnfleischtaschen vertiefen, wandern Bakterien entlang der Wurzeloberfläche. Das Immunsystem greift sowohl Bakterien als auch das Gewebe des Wirts an und zerstört das parodontalen Band und den Alveolarknochen. Tiefe Taschen von mehr als 7 Millimetern beherbergen häufig abszessbildende Bakterien.
Die Bildung von Biofilmen erschwert die Behandlung. Bakterien sekretieren extrazelluläre Polysaccharide, die eine schützende Matrix bilden. Dieser Biofilm schützt Organismen vor Antibiotika, Antikörpern im Speichel und Immunzellen. Innerhalb eines Biofilms kommunizieren Bakterien durch Quorum-Sensing und teilen Resistenzgene. Forschungen von Seneviratne (2017) in Periodontology 2000 bestätigen, dass in Biofilmen eingebettete Bakterien bis zu 1.000-mal höhere Antibiotikaresistenz zeigen als planktonische Zellen.
Was sind die Haupttypen von Zahninfektionen?
Periapikale Abszesse betreffen die Wurzelspitzen, parodontalen Abszesse greifen die unterstützenden Strukturen an, und gingivale Abszesse bleiben an den Zahnfleischrändern. Jeder Typ erfordert unterschiedliche Behandlungszeitpunkte und -ansätze.
Periapikales Abszess: Diese Infektion bildet sich an der Spitze einer Zahnwurzel nach einer Pulpanekrose. Eiter sammelt sich im Knochen um die Wurzelspitze. Patienten erleben stechende Schmerzen, die sich im Liegen verschlimmern. Der Zahn fühlt sich in seiner Alveole erhöht an. Schwellungen können auf der Gesichtshaut auftreten, wenn die Infektion den Knochen durchbricht. Röntgenaufnahmen zeigen einen radioluzenten Bereich an der Wurzelspitze. Eine Wurzelkanalbehandlung oder Extraktion beseitigt die Infektionsquelle.
Parodontaler Abszess: Diese Infektion entwickelt sich in einer bereits bestehenden parodontalen Tasche. Sie verursacht einen schnellen Beginn von Schmerzen, Schwellungen und eitrigem Ausfluss aus dem Zahnfleischrand. Der betroffene Zahn hat oft Beweglichkeit aufgrund von Knochenverlust. Parodontalabszesse erfordern eine Drainage durch die Zahnfleischtasche oder einen externen Schnitt. Eine Reinigung und Glättung der Wurzel folgt, um die Taschentiefe zu reduzieren.
Gingivaler Abszess: Die oberflächlichste Art, die auf den Zahnfleischrand beschränkt ist. Fremdkörper, Nahrungsansammlungen, Borsten von Zahnbürsten, Fragmente von Zahnseide lösen eine lokale Infektion aus. Die Schmerzen bleiben moderat. Die Schwellung bleibt begrenzt. Die Behandlung umfasst das Entfernen des Fremdkörpers und das Zulassen einer natürlichen Drainage.
Wie breitet sich eine Zahninfektion aus?
Infektionen breiten sich durch lokale Gewebeschichten, fasziale Räume und schließlich den Blutkreislauf aus. Gesichtsschwellungen, Schluckbeschwerden und Fieber signalisieren eine gefährliche Progression.
Die lokale Gewebeinvasion stellt die erste Phase dar. Bakterien und entzündungsfördernde Mediatoren zerstören das umliegende Knochen- und Weichgewebe. Die Abszesshöhle vergrößert sich. Druck komprimiert Nerven, was zu intensiven Schmerzen führt. Enzyme wie Kollagenase bauen die Barrieren des Bindegewebes ab.
Die Beteiligung von faszialen Räumen markiert eine gefährliche Eskalation. Das Gesicht und der Hals enthalten mehrere Bindegewebskompartimente, die durch fasziale Schichten getrennt sind. Bakterien wandern entlang dieser Ebenen und erzeugen lebensbedrohliche Schwellungen. Die Infektion des submandibulären Raums (Ludwig-Angina) kann die Atemwege blockieren. Der sinus cavernosus, der über die Drainage der Gesichtsvenen zugänglich ist, birgt das Risiko einer Thrombose und einer Gehirninfektion.
Die systemische Verbreitung tritt auf, wenn Bakterien in Blutgefäße gelangen. Bakteriämie, das Vorhandensein von Bakterien im Blut, tritt während zahnärztlicher Eingriffe und sogar beim kräftigen Zähneputzen auf. Bei gesunden Personen beseitigen Immunzellen die vorübergehende Bakteriämie. Bei immungeschwächten Patienten oder solchen mit schweren Infektionen schreitet die Bakteriämie zur Sepsis fort. Endokarditis, eine Infektion der Herzklappen, stellt ein besonderes Risiko für Patienten mit Prothesenklappen oder früheren Herzschäden dar.
Verbreitungsstufe | Standort | Warnsignale | Risikostufe |
Lokalisiert | Zahn und unmittelbarer Knochen | Zahnschmerzen, leichte Schwellung | Niedrig |
Regional | Faszialräume des Gesichts/Halses | Gesichtsschwellung, Trismus, Dysphagie | Mäßig-Hoch |
Systemisch | Blutbahn und entfernte Organe | Fieber, Tachykardie, Hypotonie, Verwirrung | Kritisch |
Wie erkennen und diagnostizieren Zahnärzte Zahninfektionen?
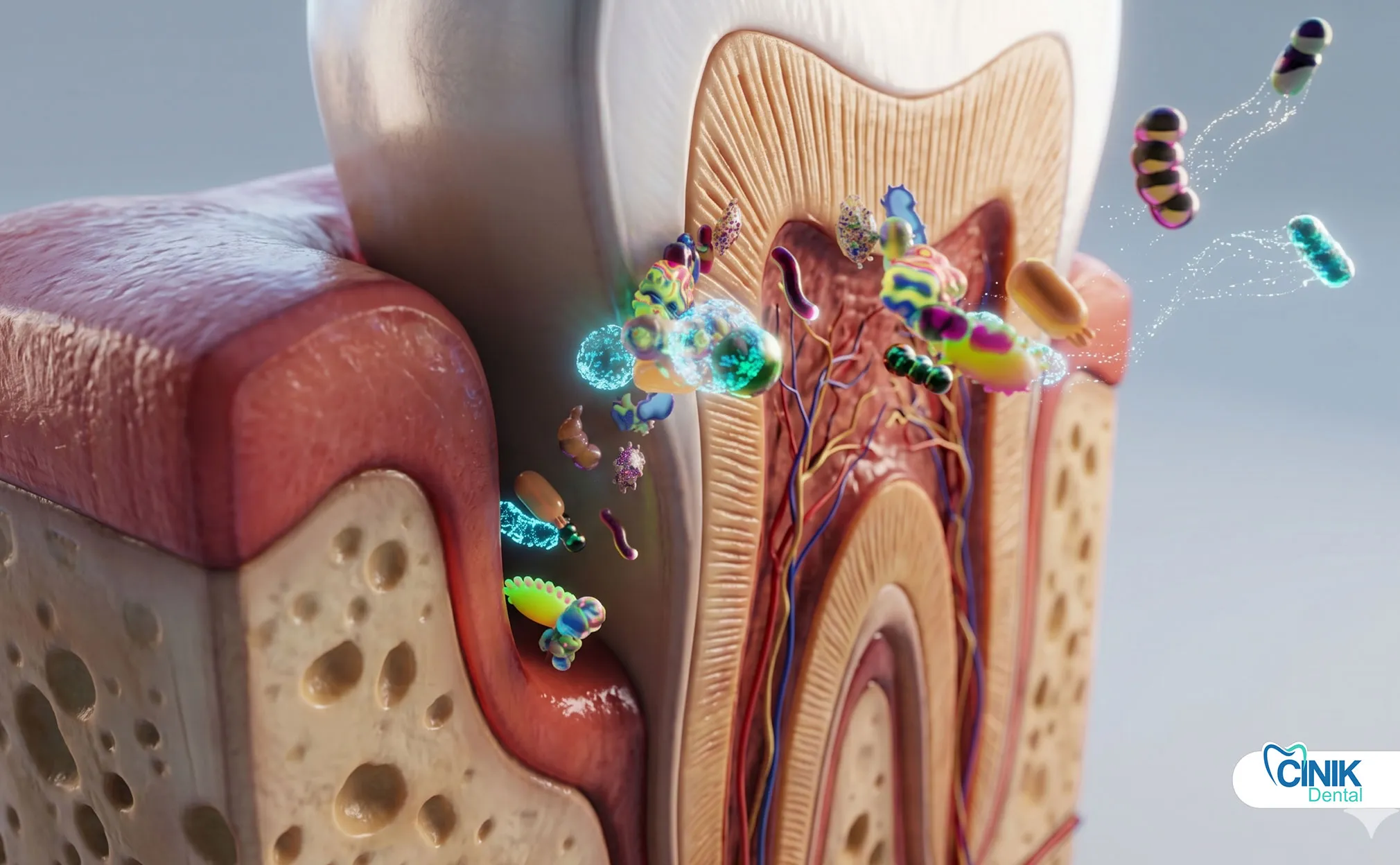
Zahnärzte verwenden klinische Untersuchungen, Patientensymptome, radiografische Bildgebung und Pulpatests, um Art, Schwere und Ausmaß der Infektion zu identifizieren.
Welche Symptome deuten auf eine Zahninfektion hin?
Starke, pochende Zahnschmerzen, Gesichtsschwellung, Rötung des Zahnfleisches, Temperaturempfindlichkeit und Fieber deuten auf eine aktive Infektion hin, die eine sofortige Bewertung erfordert.
Schmerzen sind das Hauptsymptom. Infizierte Zähne verursachen tiefes, pochendes Schmerzempfinden, das Patienten als unerträglich beschreiben. Der Schmerz verstärkt sich bei Wärmeexposition und kann bei kalter Anwendung in der frühen Pulpitis kurzzeitig abnehmen. Sobald die Pulpa nekrotisiert, verschwindet die Kälteempfindlichkeit, aber der Druckschmerz nimmt zu, während sich Eiter unter der Wurzel ansammelt.
Schwellungen signalisieren fortschreitende Infektionen. Frühe Infektionen verursachen Schwellungen des Zahnfleisches im Mund. Mit zunehmendem Druck breitet sich die Schwellung auf die Gesichtshaut aus. Die Haut wird rot, warm und gespannt. Patienten berichten möglicherweise, dass die Schwellung plötzlich auftrat und sich über Stunden ausbreitete.
Systemische Symptome deuten auf eine sich ausbreitende Infektion hin. Fieber über 38°C (100,4°F) deutet auf eine Immunmobilisierung gegen eine signifikante bakterielle Belastung hin. Unwohlsein, Appetitlosigkeit und Schwierigkeiten beim Öffnen des Mundes (Trismus) begleiten die Beteiligung des fascialen Raums. Schwierigkeiten beim Schlucken (Dysphagie) oder Atmen stellen ein Risiko für die Atemwege dar.
Welche diagnostischen Werkzeuge bestätigen Zahninfektionen?
Klinische Palpation, Perkussionstests, Röntgenaufnahmen, CBCT-Scans und elektrische Pulptest bestätigen das Vorhandensein, den Standort und den Vitalitätsstatus des Zahns.
Die klinische Untersuchung liefert sofortige Hinweise. Zahnärzte palpieren geschwollene Bereiche, um die Fluktuation zu beurteilen; weiche, mit Flüssigkeit gefüllte Schwellungen deuten auf eine Ansammlung von Eiter hin. Perkussionstests klopfen Zähne mit einem stumpfen Instrument; infizierte Zähne übertragen Vibrationen schmerzhaft durch entzündete parodontalen Bänder. Mobilitätstests identifizieren Zähne mit fortgeschrittenem Knochenverlust durch parodontalen Abszesse.
Radiografische Bildgebung visualisiert Knochenschäden. Standardmäßige periapikale Röntgenaufnahmen zeigen radioluzente Bereiche an den Wurzelspitzen, die auf Knochenverlust durch periapikale Abszesse hinweisen. Bissflügel-Röntgenaufnahmen zeigen tiefe Karies und parodontalen Knochenstand. Allerdings verpassen 2D-Röntgenaufnahmen frühe Infektionen und komplexe Anatomie.
Die Cone-Beam-Computertomographie (CBCT) bietet eine dreidimensionale Visualisierung. Diese Technologie erkennt Abszesse, bevor sichtbare Knochenschäden auf Standard-Röntgenaufnahmen erscheinen. CBCT identifiziert zusätzliche Wurzelkanäle, Wurzelfrakturen und präzise Ausbreitungsmuster in fascialen Räumen. Forschungen von Patel (2019) im International Endodontic Journal bestätigen, dass CBCT 40% mehr periapikale Läsionen erkennt als die konventionelle Radiographie.
Die Vitalitätstests des Zahnnervs unterscheiden reversible von irreversiblen Zuständen. Elektrische Pulstester stimulieren die Nervenreaktion; nicht vitale Zähne zeigen kein Gefühl. Kältetests mit Kühlmittel-Spray bewerten die Nervenfunktion. Eine nekrotische Pulpa reagiert nicht auf Kälte, während eine entzündete vitale Pulpa übertriebene, anhaltende Schmerzen verursacht.
Was sind die Grundprinzipien der Behandlung von Zahninfektionen?
Entfernen Sie zuerst die Infektionsquelle durch Drainage, Wurzelkanal oder Extraktion. Verwenden Sie Antibiotika nur, wenn sich die Infektion systemisch ausbreitet. Verlassen Sie sich niemals allein auf Antibiotika.
Das Hauptziel der Behandlung von Zahninfektionen ist die Kontrolle der Quelle. Antibiotika zirkulieren im Blut, können jedoch nicht in nekrotische Pulpenkammern, Abszesshöhlen oder durch Biofilme geschützte Bakterienkolonien eindringen. Die Infektionsquelle, eine tote Pulpa, angesammelter Eiter oder eine erkrankte parodontal Tasche, muss physisch entfernt werden.
Drainage und Débridement bilden die Grundlage der Quellenkontrolle. Eine Abszesshöhle enthält Eiter, bakterielle Toxine und entzündliche Flüssigkeit. Inzision und Drainage setzen dieses Material frei, reduzieren den Druck und die bakterielle Last. Die Wurzelkanalbehandlung entfernt infiziertes Pulpagewebe aus dem Zahn. Die Extraktion beseitigt die gesamte infizierte Struktur.
Konservative Ansätze erhalten natürliche Zähne, wenn möglich. Die Wurzelkanalbehandlung rettet Zähne mit periapikalen Abszessen, wenn genügend Zahnsubstanz für die Restauration verbleibt. Parodontalabszesse sprechen oft auf Drainage in Kombination mit einer gründlichen Reinigung an. Die Extraktion wird notwendig, wenn Zähne Frakturen unterhalb des Zahnfleischrandes, schweren Knochenverlust oder gescheiterte frühere Wurzelkanalbehandlungen aufweisen.
Chirurgische Ansätze befassen sich mit komplexen Fällen. Apikoektomie, chirurgische Entfernung der Wurzelspitze, rettet Zähne mit persistierender periapikaler Infektion nach der Wurzelkanalbehandlung. Parodontalchirurgie reduziert tiefe Taschen, die wiederkehrende Abszesse beherbergen. Krankenhausbasierte Chirurgie behandelt Infektionen im fascialen Raum, die einen Schutz der Atemwege erfordern.
Wichtige klinische Erkenntnis: Lokale Behandlung hat Vorrang vor Antibiotika. Ein Patient mit einem zahnärztlichen Abszess, der nur Antibiotika erhält, erfährt vorübergehende Linderung der Symptome, sieht sich jedoch einer garantierten Rückkehr gegenüber. Die Abszesshöhle bleibt. Bakterien besiedeln erneut. Ohne Drainage oder Zahnbehandlung kehrt die Infektion zurück, oft mit antibiotikaresistenten Organismen.
Welche zahnärztlichen Verfahren behandeln Infektionen zuerst?
Zahnärzte priorisieren Inzision und Drainage bei Abszessen, Wurzelkanalbehandlungen für erhaltbare Zähne und Extraktionen für nicht restaurierbare Zähne. Diese Verfahren beseitigen die Infektionsquellen direkt.
Wie funktioniert die Abszessdrainage?
Der Zahnarzt betäubt den Bereich, macht einen kleinen Schnitt in den Abszess und lässt Eiter abfließen. Dies reduziert sofort Schmerzen und Druck, während die bakterielle Last entfernt wird.
Inzision und Drainage bieten die schnellste Schmerzlinderung bei akuten Abszessen. Das Verfahren erfordert eine lokale Anästhesie. Der Zahnarzt identifiziert den fluktuierendsten (weichsten, am meisten mit Flüssigkeit gefüllten) Bereich der Schwellung. Ein Skalpellschnitt, typischerweise 1-2 Zentimeter, dringt bis zur Abszesshöhle vor. Eiter wird unter Druck evakuiert. Der Zahnarzt kann einen kleinen Gummischlauch einführen, um die Öffnung für 24-48 Stunden aufrechtzuerhalten.
Sofortige Vorteile umfassen Druckreduzierung und Schmerzlinderung. Patienten berichten oft von dramatischen Verbesserungen innerhalb von Stunden. Die Drainage entfernt auch das bakterielle Inokulum, wodurch die systemische bakterielle Last verringert wird. Das Verfahren dauert 15-30 Minuten in einer Zahnarztpraxis.
Die Nachsorge nach der Drainage umfasst warme Kochsalzspülungen, um die Durchgängigkeit des Abflusses aufrechtzuerhalten. Patienten setzen die Einnahme von Antibiotika fort, wenn systemische Symptome bestehen. Die definitive Zahnbehandlung, Wurzelkanal oder Extraktion, erfolgt, sobald die akute Schwellung nachlässt, normalerweise innerhalb von 3-7 Tagen.
Wann rettet die Wurzelkanalbehandlung einen infizierten Zahn?
Die Wurzelkanaltherapie entfernt infiziertes Gewebe, desinfiziert die Wurzelkanäle und versiegelt den Zahn. Sie erhält natürliche Zähne, wenn genügend Struktur für die Kronenrestauration verbleibt.
Die Wurzelkanaltherapie behandelt periapikale Abszesse, indem der Inhalt der infizierten Pulpa entfernt wird. Der Zahnarzt schafft eine Zugangsöffnung durch die Zahnkrone. Instrumente entfernen das Pulpagewebe, nekrotische Rückstände und bakteriellen Biofilm aus dem Kanalsystem. Chemische Spülmittel, Natriumhypochlorit und Chlorhexidin, desinfizieren die Kanalwände.
Das Verfahren erfordert 1-3 Termine, abhängig von der Schwere der Infektion. Der erste Besuch konzentriert sich auf die Entfernung der Pulpa und die Drainage des Abszesses durch den Zahn. Der Zahnarzt platziert antibakterielle Medikamente im Kanal und versiegelt eine temporäre Füllung. Der zweite Besuch bestätigt die Infektionskontrolle, bevor die Kanäle mit Guttapercha, einem gummiartigen Material, gefüllt werden. Eine permanente Krone stellt die Zahnstärke wieder her.
Die Erfolgsquote übersteigt 90 % bei primären Wurzelkanalbehandlungen. Forschungen von Ng (2011) im International Endodontic Journal berichten von einer Überlebensrate von 94 % nach 4 Jahren für Zähne mit periapikalen Abszessen, die mit Wurzelkanaltherapie und Kronenrestauration behandelt wurden. Misserfolge resultieren typischerweise aus verpassten Kanalästen, persistentem bakteriellen Biofilm oder koronaler Undichtigkeit.
Wann muss ein infizierter Zahn extrahiert werden?
Die Extraktion wird notwendig, wenn Zähne Frakturen unterhalb der Zahnfleischlinie, schweren Knochenverlust, gescheiterte Wurzelkanalretreatment oder unzureichende Struktur für die Restauration aufweisen.
Die Zahnextraktion bietet eine definitive Beseitigung der Infektion, wenn eine Erhaltung unmöglich ist. Vertikale Wurzelfrakturen, die unterhalb der Zahnfleischlinie reichen, verhindern eine bakterielle Abdichtung, unabhängig von der Behandlung. Schwere Parodontalerkrankungen, die mehr als 50 % des unterstützenden Knochens zerstören, machen Zähne nicht restaurierbar. Gescheiterte Wurzelkanalretreatments, insbesondere bei persistierenden periapikalen Läsionen, können eine Extraktion und Implantat-Ersatz rechtfertigen.
Das Extraktionsverfahren für infizierte Zähne erfordert Sorgfalt, um die bakterielle Ausbreitung zu verhindern. Der Zahnarzt kann präoperative Antibiotika für immungeschwächte Patienten oder schwere Infektionen verschreiben. Lokalanästhesie mit Vasokonstriktor kontrolliert die Blutung. Der Zahnarzt hebt den Zahn aus seiner Alveole, entfernt das Granulationsgewebe von der Basis der Alveole und sorgt für eine vollständige Debridement.
Die Heilung nach der Extraktion dauert 1-2 Wochen für den Verschluss des Weichgewebes. Die Knochenremodellierung dauert 3-6 Monate. Die sofortige Implantation, die in ausgewählten Fällen durchgeführt wird, verkürzt die Behandlungszeit, erfordert jedoch infektionsfreie Extraktionsstellen.
Evidenzbasierte Anmerkung: Definitive zahnärztliche Verfahren bleiben unerlässlich, da Antibiotika die Infektionsquellen nicht beseitigen können. Eine systematische Überprüfung von Cope (2014) im British Dental Journal analysierte 22 klinische Studien und kam zu dem Schluss, dass Antibiotika ohne Quellenkontrolle keinen nachhaltigen Nutzen bei zahnärztlichen Abszessen bieten. Das Wiederauftreten von Symptomen tritt in 100 % der Fälle innerhalb von Wochen auf.
Verfahren | Indikation | Erfolgsquote | Genesungszeit |
Inzision und Drainage | Akuter Abszess mit schwankender Schwellung | Sofortige Linderung; erfordert Nachsorge | 2-3 Tage |
Wurzelkanalbehandlung | Periapikaler Abszess, erhaltungswürdiger Zahn | 90-95% nach 5 Jahren | 1-2 Wochen |
Zahnentfernung | Nicht erhaltungswürdiger Zahn, gescheiterte Nachbehandlung | 100% Infektionselimination | 1-2 Wochen Weichgewebe |
Wie unterstützen Antibiotika die Behandlung von Zahninfektionen?
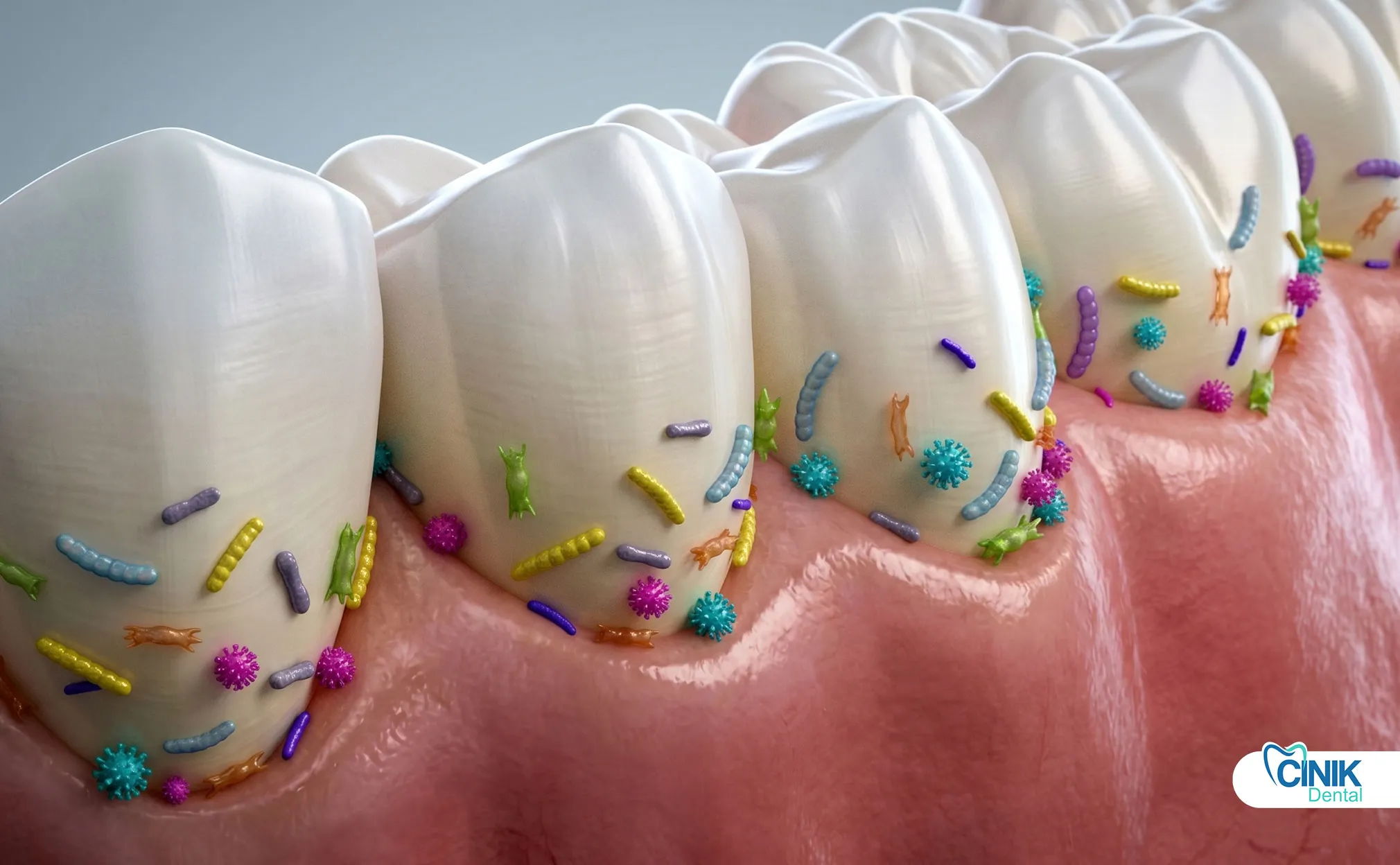
Antibiotika behandeln sich ausbreitende Infektionen mit Fieber, Gesichtszellulitis oder Immunschwäche. Sie ersetzen niemals Drainage oder Zahnbehandlung. Amoxicillin bleibt die erste Wahl.
Wann verschreiben Zahnärzte Antibiotika?
Zahnärzte verschreiben Antibiotika bei systemischen Symptomen, sich ausbreitender Zellulitis, immungeschwächten Patienten oder wenn sofortige zahnärztliche Eingriffe unmöglich sind.
Antibiotika spielen eine unterstützende Rolle im Management von Zahninfektionen. Sie heilen keine Zahnabszesse. Sie kontrollieren die bakterielle Ausbreitung, wenn die Infektion die lokale Eindämmung überschreitet. Zu den spezifischen Indikationen gehören:
Systemische Beteiligung: Fieber über 38°C, Unwohlsein oder Lymphadenopathie weisen auf eine bakterielle Belastung hin, die die lokale Immunfähigkeit überschreitet. Antibiotika reduzieren das Risiko einer Bakteriämie und unterstützen die systemische Genesung.
Ausbreitende Infektion: Cellulitis, diffuse Hautrötung ohne lokalisierten Abszess, erfordert Antibiotika, da eine Drainage nicht möglich ist. Infektionen, die in fasziale Räume eindringen, benötigen eine aggressive antibiotische Abdeckung, während auf chirurgische Eingriffe gewartet wird.
Immunokompromittierte Zustände: Patienten mit Diabetes, HIV, Chemotherapie oder Organtransplantationen haben ein höheres Risiko für Sepsis. Eine frühzeitige antibiotische Intervention schützt diese gefährdeten Bevölkerungsgruppen.
Prophylaxe bei Eingriffen: Bestimmte medizinische Bedingungen erfordern eine antibiotische Abdeckung vor zahnärztlichen Eingriffen, um Infektionen an entfernten Stellen zu verhindern. Prothetische Herzklappen, frühere infektiöse Endokarditis und einige orthopädische Implantate fallen in diese Kategorie.
Wichtiges Prinzip: Antibiotika sind unterstützend, nicht primäre Therapie. Ein Patient mit einem lokalisierten Zahnabszess und ohne systemische Symptome benötigt keine Antibiotika. Der Zahnarzt führt eine Drainage und Zahnbehandlung durch. Das Hinzufügen von Antibiotika bietet keinen Nutzen und trägt zur Resistenz bei.
Welche Antibiotika wirken am besten bei Zahninfektionen?
Amoxicillin bleibt das Antibiotikum der ersten Wahl aufgrund seiner Wirksamkeit gegen typische orale Erreger und hervorragende Verträglichkeit. Penicillin V dient als Alternative.
Amoxicillin dominiert die Verschreibung von zahnärztlichen Antibiotika der ersten Wahl. Diese Aminopenicillin deckt die grampositiven Kokken (Streptococcus -Arten) und gramnegativen Anaerobier (Prevotella, Fusobacterium) ab, die die meisten Zahninfektionen verursachen. Die orale Absorption erreicht 90%, was zuverlässige Blutspiegel erzeugt. Die Standarddosis für Erwachsene beträgt 500 mg dreimal täglich für 5-7 Tage.
Klinische Evidenz: Eine randomisierte kontrollierte Studie von Matthews (2016) im Journal of Antimicrobial Chemotherapy verglich Amoxicillin mit Placebo bei Zahnabszessen. Beide Gruppen erhielten Inzision und Drainage. Amoxicillin reduzierte die Schwellung nach dem Eingriff um 35% und verkürzte die Genesung um 2 Tage. Die Heilungsraten nach 30 Tagen waren jedoch identisch, was bestätigt, dass die Kontrolle der Quelle, nicht Antibiotika, die Ergebnisse bestimmt.
Penicillin V bietet eine Alternative mit einem engeren Spektrum. Dieses Phenoxymethylpenicillin widersteht der Zersetzung durch Magensäure, was es für die orale Anwendung geeignet macht. Die typische Dosis beträgt 500 mg viermal täglich. Penicillin V deckt die meisten odontogenen Erreger ab, hat jedoch im Vergleich zu Amoxicillin keine Abdeckung gegen gramnegative Anaerobier.
Welche Antibiotika helfen, wenn Medikamente der ersten Wahl versagen?
Metronidazol zielt auf Anaerobier ab und wird mit Amoxicillin bei schweren Infektionen kombiniert. Clindamycin ersetzt Penicillin bei allergischen Patienten. Azithromycin bietet eine weitere Alternative.
Metronidazol zielt speziell auf obligate anaerobe Bakterien ab. Diese Organismen dominieren nekrotisches Gewebe und tiefe parodontalen Taschen. Metronidazol allein deckt keine aeroben Streptokokken ab, daher kombinieren Zahnärzte es oft mit Amoxicillin bei schweren, gemischten Infektionen. Die Dosis beträgt 400 mg dreimal täglich. Patienten müssen während der Behandlung und 48 Stunden nach Abschluss auf Alkohol verzichten, da es zu disulfiramähnlichen Reaktionen kommen kann.
Clindamycin dient Patienten mit Penicillinallergie. Dieses Lincosamid-Antibiotikum deckt grampositive Organismen und Anaerobier effektiv ab. Die Dosis beträgt 300 mg viermal täglich. Zahnärzte reservieren Clindamycin für echte Penicillinallergien, da es ein höheres Risiko für Clostridioides difficile Kolitis, eine schwere Darminfektion, birgt.
Azithromycin bietet eine weitere Alternative für Patienten mit Penicillinallergie. Dieses Makrolid-Antibiotikum bietet eine bequeme Dosierung, 500 mg täglich für 3 Tage, aufgrund seiner langen Gewebehalbwertszeit. Allerdings begrenzt der zunehmende Widerstand unter oralen Streptokokken seine Zuverlässigkeit. Zahnärzte verwenden Azithromycin, wenn Clindamycin kontraindiziert ist.
Warum bedroht Antibiotikaresistenz die zahnärztliche Behandlung?
Die Überverschreibung von zahnärztlichen Antibiotika beschleunigt die bakterielle Resistenz. Richtlinien raten mittlerweile von der routinemäßigen Anwendung von Antibiotika bei lokalisierten Infektionen ohne systemische Ausbreitung ab.
Antibiotikaresistenz untergräbt das Management zahnärztlicher Infektionen. Die Centers for Disease Control and Prevention identifizieren die zahnärztliche Verschreibung als einen wesentlichen Beitrag zur unnötigen Anwendung von Antibiotika. Studien schätzen, dass 30-50% der zahnärztlichen Antibiotikaverschreibungen unnötig sind, da sie für Bedingungen gegeben werden, bei denen die Kontrolle der Quelle allein ausreicht.
Die Folgen gehen über einzelne Patienten hinaus. Resistente Bakterien kolonisieren die Mundhöhle und breiten sich auf Familienmitglieder, Gesundheitseinrichtungen und Gemeinschaften aus. Streptococcus pneumoniae und Staphylococcus aureus Stämme, die resistent gegen Penicillin und Clindamycin sind, treten zunehmend bei zahnärztlichen Infektionen auf.
Programme zur Antibiotikaüberwachung zielen auf die Überverschreibung in der Zahnmedizin ab. Die American Dental Association aktualisierte 2019 die Richtlinien und stellte ausdrücklich fest, dass Antibiotika bei lokalisierten intraoralen Schwellungen ohne systemische Beteiligung nicht angezeigt sind. Die Richtlinien betonen: "Die primäre Methode zur Behandlung einer zahnärztlichen Infektion sollte die Kontrolle der Quelle sein."
Gezielte Therapie ersetzt die empirische Verschreibung in wiederkehrenden oder komplexen Fällen. Kultur- und Empfindlichkeitstests identifizieren spezifische Bakterien und deren Resistenzmuster. Dieser Ansatz, der in Krankenhausumgebungen Standard ist, wird in der zahnärztlichen Praxis für immungeschwächte Patienten oder Behandlungsfehler zunehmend häufiger.
Antibiotikum | Spektrum | Typische Dosis | Am besten für |
Amoxicillin | Breit (aerobe + anaerobe) | 500 mg TID x 5-7 Tage | Erste Wahl, die meisten Infektionen |
Penicillin V | Eng (aerobe) | 500 mg QID x 5-7 Tage | Milde Infektionen, Penicillin-Präferenz |
Metronidazol | Nur Anaerobier | 400 mg TID x 5-7 Tage | Kombiniert mit Amoxicillin für schwere Fälle |
Clindamycin | Aerobe + Anaerobe | 300 mg QID x 5-7 Tage | Penicillin-Allergie |
Azithromycin | Breit | 500 mg täglich x 3 Tage | Penicillinallergie, Clindamycin kontraindiziert |
Wie gehen Zahnärzte mit Schmerzen während der Infektionsbehandlung um?
NSAIDs wie Ibuprofen bieten eine überlegene Schmerzlinderung bei Zahnschmerzen im Vergleich zu Opioiden. Paracetamol bietet eine Alternative für Patienten, die keine NSAIDs einnehmen können. Lokalanästhesie während der Eingriffe beseitigt Verfahrensschmerzen.
Das Schmerzmanagement bei Zahninfektionen folgt einem multimodalen Ansatz. Nicht-steroidale entzündungshemmende Medikamente (NSAIDs) bilden das Fundament. Ibuprofen, 400-600 mg alle 6-8 Stunden, reduziert die Entzündung am Infektionsort und bietet Analgesie. Forschungen von Moore (2015) in der Cochrane-Datenbank für systematische Übersichten bestätigen, dass Ibuprofen 400 mg eine bessere Schmerzlinderung bietet als Codein 60 mg bei Zahnschmerzen, mit weniger Nebenwirkungen.
Paracetamol dient Patienten mit NSAID-Kontraindikationen, peptischen Geschwüren, Antikoagulationstherapie oder Nierenfunktionsstörungen. Die Dosis beträgt 500-1000 mg alle 6 Stunden, nicht mehr als 3000 mg täglich. Paracetamol hat keine entzündungshemmende Wirkung, bietet jedoch eine effektive Analgesie.
Die Kombinationstherapie verbessert die Schmerzbekämpfung. Das abwechselnde Einnehmen von Ibuprofen und Paracetamol hält die Medikamentenspiegel konstant. Einige Studien legen nahe, dass die gleichzeitige Verabreichung eine bessere Linderung als jedes Medikament allein bietet, obwohl die Patienten die Dosierungsintervalle sorgfältig verfolgen müssen, um eine Überdosierung zu vermeiden.
Die Verschreibung von Opioiden ist in der zahnärztlichen Praxis dramatisch zurückgegangen. Die Opioid-Epidemie führte zu einer Neubewertung der Schmerzprotokolle in der Zahnmedizin. Aktuelle Richtlinien reservieren Opioide für schwere postoperative Schmerzen, die nicht auf NSAIDs ansprechen. Wenn sie verschrieben werden, beschränken Zahnärzte die Mengen auf 3-5 Tage und kombinieren sie mit NSAIDs, um den Opioidbedarf zu reduzieren.
Unterstützende Maßnahmen ergänzen die Medikation. Eine ausreichende Flüssigkeitszufuhr erhält den Speichelfluss und unterstützt die Immunfunktion. Warme Salzwasserspülungen (einen halben Teelöffel Salz in warmem Wasser, 30 Sekunden spülen) reduzieren die bakterielle Last und fördern die Drainage aus Zahnfleischtaschen. Weiche Nahrungsmittel verhindern mechanische Reizungen des infizierten Gewebes. Das Hochlagern des Kopfes während des Schlafs reduziert den Blutfluss zu geschwollenen Gesichtsteilen und verringert pochende Schmerzen.
Was passiert, wenn Zahninfektionen unbehandelt bleiben?
Unbehandelte Zahninfektionen verursachen lokale Knochenschäden, Gewebsnekrose und potenziell tödliche systemische Komplikationen, einschließlich Sepsis, Atemwegsobstruktion und Gehirnabszess.
Welche lokalen Schäden verursachen unbehandelte Infektionen?
Unbehandelte Infektionen zerstören den Kieferknochen (Osteomyelitis), töten Weichgewebe (Nekrose) und breiten sich durch Gesichtsbereiche aus, was zu Entstellungen und Funktionsverlust führt.
Osteomyelitis stellt eine Knocheninfektion durch bakterielle Besiedelung dar. Der Kieferknochen entwickelt Bereiche von totem Knochen (Sequestra), die von entzündetem Gewebe umgeben sind. Chronische Osteomyelitis verursacht anhaltende Schmerzen, abfließende Fisteln und pathologische Frakturen. Die Behandlung erfordert langanhaltende Antibiotika (4-6 Wochen) und chirurgische Entfernung von totem Knochen. Hyperbare Sauerstofftherapie unterstützt die Heilung in refraktären Fällen.
Gewebsnekrose tritt auf, wenn eine Infektion die Blutversorgung beeinträchtigt. Der Gaumen, die Zunge oder die Gesichtshaut können schwarze, vitalitätslose Bereiche entwickeln, die eine chirurgische Debridement erfordern. Nekrotisierende Fasziitis, obwohl selten bei Zahninfektionen, zerstört Gewebeschichten schnell und erfordert eine Notfalloperation.
Infektionen der Gesichtsbereiche verzerren die Anatomie. Die submandibulären, pterygomandibulären und caninen Räume schwellen dramatisch an. Patienten entwickeln ein "Stiernacken"-Erscheinungsbild aufgrund der bilateralen Beteiligung der Submandibula. Trismus, Kieferverriegelung durch Muskelentzündung, verhindert das Essen und Sprechen.
Welche systemischen Risiken schaffen Zahninfektionen?
Bakterien aus Zahninfektionen gelangen in den Blutkreislauf, was zu Sepsis, Herzklappeninfektionen und entfernten Abszessen führt. Eine Atemwegsobstruktion durch Halsanschwellung kann zu Erstickung führen.
Sepsis stellt die gefürchtetste systemische Komplikation dar. Bakterielle Toxine lösen massive Immunaktivierung aus. Fieber, schnelle Herzfrequenz, schnelles Atmen und Verwirrung signalisieren Sepsis. Der Blutdruck sinkt. Organe versagen. Septischer Schock hat eine Sterblichkeitsrate von 40%, selbst bei intensivmedizinischer Behandlung. Zahninfektionen verursachen 10-15% aller Fälle von Gesichtsepsis.
Atemwegsobstruktion bedroht das Leben innerhalb von Stunden. Ludwig-Angina, eine bilaterale Infektion des submandibulären Raums, drückt die Zunge nach oben und hinten. Der Mundboden wird bretthart. Patienten sabbern, können Speichel nicht schlucken und entwickeln Stridor (geräuschvolles Atmen). Eine Notfalltracheotomie oder Intubation sichert die Atemwege vor der chirurgischen Drainage.
Hirnabszess, obwohl selten, folgt hämatogenem Ausbreitung oder direkter Ausdehnung durch die Schädelknochen. Infektionen der Frontzähne erreichen den Frontallappen. Kieferinfektionen erreichen den Temporallappen. Hirnabszesse verursachen Kopfschmerzen, Krampfanfälle, fokale Schwäche und veränderten Bewusstseinszustand. Neurochirurgische Drainage und langanhaltende Antibiotika (6-8 Wochen) behandeln diese Komplikation.
Endokarditis betrifft die Herzklappen, insbesondere bei Patienten mit bereits bestehenden Klappenerkrankungen oder Prothesenklappen. Viridans-Streptokokken aus Zahninfektionen haften an geschädigtem Endokard, bilden Vegetationen, die ins Gehirn, die Nieren und die Gliedmaßen embolisieren. Prophylaktische Antibiotika vor zahnärztlichen Eingriffen verhindern diese Komplikation bei Hochrisikopatienten.
Komplikation | Mechanismus | Sterberisiko | Behandlung erforderlich |
Osteomyelitis | Knocheninfektion und Nekrose | Niedrig | Chirurgie + 4-6 Wochen Antibiotika |
Sepsis | Bakterielle Ausbreitung im Blutstrom | 15-40% | Intensivpflege, IV-Antibiotika, Quellenkontrolle |
Ludwig's Angina | Bilateral submandibuläre Infektion | 10-20% | Notfall-Atemweg + chirurgische Drainage |
Hirnabszess | Hämatogene oder direkte Ausbreitung | 10-30% | Neurochirurgie + 6-8 Wochen Antibiotika |
Wie sollten spezielle Bevölkerungsgruppen zahnärztliche Infektionsversorgung erhalten?
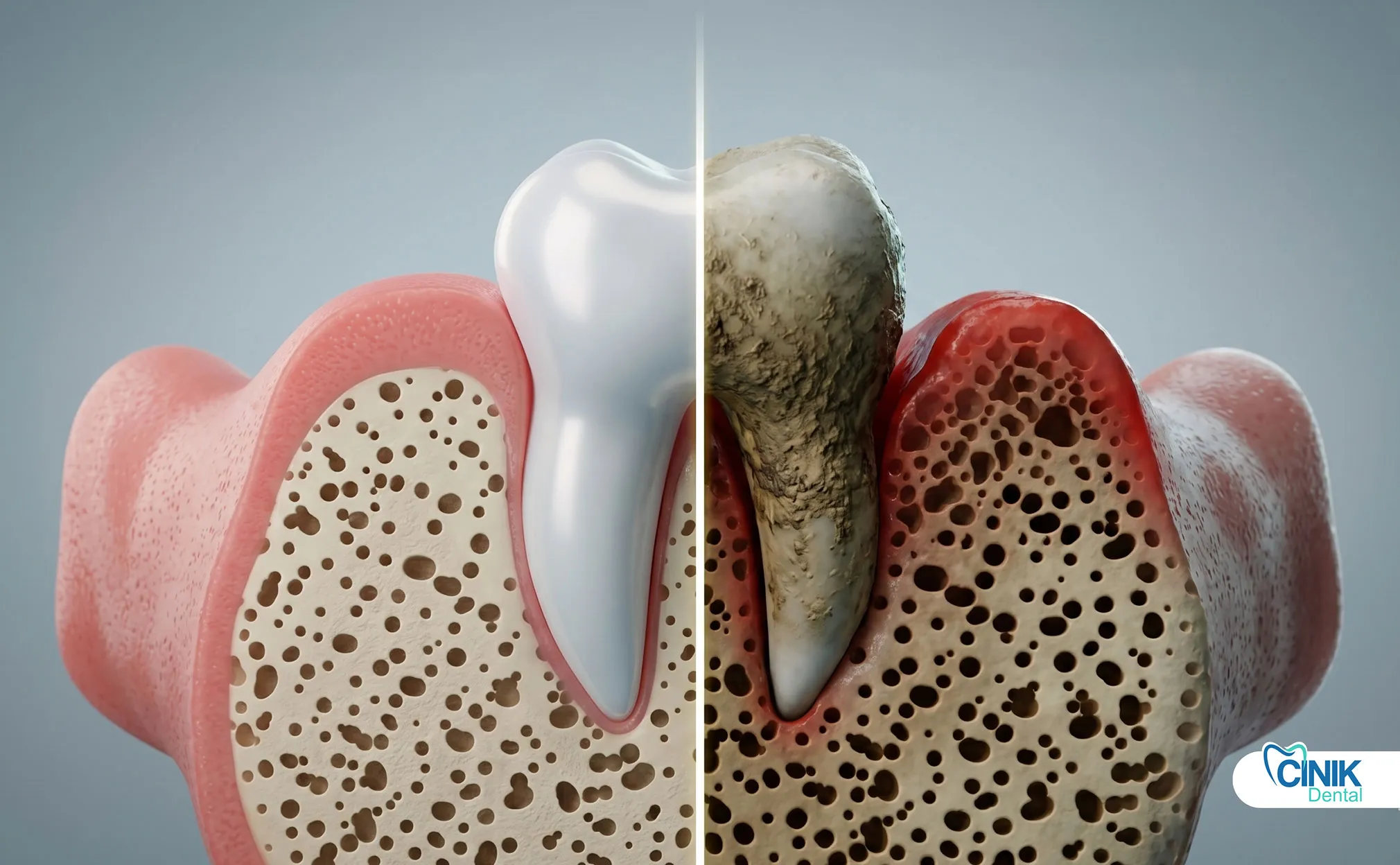
Immungeschwächte, pädiatrische und ältere Patienten benötigen angepasste Behandlungsansätze, frühere Antibiotika-Interventionen, angepasste Medikamentendosierungen und engere Überwachung.
Welche zusätzliche Pflege benötigen immungeschwächte Patienten?
Immungeschwächte Patienten haben ein höheres Risiko für systemische Ausbreitung. Sie benötigen frühere Antibiotikagaben, breitere Abdeckung, behandlungsbedürftige moderate Infektionen im Krankenhaus und längere Überwachung der Genesung.
Immungeschwächte Zustände umfassen Diabetes mellitus, HIV/AIDS, Chemotherapie, Organtransplantation, chronische Kortikosteroid-Anwendung und angeborene Immundefizienzen. Diese Bedingungen beeinträchtigen die Funktion der Neutrophilen, die Antikörperproduktion oder die zellvermittelte Immunität, die entscheidende Abwehrmechanismen gegen zahnmedizinische Krankheitserreger sind.
Ein höheres Risiko für die Ausbreitung von Infektionen erfordert ein aggressives Management. Ein lokalisierter Abszess bei einem gesunden Patienten kann Tage lang begrenzt bleiben. Der gleiche Abszess bei einem neutropenischen Chemotherapie-Patienten kann innerhalb von Stunden zu einer Sepsis fortschreiten. Zahnärzte senken die Schwellenwerte für den Beginn von Antibiotika und die Überweisung ins Krankenhaus.
Frühe Antibiotika-Intervention verwendet breitere Spektrum-Abdeckung. Während gesunde Patienten nur Amoxicillin erhalten, benötigen immungeschwächte Patienten möglicherweise Amoxicillin-Clavulansäure (Augmentin) für eine verbesserte Abdeckung von Anaerobiern oder sogar intravenöse Antibiotika für die Krankenhausaufnahme.
Eine behandlungsbedürftige Infektion im Krankenhaus wird notwendig für Infektionen, die bei gesunden Patienten in der Praxis behandelt werden würden. IV-Zugang ermöglicht eine zuverlässige Medikamentenabgabe. Die Überwachung verfolgt Temperatur, weiße Blutkörperchen und Entzündungsmarker. Chirurgische Teams stehen bereit für das Management der Atemwege, falls eine Beteiligung des faszialen Raums auftritt.
Wie passen Zahnärzte die Behandlung für Kinder und ältere Patienten an?
Kinder benötigen gewichtsbasiertes Dosing und Verhaltensmanagement. Ältere Patienten benötigen eine Beurteilung der Nierenfunktion, eine Überprüfung von Arzneimittelwechselwirkungen und die Berücksichtigung von Begleiterkrankungen.
Pädiatrische Zahninfektionen stellen einzigartige Herausforderungen dar. Milchzähne mit periapikalen Abszessen erfordern oft eine Extraktion anstelle einer Wurzelkanaltherapie aufgrund der komplexen Wurzelanatomie und des bevorstehenden Exfoliationszeitpunkts. Platzhalter verhindern kieferorthopädische Komplikationen nach vorzeitigem Zahnverlust. Die Antibiotika-Dosierung erfolgt nach gewichtsbasierten Berechnungen, Amoxicillin 50 mg/kg/Tag aufgeteilt in 3 Dosen.
Verhaltensmanagement ermöglicht die Behandlung bei jungen Patienten. Lokalanästhesie erfordert eine sorgfältige Technik, um intravaskuläre Injektionen bei kleinen Patienten zu vermeiden. Sedierung oder Vollnarkose kann für umfangreiche Eingriffe notwendig sein. Eltern spielen eine entscheidende Rolle in der Nachsorge, um die Medikamenteneinnahme und diätetische Änderungen sicherzustellen.
Geriatrische Patienten weisen unterschiedliche Komplexitäten auf. Polypharmazie erhöht die Risiken von Arzneimittelinteraktionen. Antibiotika können mit Warfarin interagieren (Clindamycin und Metronidazol verstärken die Wirkungen), Statinen oder Herzmedikamenten. Der Rückgang der Nierenfunktion erfordert Dosisanpassungen für renal ausgeschiedene Medikamente wie Amoxicillin und Metronidazol.
Kognitive Beeinträchtigungen erschweren die Symptomanzeige. Ältere Patienten mit Demenz können Schmerzen möglicherweise nicht effektiv kommunizieren. Pflegekräfte müssen Verhaltensänderungen, Nahrungsverweigerung, Berührungen im Gesicht oder Unruhe als Infektionsindikatoren beobachten. Die Behandlungsplanung priorisiert Einfachheit und Haltbarkeit über idealistische Ansätze.
Bevölkerung | Wichtige Überlegung | Antibiotika-Anpassung | Besondere Bedürfnisse |
Immungeschwächte | Hohes Verbreitungsrisiko | Breiteres Spektrum, früherer Beginn | Krankenhausüberweisungsschwelle gesenkt |
Pädiatrisch | Wachstum und Entwicklung | Gewichtsbasierte Dosierung | Verhaltensmanagement, Raumaufrechterhaltung |
Geriatrisch | Komorbiditäten, Polypharmazie | Renale Dosisanpassung | Überprüfung der Arzneimittelinteraktionen, kognitive Bewertung |
Wie können Menschen Zahninfektionen verhindern?
Tägliches Zähneputzen und Zahnseide, regelmäßige zahnärztliche Kontrollen alle 6 Monate, schnelle Behandlung von Karies und Management von Zahnfleischerkrankungen verhindern die Bedingungen, die zu Zahninfektionen führen.
Die Prävention von Zahninfektionen zielt auf die Ursachen ab: Karies und Parodontalerkrankungen. Mundhygienepraktiken stören die Bildung von bakteriellen Biofilmen, bevor sie Gewebeschäden verursachen. Die American Dental Association empfiehlt, zweimal täglich mit fluoridhaltiger Zahnpasta 2 Minuten lang zu putzen, wobei eine weiche Zahnbürste in sanften kreisenden Bewegungen am Zahnfleischrand verwendet wird.
Zahnseide erreicht Bereiche, die von Bürsten nicht erreicht werden, zwischen den Zähnen und unter den Zahnfleischrändern, wo parodontalpathogene Bakterien siedeln. Wasserzahnseide und Interdentalbürsten unterstützen Patienten mit eingeschränkter manueller Geschicklichkeit. Mundspülungen mit Chlorhexidin oder ätherischen Ölen reduzieren die bakterielle Last, ersetzen jedoch nicht die mechanische Reinigung.
Regelmäßige zahnärztliche Kontrollen ermöglichen eine frühzeitige Intervention. Professionelle Reinigungen entfernen Zahnstein (Tartar), der Bakterien beherbergt. Untersuchungen erkennen Karies, bevor sie die Pulpa erreichen. Bitewing-Röntgenaufnahmen identifizieren interproximale Karies, die bei visueller Inspektion unsichtbar ist. Das 6-monatige Recall-Intervall eignet sich für die meisten Patienten, obwohl Patienten mit hohem Kariesrisiko oder aktiven Parodontalerkrankungen möglicherweise 3-4 Monate Intervalle benötigen.
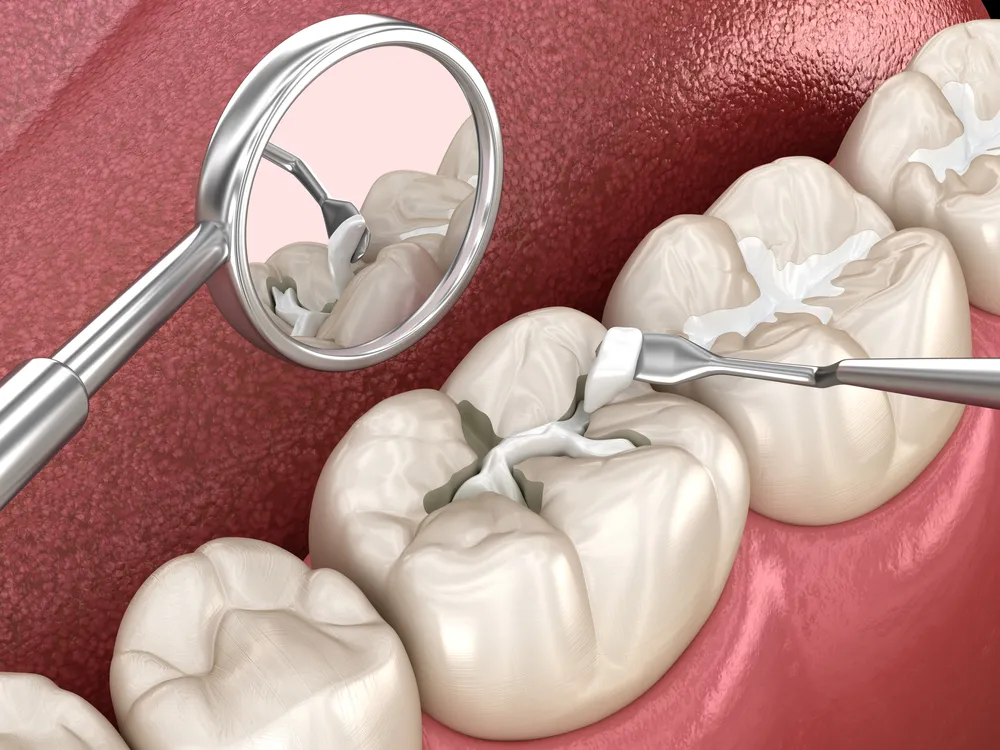
Eine frühzeitige Behandlung von Karies verhindert eine Pulpa-Infektion. Kleine Karies erfordern einfache Füllungen. Eine Verzögerung lässt die Karies tiefer werden, was schließlich eine Wurzelkanalbehandlung oder Extraktion erforderlich macht. Zahnversiegelungen auf den hinteren Zähnen schützen Kinder und Jugendliche vor Karies an den Kauflächen.
Das Management von Parodontalerkrankungen verhindert parodontalen Abszesse. Scaling und Wurzelglättung (tiefe Reinigung) entfernt Zahnstein von den Wurzeloberflächen. Parodontalpflege alle 3 Monate kontrolliert das Fortschreiten der Erkrankung. Chirurgische Taschenreduktion beseitigt tiefe Räume, in denen Abszesse entstehen.
Ernährungsmodifikationen unterstützen die Prävention. Die Begrenzung der Zuckeraussetzung, insbesondere häufiges Snacking und zuckerhaltige Getränke, reduziert die Säureproduktion von Streptococcus mutans. Das Kauen von zuckerfreiem Kaugummi regt den Speichelfluss an, der die Säure neutralisiert und den Zahnschmelz remineralisiert. Fluoridiertes Wasser stärkt die Zahnstruktur gegen Säureangriffe.
Was ist die erwartete Genesung nach der Behandlung von Zahninfektionen?
Schmerzen verbessern sich innerhalb von 24-48 Stunden nach der Kontrolle der Quelle. Weichgewebe heilt in 1-2 Wochen. Die Heilung des Knochens dauert 3-6 Monate. Eine frühzeitige Intervention führt zu einer schnelleren, vollständigeren Genesung.
Die erwarteten Heilungszeiträume variieren je nach Verfahren und Schwere der Infektion. Die Entwässerung eines akuten Abszesses führt zu sofortiger Schmerzlinderung. Schwellungen klingen innerhalb von 2-3 Tagen ab. Der kleine Schnitt heilt innerhalb einer Woche. Der zugrunde liegende Zahn benötigt jedoch weiterhin eine definitive Behandlung, um ein Wiederauftreten zu verhindern.
Die Genesung nach einer Wurzelkanaltherapie folgt einem vorhersehbaren Muster. Postoperative Schmerzen dauern 2-3 Tage an und sind mit NSAIDs behandelbar. Der periapikale Knochen beginnt innerhalb von Wochen zu heilen, obwohl eine vollständige radiografische Knochenauffüllung 6-12 Monate erfordert. Die endgültige Kronenplatzierung, 2-4 Wochen nach Abschluss des Wurzelkanals, stellt die Funktion wieder her und verhindert Brüche.
Extraktionsstellen heilen in Phasen. Die Blutgerinnselbildung erfolgt sofort. Das Weichgewebe schließt sich über 1-2 Wochen. Der Knochen füllt die Alveole über 3-6 Monate. Die Implantation, wenn geplant, erfolgt typischerweise 3-4 Monate nach der Extraktion, um die anfängliche Knochenheilung zu ermöglichen.
Frühe Intervention verbessert die Ergebnisse erheblich. Ein periapikales Abszess, der innerhalb von Tagen nach Beginn der Symptome behandelt wird, spricht auf eine einfache Wurzelkanaltherapie an. Eine Verzögerung von Wochen lässt die Knochenschädigung sich ausbreiten, was die Behandlung kompliziert und die Überlebenswahrscheinlichkeit des Zahns verringert. Periodontale Abszesse, die umgehend behandelt werden, erhalten die Zähne; eine verzögerte Behandlung führt oft zu einer hoffnungslosen Prognose, die eine Extraktion erfordert.
Faktoren, die die Ergebnisse beeinflussen, sind die Compliance des Patienten, der Immunstatus und die Nachverfolgung der definitiven Versorgung. Patienten, die die verordneten Antibiotikakuren abschließen und zu geplanten definitiven Eingriffen zurückkehren, erleben bessere Ergebnisse. Rauchen beeinträchtigt die Heilung, indem es den Blutfluss und die Immunfunktion verringert. Diabetes erfordert eine glykämische Kontrolle für eine optimale Genesung.
Welche Fortschritte prägen die zukünftige Behandlung von Zahninfektionen?
Neue antimikrobielle Peptide zielen auf Biofilme ab, ohne Resistenzen zu entwickeln. Laserassistierte Desinfektion verbessert die Sterilisation des Wurzelkanals. Personalisierte Medizin nutzt genetische Tests, um das Infektionsrisiko und die Behandlungsreaktion vorherzusagen.
Fortschritte in der antimikrobiellen Therapie gehen auf die Resistenz von Biofilmen ein. Traditionelle Antibiotika versagen gegen bakterielle Biofilme. Forscher entwickeln antimikrobielle Peptide, kurze Proteinfragmente, die bakterielle Membranen stören, ohne dass Resistenzen entstehen. Diese Peptide, die aus natürlichen Immunmolekülen stammen, zeigen vielversprechende Ergebnisse als Wurzelkanalspülungen und topische Behandlungen.
Die photodynamische Therapie verwendet lichtaktivierte Farbstoffe, um Bakterien abzutöten. Der Zahnarzt trägt ein photosensibilisierendes Mittel auf den infizierten Bereich auf und exponiert ihn dann bestimmten Lichtwellenlängen. Reaktive Sauerstoffspezies zerstören bakterielle Membranen und DNA. Diese Technik sterilisiert Wurzelkanalsysteme und parodontalen Taschen ohne Antibiotika.
Minimalinvasive Techniken erhalten die Zahnstruktur. Die GentleWave-Technologie nutzt multisonische Energie und fortschrittliche Fluiddynamik, um komplexe Wurzelkanalanatomien mit minimalem Instrumenteneinsatz zu desinfizieren. Die laserassistierte Wurzelkanalbehandlung verdampft infiziertes Gewebe und sterilisiert gleichzeitig die Kanalwände.
Personalisierte Zahnmedizin nutzt genetische und Mikrobiomanalysen. Genetische Tests identifizieren Patienten mit angeborenen Immunmängeln, die zu schweren Infektionen neigen. Die Profilierung des oralen Mikrobioms sagt das Risiko für Parodontalerkrankungen voraus und leitet gezielte probiotische Therapien. Pharmakogenomik bestimmt die optimale Antibiotikaauswahl basierend auf dem individuellen Stoffwechsel.
Regenerative Endodontie stellt einen Paradigmenwechsel dar. Anstatt das Zahnmark zu entfernen und die Kanäle mit inertem Material zu füllen, fördert dieser Ansatz die Regeneration von Zahnmarkgewebe unter Verwendung von Stammzellen und Wachstumsfaktoren. Unreife Zähne mit infiziertem Zahnmark können die Wurzelentwicklung fortsetzen und stärkere, langlebigere Zähne produzieren. Forschungen von Galler (2021) im Journal of Endodontics zeigen eine fortgesetzte Wurzelreifung bei 80 % der behandelten unreifen bleibenden Zähne.
Häufig gestellte Fragen zur Behandlung von Zahninfektionen
Benötigen alle Zahninfektionen Antibiotika?
Nein. Lokalisierte zahnärztliche Abszesse ohne Fieber oder Schwellungen im Gesicht benötigen nur eine Quellenkontrolle, Drainage, Wurzelkanalbehandlung oder Extraktion. Antibiotika helfen nur, wenn die Infektion systemisch verbreitet ist.
Das Missverständnis, dass jede Zahninfektion Antibiotika benötigt, führt zu einer Überverschreibung. Klinische Richtlinien der American Dental Association und des British National Institute for Health and Care Excellence besagen ausdrücklich, dass Antibiotika für die meisten lokalisierten Zahninfektionen unnötig sind. Quellenkontrollverfahren beseitigen die Infektion direkt. Die Hinzufügung von Antibiotika bietet keinen Nutzen und trägt zur Resistenz bei.
Antibiotika werden notwendig, wenn Patienten systemische Beteiligung zeigen. Fieber, Unwohlsein, Lymphadenopathie oder sich ausbreitende Cellulitis deuten auf eine bakterielle Belastung hin, die die lokale Eindämmung übersteigt. Immungeschwächte Patienten benötigen möglicherweise früher einen Antibiotikastart. Wenn Zahnärzte aufgrund von Zugangsproblemen beim Patienten keine sofortige Quellenkontrolle durchführen können, dienen Antibiotika als vorübergehende Überbrückung zur definitiven Behandlung.
Wie lange dauert die Behandlung von Zahninfektionen?
Die Drainage eines akuten Abszesses bietet sofortige Linderung. Die Wurzelkanaltherapie erfordert 1-3 Termine über 1-2 Wochen. Die Heilung nach einer Extraktion erfolgt in 1-2 Wochen. Antibiotikakuren dauern 5-7 Tage.
Die Behandlungsdauer hängt von der Schwere der Infektion und dem gewählten Ansatz ab. Die einfache Drainage eines Abszesses dauert 30 Minuten in der Zahnarztpraxis. Die Schmerzen verbessern sich innerhalb von Stunden. Der Patient muss jedoch innerhalb von Tagen zur definitiven Zahnbehandlung zurückkehren, um ein Wiederauftreten zu verhindern.
Die Wurzelkanaltherapie erstreckt sich typischerweise über zwei Termine. Der erste Besuch entfernt das infizierte Zahnmark und platziert antibakterielle Medikamente. Der zweite Besuch, 1-2 Wochen später, füllt und versiegelt die Kanäle. Ein dritter Termin platziert die permanente Krone 2-4 Wochen später. Gesamte Behandlungszeit: 4-8 Wochen für eine vollständige Wiederherstellung.
Die Extraktion bietet die schnellste definitive Lösung. Der Eingriff dauert 20-40 Minuten. Das Weichgewebe heilt in 1-2 Wochen. Wenn ein Implantataustausch geplant ist, verlängert sich der Zeitrahmen um 3-6 Monate für die Knochenheilung vor der Implantation.
Antibiotikakuren bleiben kurz. Fünf bis sieben Tage reichen für Zahninfektionen, im Gegensatz zu den verlängerten Kuren, die für tiefes Gewebe oder Knocheninfektionen benötigt werden. Patienten müssen die gesamte Kur abschließen, auch wenn sich die Symptome früher verbessern, um ein Wiederauftreten und Resistenzen zu verhindern.
Können Zahninfektionen von selbst heilen?
Nein. Zahninfektionen erfordern professionelle Intervention. Der Körper kann Infektionsquellen in Zähnen oder Abszesshöhlen nicht beseitigen. Eine verzögerte Behandlung erhöht das Risiko von Komplikationen.
Gelegentlich reißt ein Abszess spontan auf, entleert Eiter und lindert vorübergehend den Druck. Patienten können dies als "Heilung" interpretieren. Die Infektionsquelle, nekrotisches Gewebe, tiefer Karies oder parodontaler Taschen bleibt jedoch bestehen. Bakterien siedeln sich wieder an. Der Abszess tritt erneut auf, oft mit widerstandsfähigeren Organismen.
Die geschlossene Umgebung einer Zahnwurzel oder Abszesshöhle verhindert den Zugang des Immunsystems. Neutrophile und Antikörper können nekrotisches Gewebe oder dicken Eiter nicht effektiv durchdringen. Antibiotika, die im Blut zirkulieren, können die Bakterien in diesen avaskulären Räumen nicht erreichen. Nur mechanische Entfernung, Drainage, Wurzelkanalbehandlung oder Extraktion beseitigen die Infektion.
Selten bestehen chronische, niedriggradige Infektionen monatelang ohne akute Symptome. Diese "stillen" Infektionen zerstören dennoch Knochen und setzen entzündliche Mediatoren in den Blutkreislauf frei. Sie tragen zu systemischen Gesundheitsproblemen bei, ohne spürbare Schmerzen zu verursachen. Regelmäßige zahnärztliche Röntgenaufnahmen erkennen diese versteckten Infektionen.
Wann sollte jemand bei einer Zahninfektion Notfallversorgung suchen?
Suchen Sie Notfallversorgung bei Atem- oder Schluckbeschwerden, schnell anschwellendem Gesicht, Fieber über 39°C (102°F), Verwirrtheit oder Augenbeteiligung bei oberen Zahninfektionen.
Notfallwarnzeichen deuten auf eine lebensbedrohliche Verschlechterung hin. Eine Atemwegseinschränkung durch submandibuläre oder Mundboden-Schwellung erfordert eine sofortige Bewertung in der Notaufnahme. Patienten, die ihren eigenen Speichel nicht schlucken können, die lautes Atmen (Stridor) entwickeln oder das Gefühl haben, dass sich ihr Hals schließt, benötigen eine Notfall-Atemweg-Management.
Schnell fortschreitende Cellulitis, Schwellung, die sich über Stunden sichtbar ausdehnt, deutet auf einen aggressiven bakteriellen Stamm oder beeinträchtigte Immunität hin. IV-Antibiotika und möglicherweise chirurgische Drainage werden notwendig. Gesichtsschwellungen, die die Mittellinie überschreiten oder beide Seiten betreffen, deuten auf eine bilaterale Ausbreitung hin.
Systemische Toxizität signalisiert Sepsis. Hohe Fieber, schnelle Herzfrequenz (über 100 Schläge pro Minute), schnelles Atmen (über 20 Atemzüge pro Minute) und veränderter mentaler Zustand erfordern Notfallversorgung. Diese Patienten benötigen Blutkulturen, IV-Flüssigkeiten und Breitbandantibiotika in einer Intensivpflegeeinrichtung.
Augenbeteiligung bei oberen Zahninfektionen gefährdet das Sehvermögen. Schwellungen um das Auge, Doppelbilder oder die Unfähigkeit, das Auge zu bewegen, deuten auf eine orbitale Cellulitis hin. Diese Komplikation, die aus maxillären Zahninfektionen resultiert, die durch dünnes Knochengewebe in die Augenhöhle eindringen, erfordert eine Notfallkonsultation bei Augenheilkunde und HNO.
Symptom | Erforderliche Maßnahme | Zeitrahmen |
Zahnschmerzen mit leichter Schwellung | Zahnarzttermin | Innerhalb von 24-48 Stunden |
Gesichtsschwellung, Fieber | Dringende zahnärztliche oder medizinische Versorgung | Am selben Tag |
Atem- oder Schluckbeschwerden | Notaufnahme | Sofort |
Augenschwellung, Sehveränderungen | Notaufnahme | Sofort |
Verwirrtheit, hohes Fieber, schneller Herzschlag | Notaufnahme/911 | Sofort |
Fazit: Warum frühes Handeln Zähne und Leben rettet
Zahninfektionen erfordern eine schnelle Quellenkontrolle durch Drainage, Wurzelkanal oder Extraktion. Antibiotika spielen eine unterstützende Rolle bei der systemischen Ausbreitung. Prävention durch regelmäßige Pflege vermeidet die Schmerzen, Kosten und Gefahren fortgeschrittener Infektionen.
Die Behandlung von Zahninfektionen basiert auf klaren Prinzipien. Entfernen Sie die Infektionsquelle. Entleeren Sie Eiter und nekrotisches Gewebe. Erhalten Sie natürliche Zähne, wenn möglich. Extrahieren Sie, wenn nötig. Verwenden Sie Antibiotika mit Bedacht, nur bei systemischer Beteiligung oder wenn Verfahren verzögert werden müssen.
Die Beweise unterstützen diesen Ansatz überwältigend. Antibiotika allein versagen, weil sie die Bakterien in nekrotischen Pulpkammern und Abszesshöhlen nicht erreichen können. Biofilm-geschützte Organismen widerstehen dem Eindringen von Medikamenten. Nur die mechanische Entfernung von infiziertem Gewebe führt zur Heilung.
Eine frühe Diagnose verhindert Komplikationen. Eine kleine periapikale Läsion im Röntgenbild warnt vor einem bevorstehenden Abszess. Eine tiefe parodontalen Tasche signalisiert das Risiko eines Abszesses. Die Behandlung dieser Zustände, bevor akute Symptome auftreten, rettet Zähne, Geld und Gesundheit.
Ein ausgewogener Einsatz von Antibiotika schützt individuelle Patienten und die öffentliche Gesundheit. Jedes unnötige Rezept trägt zur Resistenz bei. Zahnärzte, die die Richtlinien zur verantwortungsvollen Verschreibung befolgen, verschreiben nur in indizierten Fällen, wählen Breitband-Antibiotika der ersten Wahl und begrenzen die Dauer, erhalten die Wirksamkeit von Antibiotika für zukünftige Generationen.
Die Integration von klinischer Behandlung und Prävention bietet die besten Ergebnisse. Patienten, die regelmäßige Zahnarztbesuche mit täglicher Mundpflege kombinieren, entwickeln selten Infektionen. Wenn Infektionen auftreten, suchen sie umgehend Hilfe, anstatt Schmerzen zu ertragen oder auf eine spontane Lösung zu hoffen.
Die Zukunft der Behandlung von Zahninfektionen sieht vielversprechend aus. Biofilm-zielgerichtete Therapien, regenerative Techniken und personalisierte Medizinansätze werden die Ergebnisse verbessern und gleichzeitig die Abhängigkeit von Antibiotika verringern. Das grundlegende Prinzip bleibt jedoch unverändert: Identifizieren Sie die Quelle, entfernen Sie die Infektion und stellen Sie die Gesundheit wieder her.
Referenzen
Cope, Anwen L., et al. "Antibiotikaeinsatz in der Zahnmedizin: Eine systematische Überprüfung." British Dental Journal, Bd. 216, Nr. 9, 2014, S. 523-30.
Galler, Kerstin M., et al. "Regenerative endodontische Verfahren zur Behandlung von Pulpanekrose bei unreifen bleibenden Zähnen: Eine systematische Überprüfung." Journal of Endodontics, Bd. 47, Nr. 8, 2021, S. 1193-202.
Lockhart, Peter B., et al. "Schlechte Mundgesundheit als chronische, potenziell infektiöse und entzündliche Erkrankung." Journal of Dental Research, Bd. 98, Nr. 10, 2019, S. 1073-80.
Matthews, David C., et al. "Antibiotika bei akuten Zahnabszessen: Eine systematische Überprüfung." Journal of Antimicrobial Chemotherapy, Bd. 71, Nr. 3, 2016, S. 564-71.
Moore, R. Andrew, et al. "Nicht-steroidale entzündungshemmende Medikamente bei akuten Zahnschmerzen." Cochrane Database of Systematic Reviews, Nr. 12, 2015, CD004978.
Ng, Yuan-Ling, et al. "Ergebnis der primären Wurzelkanalbehandlung: Systematische Überprüfung der Literatur." International Endodontic Journal, Bd. 44, Nr. 7, 2011, S. 597-612.
Patel, Shanon, et al. "Cone Beam Computed Tomography in Endodontics." International Endodontic Journal, vol. 52, no. 9, 2019, pp. 1248-64.
Petersen, Poul Erik. "Weltgesundheitsorganisation Globale Politik zur Verbesserung der Mundgesundheit." International Dental Journal, vol. 72, no. 4, 2022, pp. 302-07.
Seneviratne, Chaminda J., et al. "Zahnplaque-Biofilm: Ein archetypischer Biofilm." Periodontology 2000, vol. 75, no. 1, 2017, pp. 34-44.