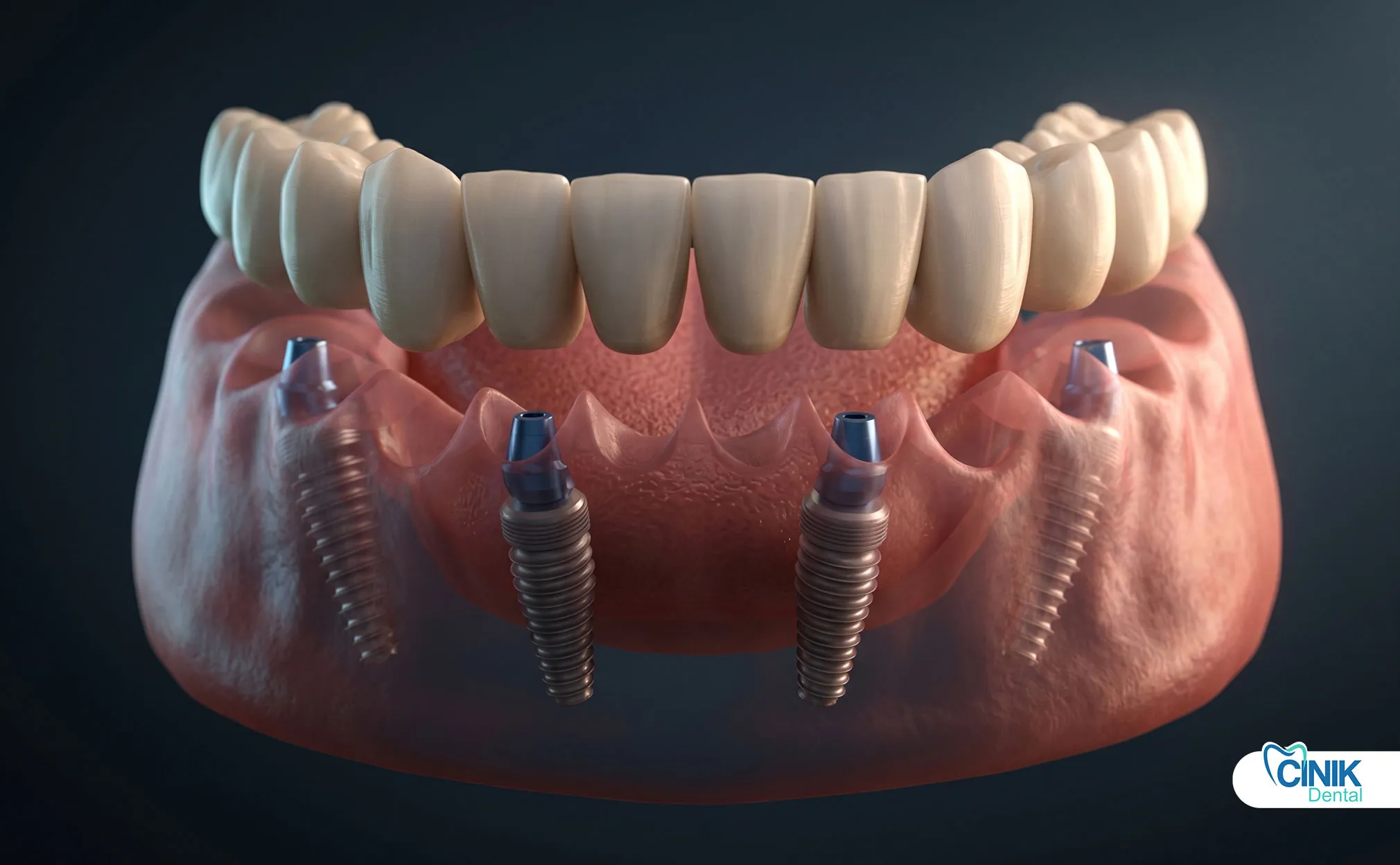
L'élimination du nerf dentaire représente une procédure endodontique spécialisée qui élimine le tissu pulpaire infecté ou endommagé de l'intérieur de la dent. Les dentistes appellent ce processus le traitement de canal radiculaire. La procédure sauve des millions de dents naturelles chaque année en éliminant la source de l'infection tout en préservant la structure externe de la dent.
La dentisterie moderne repose fortement sur cette intervention. La thérapie endodontique est l'une des procédures dentaires les plus courantes dans le monde. Des données épidémiologiques récentes montrent que les praticiens dentaires effectuent des millions de ces traitements chaque année dans les pays développés. La prévalence reflète à la fois la forte incidence des caries dentaires et les taux de réussite qui rendent cette approche préférable à l'extraction pour de nombreux patients.
Le but principal de cet article relie la science clinique à la compréhension pratique des patients. Les lecteurs apprendront les mécanismes biologiques derrière la maladie pulpaire. Ils comprendront pourquoi les dentistes recommandent l'élimination du nerf dans des scénarios cliniques spécifiques. Plus important encore, ils découvriront comment les technologies modernes ont transformé cette procédure d'une intervention redoutée en une option de traitement prévisible et confortable.
La procédure d'élimination du nerf dentaire traite des conditions pathologiques au sein de la chambre pulpaire. Ces conditions incluent la pulpite irréversible, le tissu pulpaire nécrotique et les infections périapicales. Si elles ne sont pas traitées, ces conditions entraînent la formation d'abcès, la perte osseuse et la perte éventuelle de la dent. Une intervention précoce prévient ces complications et maintient la dentition naturelle du patient.
Quelle anatomie compose le nerf dentaire et le complexe pulpaire ?
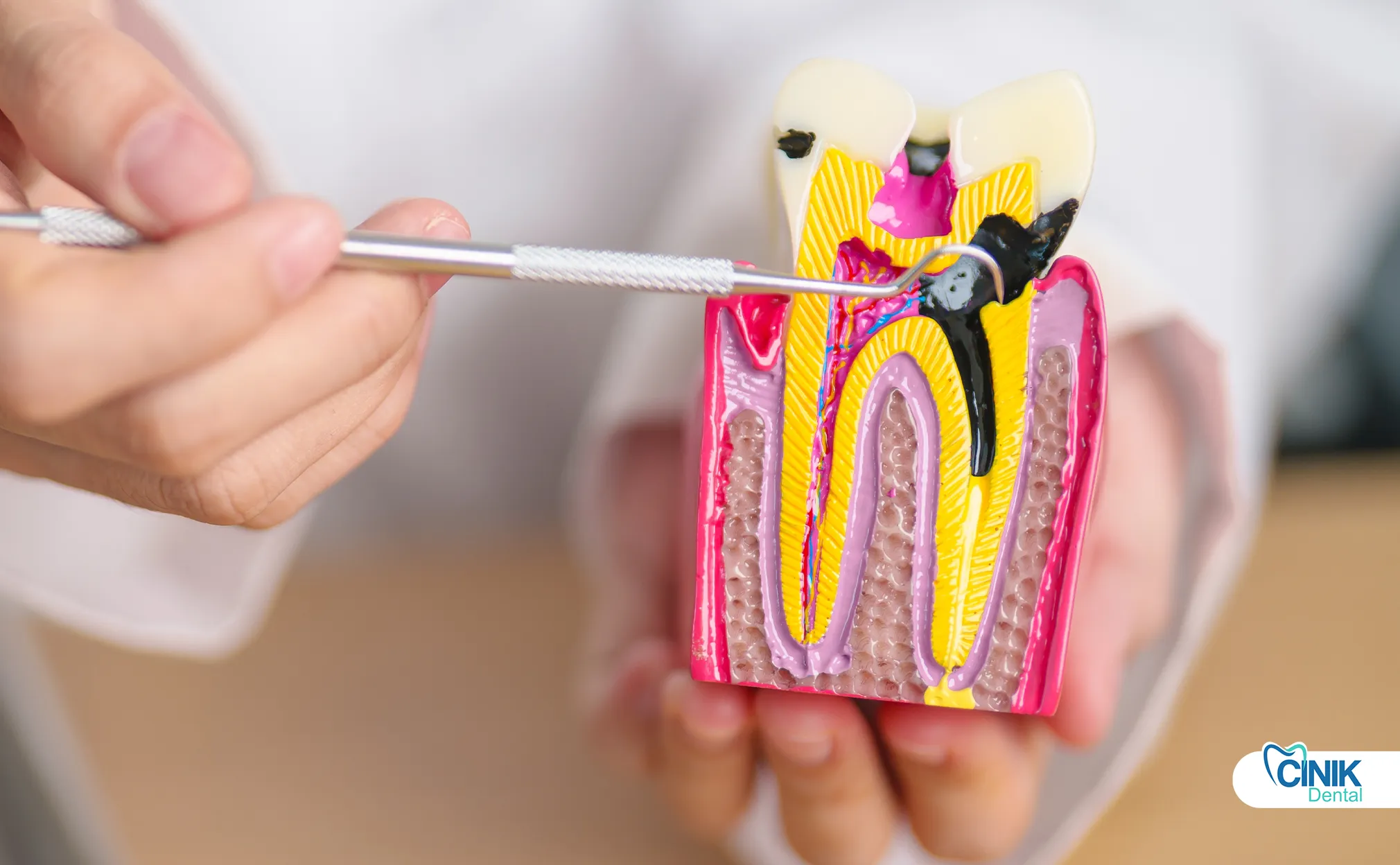
Le complexe nerveux dentaire se compose de l'émail, de la dentine, de la chambre pulpaire et des canaux radiculaires. La pulpe contient des nerfs, des vaisseaux sanguins et du tissu conjonctif qui fournissent une fonction sensorielle et un soutien au développement pendant la formation de la dent.
Comprendre l'anatomie dentaire aide les patients à saisir pourquoi l'élimination du nerf devient nécessaire. La dent se compose de plusieurs couches distinctes, chacune ayant des fonctions biologiques spécifiques.
La couche la plus externe, l'émail, est composée de la substance la plus dure du corps humain. Cette structure cristalline protège la dent des dommages mécaniques et de l'érosion chimique. Sous l'émail se trouve la dentine, un tissu calcifié contenant des tubules microscopiques. Ces tubules canalisent les signaux sensoriels de l'environnement externe vers la chambre pulpaire centrale.
La chambre pulpaire abrite la pulpe dentaire, un tissu conjonctif mou contenant le faisceau neurovasculaire. Selon Niki et al. (2025), la pulpe contient deux types de nerfs principaux qui innervent le tissu dentaire : des fibres autonomes et des fibres sensorielles afférentes. Les fibres autonomes sympathiques proviennent du ganglion cervical supérieur et régulent le flux sanguin à travers le muscle lisse arteriolaire. Les fibres sensorielles afférentes proviennent des branches maxillaires et mandibulaires du nerf trijumeau. Ces fibres sensorielles transmettent des signaux de douleur, de température et de pression au cerveau.
La pulpe dentaire contient des odontoblastes, des cellules spécialisées qui produisent de la dentine tout au long de la vie de la dent. Ces cellules tapissent la chambre pulpaire et étendent des processus dans les tubules dentinaires. Les vaisseaux sanguins à l'intérieur de la pulpe fournissent des nutriments et de l'oxygène. Les vaisseaux lymphatiques drainent les produits de déchets et soutiennent la surveillance immunitaire.
Pendant le développement dentaire, la pulpe joue un rôle critique. Elle stimule la formation des racines et l'éruption des dents. Cependant, une fois que la dent est mature, l'importance fonctionnelle de la pulpe diminue. Une dent entièrement développée peut survivre sans la pulpe car le ligament parodontal et les tissus environnants fournissent un soutien suffisant. Cette réalité biologique permet aux dentistes d'enlever la pulpe malade sans compromettre la viabilité à long terme de la dent.
L'âge modifie considérablement la pulpe. Des recherches de Carvalho et Lussi (2017) montrent que la densité cellulaire diminue d'environ 50 % entre 20 et 70 ans. La pulpe subit une fibrose et accumule des fibres de collagène à mesure que les patients vieillissent. Les vaisseaux sanguins et les nerfs dégénèrent progressivement. Ces changements expliquent pourquoi les patients plus âgés ressentent parfois moins de douleur en raison de caries profondes malgré une implication pulpaire étendue.
Qu'est-ce qui cause des dommages aux nerfs dentaires et des infections ?
Les caries dentaires profondes, les fractures dentaires, les procédures dentaires répétées et les restaurations défectueuses causent des dommages à la pulpe. Les bactéries envahissent la chambre pulpaire, forment des biofilms et déclenchent une inflammation qui conduit à une pulpite irréversible ou à une nécrose.
De multiples facteurs étiologiques contribuent à la pathologie pulpaire. Comprendre ces facteurs aide les patients à prévenir des conditions nécessitant l'élimination des nerfs.
Les caries dentaires profondes représentent la cause la plus courante de maladie pulpaire. Lorsque les caries pénètrent à travers l'émail et la dentine, elles atteignent la chambre pulpaire. Les bactéries colonisent le tissu et déclenchent des réponses inflammatoires. Le corps tente de lutter contre l'infection en envoyant des cellules immunitaires dans la zone. Ce processus inflammatoire augmente la pression à l'intérieur de la chambre pulpaire rigide, comprimant les nerfs et causant de la douleur.
Les fractures dentaires et les traumatismes offrent une autre voie pour l'invasion bactérienne. Les fissures permettent aux fluides buccaux et aux micro-organismes d'entrer directement dans la chambre pulpaire. Même les fractures microscopiques invisibles à l'œil nu peuvent abriter des bactéries. Les procédures dentaires répétées stressent également la pulpe. Chaque épisode de forage enlève de la structure dentaire et génère de la chaleur, ce qui peut irriter le tissu pulpaire.
Les restaurations défectueuses créent des micro-espaces à l'interface dent-restauration. Ces espaces accumulent la plaque et permettent les fuites bactériennes. Au fil du temps, cette carie secondaire atteint la pulpe et provoque une infection.
Une fois que les bactéries pénètrent dans la pulpe, elles forment des communautés complexes appelées biofilms. Selon la revue du NIH sur les biofilms endodontiques (2023), la formation de biofilm implique quatre étapes principales : formation d'un film de conditionnement, adhésion et colonisation bactérienne, croissance et expansion, et enfin détachement. Ces biofilms résistent à la fois aux défenses de l'hôte et aux traitements antimicrobiens.
La maladie progresse à travers des étapes distinctes. L'invasion bactérienne initiale provoque une pulpite réversible. À ce stade, le retrait de l'irritant permet à la pulpe de guérir. Cependant, une infection persistante conduit à une pulpite irréversible. Le tissu pulpaire se décompose, et l'inflammation se propage aux tissus périapicaux. Finalement, la pulpe nécrose complètement. Les bactéries sortent alors de l'apex radiculaire et infectent l'os environnant, formant des lésions périapicales ou des abcès.
Enterococcus faecalis joue un rôle particulièrement problématique dans les infections persistantes. Ce bacille gram positif survit à des conditions difficiles et résiste à l'hydroxyde de calcium, un médicament intracanal courant. Svensäter et Bergenholtz (2004) ont identifié cet organisme comme une cause majeure d'échec du traitement car il pénètre dans les tubules dentinaires et maintient des communautés de biofilms qui échappent à une élimination complète.
Quels symptômes indiquent que vous avez besoin d'une extraction du nerf dentaire ?
Une douleur dentaire sévère et persistante, une sensibilité aux stimuli chauds et froids, un gonflement, la formation de fistules et des preuves radiographiques d'infection indiquent la nécessité d'une intervention endodontique. Les dentistes confirment les diagnostics par des tests thermiques et des tests électriques de la pulpe.
Les patients doivent reconnaître des signes d'alerte spécifiques qui signalent une maladie pulpaire. Ces symptômes guident les décisions de traitement et le moment de l'intervention.
Une douleur dentaire sévère et persistante constitue l'indicateur le plus évident. Cette douleur est souvent pulsatile et s'aggrave lorsque les patients s'allongent. Elle peut réveiller les patients pendant leur sommeil. La douleur se localise généralement à une dent spécifique, bien qu'elle puisse irradier vers des zones adjacentes. Une douleur spontanée sans stimulus suggère fortement une pulpite irréversible.
La sensibilité à la température fournit un autre indice critique. Les patients atteints de maladie pulpaire ressentent souvent une douleur aiguë et persistante lors de la consommation de boissons chaudes ou froides. La douleur persiste pendant des minutes après le retrait du stimulus thermique. Cette réponse persistante diffère de la sensibilité dentaire normale, qui se résout immédiatement après le retrait du stimulus.
Le gonflement autour de la dent affectée indique une infection avancée. Le gonflement peut se localiser au tissu gingival ou se propager au visage et au cou. Certains patients développent une fistule, une petite ouverture de drainage ressemblant à un bouton sur le tissu gingival. Cette fistule représente la tentative du corps de drainer le liquide de l'abcès. Les patients peuvent goûter un écoulement malodorant provenant de ces ouvertures.
L'imagerie radiographique révèle une perte osseuse autour de l'apex radiculaire. Les dentistes prennent des radiographies périapicales ou des scans de tomographie à faisceau conique (CBCT) pour visualiser ces lésions. Les zones sombres autour des pointes radiculaires indiquent une radiolucidité périapicale, signalant une destruction osseuse due à l'infection.
Les dentistes emploient des tests diagnostiques spécifiques pour confirmer l'état de la pulpe. Les tests thermiques appliquent du froid ou de la chaleur à la surface de la dent. Les dents saines réagissent brièvement ; les dents malades réagissent intensément et pendant des périodes prolongées. Le test électrique de la pulpe délivre un léger stimulus électrique pour évaluer la viabilité du nerf. Une lecture non réactive suggère une pulpe nécrotique.
Le test de percussion tapote doucement la dent pour vérifier l'inflammation périapicale. La douleur à la percussion indique que l'inflammation s'est propagée au-delà de la pulpe vers le ligament parodontal entourant l'apex radiculaire.
Comment les dentistes effectuent-ils la procédure d'élimination du nerf dentaire étape par étape ?
Les dentistes suivent un protocole systématique : diagnostic et planification, anesthésie et isolation, préparation de la cavité d'accès, élimination de la pulpe, nettoyage et mise en forme, remplissage du canal et restauration finale. Les techniques modernes garantissent le confort du patient tout au long de la procédure de 60 à 90 minutes.
Le traitement de canal suit une séquence précise conçue pour éliminer l'infection et sceller le système canalaire. Comprendre ces étapes réduit l'anxiété du patient et améliore la coopération.
Comment fonctionne la phase de diagnostic et de planification du traitement ?
Les cliniciens examinent la dent cliniquement et radiographiquement. Ils prennent des radiographies ou des scans CBCT pour visualiser l'anatomie du canal et l'état périapical. Ils formulent un plan de traitement basé sur ces résultats.
Le dentiste commence par un examen clinique complet. Il évalue l'état de la dent, vérifie la mobilité et évalue les tissus mous environnants. Il passe en revue les antécédents médicaux du patient pour identifier les contre-indications ou les considérations spéciales.
L'imagerie radiographique fournit des informations diagnostiques essentielles. Les radiographies périapicales standard montrent la longueur de la racine, la courbure et le nombre de canaux. Les cas complexes peuvent nécessiter une imagerie CBCT. Cette vue tridimensionnelle révèle la ramification des canaux, les calcifications et les lésions périapicales que les radiographies bidimensionnelles manquent.
Comment l'anesthésie et l'isolation garantissent-elles le confort du patient ?
L'anesthésique local élimine la sensation de douleur. Le digue en caoutchouc isole la dent de la salive et empêche la contamination bactérienne pendant la procédure.
Les dentistes administrent une anesthésie locale pour bloquer la conduction nerveuse. Ils utilisent généralement de la lidocaïne ou de l'articaïne avec de l'épinéphrine pour prolonger l'effet anesthésique. Les patients restent éveillés mais ne ressentent aucune douleur dans la zone traitée.
La digue en caoutchouc fournit une isolation critique. Cette fine feuille de latex ou de matériau non latex couvre la bouche sauf pour un petit trou exposant la dent traitée. La digue empêche la salive d'entrer dans l'espace canalaire. Elle protège également le patient d'avaler des instruments ou des solutions d'irrigation.
Comment les cliniciens accèdent-ils et retirent-ils la pulpe ?
Le dentiste perce une cavité d'accès à travers la couronne pour atteindre la chambre pulpaire. Il utilise ensuite des instruments spécialisés pour retirer tout le tissu pulpaire de la chambre et des canaux radiculaires.
La préparation de la cavité d'accès nécessite de la précision. Le dentiste retire le toit de la chambre pulpaire tout en préservant la structure dentaire. Il utilise une fraise à grande vitesse pour créer une ouverture qui permet un accès en ligne droite aux orifices canalaire.
Le retrait de la pulpe suit immédiatement. Le dentiste insère des broches ou des fichiers barbelés dans les canaux. Il retire ces instruments pour extraire le tissu pulpaire. Les instruments rotatifs avec des fichiers en nickel-titane dominent désormais la pratique moderne. Ces instruments flexibles naviguent plus en toute sécurité dans les canaux courbés que les fichiers en acier inoxydable traditionnels.
Comment la phase de nettoyage et de mise en forme élimine-t-elle l'infection ?
L'instrumentation mécanique combinée à l'irrigation chimique élimine les biofilms bactériens et les débris. L'hypochlorite de sodium dissout les tissus organiques et tue les microorganismes.
La phase de nettoyage et de mise en forme constitue l'étape la plus critique. Le dentiste utilise des fichiers de plus en plus grands pour agrandir et façonner les canaux. Cette action mécanique élimine la dentine infectée et crée de l'espace pour les solutions d'irrigation.
L'irrigation chimique suit chaque séquence de fraisage. La solution d'hypochlorite de sodium sert d'irrigant principal. Cette solution alcaline dissout les résidus pulpaire et détruit les parois cellulaires bactériennes. Les dentistes utilisent des concentrations de 2-3 % pour les traitements primaires. Ils administrent la solution à l'aide de seringues avec des aiguilles à évent latéral pour éviter de forcer le liquide à travers l'apex.
L'EDTA (acide éthylènediaminetétraacétique) fournit une irrigation adjuvante. Cet agent chélatant élimine la couche de débris inorganique que créent les fichiers. L'élimination de cette couche expose les tubules dentinaires et améliore la désinfection des canaux.
Les techniques modernes incluent l'irrigation ultrasonique et les systèmes à pression négative. Ces méthodes améliorent la pénétration de l'irrigant dans les branches canalaire et les tubules dentinaires où se cachent les bactéries.
Comment les dentistes remplissent-ils et scellent-ils les canaux ?
Les dentistes remplissent les canaux nettoyés avec de la gutta-percha et un scellant. Cette obturation empêche la réintroduction bactérienne et scelle l'apex contre les fluides périapicaux.
Le remplissage du canal se produit après un séchage approfondi. Le dentiste sélectionne des points de gutta-percha qui correspondent à la taille du fichier final. La gutta-percha, un caoutchouc naturel provenant des arbres, fournit un matériau de remplissage inerte et biocompatible.
Les scellants recouvrent les parois du canal avant l'insertion de la gutta-percha. Ces ciments créent un effet monobloc, liant le remplissage à la dentine. Les scellants biocéramiques ont largement remplacé les scellants traditionnels à base de résine ou d'oxyde de zinc-eugénol. Ces matériaux à base de silicate de calcium scellent mieux et provoquent moins d'inflammation.
Le dentiste compacte la gutta-percha en utilisant des techniques de condensation verticale chaude ou de compactage latéral. Ils retirent l'excès de matériau de la chambre et placent un scellé coronal temporaire ou permanent.
Comment la restauration finale complète-t-elle le traitement ?
Le dentiste place un remplissage permanent ou une couronne pour restaurer la fonction et prévenir les fractures. Les dents postérieures nécessitent des couronnes pour se protéger contre les défaillances structurelles.
La restauration finale dépend de l'état et de l'emplacement de la dent. Les dents antérieures avec une perte de structure minimale peuvent recevoir des remplissages composites. Les dents postérieures subissant un traitement de canal nécessitent des couronnes à couverture totale. Ces couronnes répartissent les forces de mastication et préviennent les fractures verticales.
Quels matériaux et technologies les endodontistes utilisent-ils aujourd'hui ?
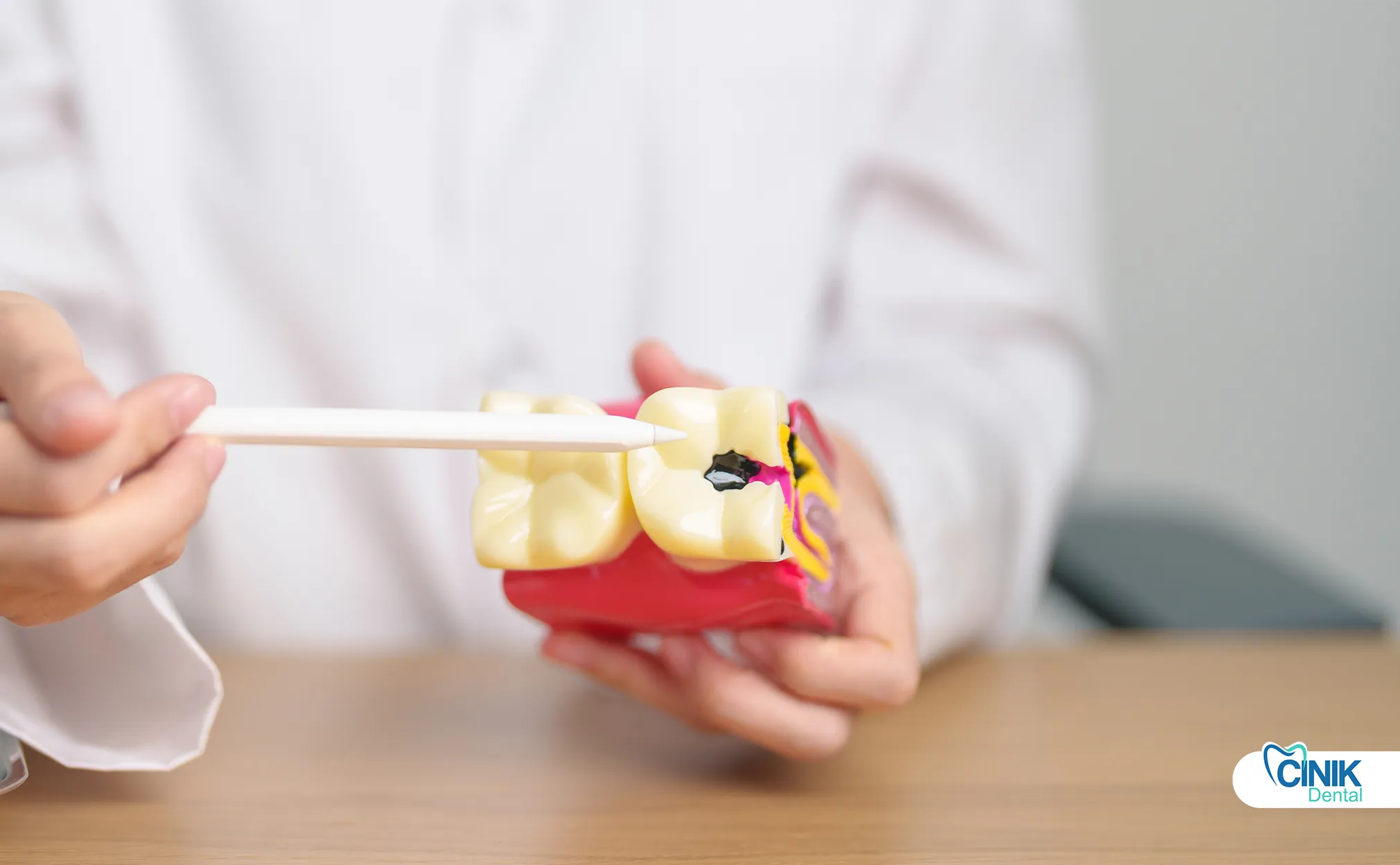
L'endodontie moderne utilise des instruments rotatifs en nickel-titane, des localisateurs d'apex électroniques, des microscopes opératoires dentaires, des scellants biocéramiques et de l'imagerie 3D. Les technologies émergentes incluent la désinfection assistée par laser et les approches régénératives.
La technologie endodontique a considérablement progressé au cours des deux dernières décennies. Ces innovations améliorent les taux de réussite, réduisent le temps de traitement et augmentent le confort des patients.
Quels matériaux traditionnels restent essentiels ?
La gutta-percha reste le principal matériau de remplissage. Divers scellants assurent des scellés apicaux et coronaux. Les fichiers en acier inoxydable servent encore à des fins spécifiques malgré les alternatives plus récentes.
La gutta-percha a rempli les canaux radiculaires pendant plus d'un siècle. Ce matériau thermoplastique s'adapte bien aux irrégularités du canal lorsqu'il est chauffé. Il reste stable pendant des décennies sans se dégrader ni provoquer d'inflammation.
Les scellants à base d'oxyde de zinc-eugénol ont fourni la norme pendant des générations. Ces matériaux offrent des propriétés antimicrobiennes et une manipulation facile. Cependant, ils se dissolvent lentement au fil du temps et peuvent permettre des fuites. Les scellants en résine modernes et les scellants biocéramiques offrent une capacité de scellement supérieure et une stabilité dimensionnelle.
Quelles avancées modernes améliorent les résultats des traitements ?
Les instruments rotatifs en nickel-titane naviguent en toute sécurité dans les canaux courbés. Les localisateurs d'apex électroniques déterminent la longueur de travail avec précision. Les microscopes dentaires améliorent la visibilité. L'imagerie CBCT révèle une anatomie complexe.
Les instruments rotatifs en nickel-titane (NiTi) ont révolutionné le façonnage des canaux. Ces fichiers superélastiques se plient autour des courbes qui feraient redresser ou perforer les fichiers en acier inoxydable. Ils coupent efficacement et maintiennent la courbure originale du canal.
Les localisateurs d'apex électroniques (EAL) déterminent la longueur de travail du canal électroniquement. Ces dispositifs mesurent la résistance électrique entre un fichier dans le canal et la muqueuse buccale. Ils signalent lorsque le fichier atteint la constriction apicale, améliorant la précision de la longueur par rapport aux radiographies seules.
Les microscopes opératoires dentaires offrent un grossissement de 6 à 25x. Les endodontistes utilisent ces microscopes pour localiser les entrées de canal calcifiées, identifier les canaux manqués et effectuer des retraites. Une visibilité améliorée réduit les erreurs procédurales et améliore les résultats.
La tomographie par ordinateur à faisceau conique (CBCT) représente la norme d'imagerie pour les cas complexes. Cette imagerie tridimensionnelle révèle les isthmes canaux, les bifidités apicales et les lésions périapicales avec une résolution de 0,1 mm. Les dentistes utilisent le CBCT pour la planification préopératoire dans les cas difficiles.
Quelles technologies émergentes montrent des promesses ?
La désinfection assistée par laser, l'impression biographique 3D de tissu pulpaire, la thérapie par cellules souches et les procédures guidées par intelligence artificielle représentent l'avant-garde de la recherche endodontique.
Les lasers assistent désormais à la désinfection des canaux. Les lasers Er,Cr:YSGG et à diode activent les solutions d'irrigation et vaporisent les débris dans les branches du canal. Ils réduisent les comptes bactériens au-delà de ce que l'instrumentation mécanique atteint seule.
L'endodontie régénérative offre une alternative biologique au traitement traditionnel. Les chercheurs ont exploré la transplantation de cellules souches depuis que Gronthos et al. (2000) ont d'abord isolé des cellules souches de pulpe dentaire. Nakashima et al. (2017) ont démontré la régénération réussie de la pulpe en utilisant des cellules souches de pulpe dentaire autologues dans un essai clinique pilote. Les patients ont retrouvé la sensibilité de la pulpe, et l'imagerie a montré la formation de tissu semblable à de la dentine.
Les approches d'impression biographique tridimensionnelle visent à fabriquer du tissu pulpaire pour la transplantation. Les chercheurs impriment des échafaudages en utilisant de l'hydroxyapatite et du méthacryloyl de gélatine (GelMA) chargés de cellules souches de pulpe dentaire. Ces constructions soutiennent la vascularisation et l'innervation lorsqu'elles sont implantées dans les canaux radiculaires.
L'intelligence artificielle assiste désormais dans le diagnostic et la planification du traitement. Les algorithmes d'apprentissage automatique analysent les radiographies pour détecter les lésions périapicales et prédire les résultats du traitement. Les applications futures pourraient inclure le façonnage de canaux assisté par robot et la surveillance en temps réel de la localisation de l'apex.
Quelles taux de succès les patients peuvent-ils attendre d'un traitement de canal radiculaire ?
Des études à long terme montrent 97 % de survie à 10 ans, 81 % à 20 ans et 68 % à 37 ans. Les taux de succès endodontiques varient de 89 à 93 % selon les conditions préopératoires et les soins de suivi.
La mesure du succès en endodontie inclut deux métriques : la survie de la dent (restant dans la bouche) et le succès endodontique (absence de symptômes et guérison radiographique). Les deux sont importants pour les patients, bien qu'ils diffèrent cliniquement.
Que révèlent les études de survie à long terme ?
Des traitements de canal radiculaire bien réalisés entraînent la rétention des dents pendant des décennies. Les principales causes d'échec tardif sont la maladie parodontal et la fracture structurelle plutôt que des facteurs endodontiques.
López-Valverde et al. (2023) ont publié des données marquantes suivant des patients pendant 5 à 37 ans. Leur étude de 598 dents traitées endodontiquement a démontré des taux de survie cumulés de 97 % à 10 ans, 81 % à 20 ans, 76 % à 30 ans et 68 % à 37 ans. Ces statistiques confirment que le traitement de canal radiculaire fournit des résultats durables.
L'étude a identifié des facteurs pronostiques spécifiques. Les dents sans radiolucidité périapicale préopératoire ont survécu plus longtemps. Les dents restaurées avec des couronnes ont montré une meilleure survie que celles avec de grandes obturations. Les patients sans poches parodontales profondes ont maintenu leurs dents traitées plus longtemps.
Comment les traitements de canal radiculaire se comparent-ils aux implants ?
Les dents traitées endodontiquement et les implants unitaires montrent des taux de survie comparables sur 5 à 10 ans. La préservation des dents naturelles offre souvent de meilleurs résultats fonctionnels et esthétiques.
Les revues systématiques comparant ces options montrent des pourcentages de succès similaires. À 5 ans, les deux traitements atteignent environ 95 % de survie. Cependant, les différences biologiques et économiques sont importantes.
Les dents naturelles maintiennent les ligaments parodontaux. Ces ligaments fournissent la proprioception, la capacité de sentir la pression de morsure. Les implants manquent de ce mécanisme de rétroaction, ce qui peut entraîner une surcharge. Les dents naturelles préservent également l'os alvéolaire grâce à une charge fonctionnelle. Les implants peuvent provoquer une résorption osseuse crête au fil du temps.
D'un point de vue économique, la préservation des dents naturelles coûte moins cher que l'extraction et la pose d'implants. La thérapie par implant nécessite des interventions chirurgicales, des périodes de guérison et des complications potentielles comme la péri-implantite.
Quels mécanismes biologiques permettent la guérison ?
Le système immunitaire élimine les bactéries résiduelles des tissus périapicaux. L'os se régénère une fois la source de l'infection éliminée. Le ligament parodontal se rattache à la surface de la racine.
La guérison périapicale commence immédiatement après la désinfection du canal. Les macrophages et les ostéoclastes éliminent le tissu inflammatoire et l'os nécrotique. Les ostéoblastes déposent ensuite une nouvelle matrice osseuse. La guérison radiographique peut prendre 6 à 12 mois pour apparaître complètement.
Le remplissage du canal radiculaire empêche la recontamination bactérienne. La restauration coronaire scelle le système canalaire des fluides buccaux. Ensemble, ces scellants permettent aux tissus périapicaux de se régénérer et de maintenir leur santé indéfiniment.
Quels soins post-traitement garantissent un succès à long terme ?
Les patients doivent gérer la sensibilité à court terme, maintenir une excellente hygiène buccale, assister aux visites de suivi et obtenir des couronnes permanentes sur les dents postérieures dans les semaines suivant le traitement.
Les soins post-traitement ont un impact significatif sur les résultats à long terme. Les patients doivent comprendre les exigences immédiates et à long terme.
Quels symptômes à court terme les patients doivent-ils attendre ?
Une légère sensibilité à la mastication et aux changements de température dure de 3 à 7 jours. Les médicaments anti-inflammatoires gèrent efficacement l'inconfort. Une douleur ou un gonflement sévère nécessite un contact dentaire immédiat.
Après la disparition de l'anesthésie, les patients peuvent ressentir un léger inconfort. Cette sensibilité résulte de l'instrumentation près de l'apex de la racine et d'une inflammation temporaire dans le ligament parodontal. L'ibuprofène ou l'acétaminophène en vente libre résout généralement cet inconfort.
Les patients doivent éviter de mâcher du côté traité jusqu'à ce que la restauration permanente soit placée. Le remplissage ou la couronne temporaire peut se fracturer sous des forces importantes. Les aliments durs risquent de fracturer la dent avant la mise en place de la restauration complète.
Quels protocoles de soins à long terme maintiennent les résultats ?
Le brossage et le fil dentaire quotidiens préviennent les fuites coronales. Les protège-dents nocturnes protègent contre les forces de broyage. Les radiographies annuelles surveillent la santé périapicale. Le remplacement rapide des restaurations prévient la réintroduction bactérienne.
L'hygiène buccale est cruciale pour les dents traitées endodontiquement. Bien que le canal radiculaire élimine l'infection interne, une nouvelle carie au niveau de la marge de restauration peut entraîner un échec. Les patients doivent se brosser les dents deux fois par jour et passer le fil dentaire autour de toutes les dents restaurées.
Le bruxisme (grincement des dents) met en danger les dents traitées. La nature fragile des dents traitées endodontiquement les rend susceptibles aux fractures verticales sous des forces importantes. Les protège-dents nocturnes répartissent ces forces et protègent l'investissement.
Les radiographies de suivi à 6-12 mois après le traitement confirment la guérison périapicale. Les dentistes comparent ces images aux films préopératoires pour évaluer la régénération osseuse. La surveillance annuelle par la suite permet de détecter précocement les échecs potentiels.
Quelles complications peuvent survenir pendant ou après le traitement ?
Le nettoyage incomplet des canaux, les branches de canaux manquées, les fuites coronales et les fractures radiculaires verticales causent la plupart des échecs. Le retraitement ou la chirurgie apicale traite les infections persistantes.
Malgré des taux de succès élevés, des complications surviennent. Comprendre ces risques aide les patients à prendre des décisions éclairées et à rechercher une intervention rapide.
Quelles erreurs procédurales mènent à l'échec ?
L'anatomie complexe des canaux radiculaires peut abriter une infection non traitée. Les dentistes peuvent manquer des canaux étroits ou calcifiés. La séparation des instruments peut bloquer l'accès au canal. Les perforations peuvent créer de nouveaux chemins pour les bactéries.
Les systèmes de canaux radiculaires contiennent souvent plus de complexité que ne le suggèrent les manuels d'anatomie standard. Les isthmes relient des canaux adjacents. Les canaux accessoires se ramifient à angle droit. Les canaux en forme de C dans les deuxièmes molaires mandibulaires défient l'instrumentation conventionnelle.
Les canaux manqués restent la cause la plus courante d'infection persistante. Les molaires supérieures ont généralement trois ou quatre canaux ; manquer le deuxième canal méso-buccal (MB2) invite à l'échec. Les dents antérieures inférieures peuvent avoir deux canaux qui apparaissent comme un seul sur les radiographies.
La séparation des instruments se produit lorsque les fichiers se fatiguent dans des canaux courbés. Les fichiers en acier inoxydable se séparaient plus fréquemment que les instruments modernes en NiTi, mais la séparation se produit toujours. Les instruments séparés bloquent l'accès au canal et peuvent abriter des bactéries.
Quels facteurs post-traitement causent l'échec ?
De mauvais scellants coronaux permettent la réintroduction bactérienne. Le placement retardé de la restauration permanente risque de fracture. Les caries secondaires envahissent par des espaces marginaux.
La qualité de la restauration finale prédit mieux la survie à long terme que la technique endodontique. Des études de Gillen et al. (2011) démontrent que des restaurations inadéquates causent plus d'échecs que la recontamination des canaux. Les bactéries pénètrent par des marges fuyantes et réinfectent le système canalaire.
Les fractures structurelles représentent un autre mode d'échec majeur. Les dents traitées endodontiquement perdent leur teneur en humidité et deviennent fragiles. Sans couronnes de couverture complète, les dents postérieures peuvent se fendre verticalement. Ces fractures rendent souvent la dent non restaurable.
Comment les cliniciens gèrent-ils les traitements échoués ?
Le retraitement non chirurgical enlève les anciennes obturations et traite l'anatomie manquée. La chirurgie apicale enlève le bout de la racine et place des scellants rétrogrades. L'extraction reste le dernier recours lorsque des fractures ou une perte osseuse extensive se produisent.
Le retraitement endodontique suit les mêmes principes que le traitement primaire avec une complexité ajoutée. Le dentiste doit enlever les obturations en gutta-percha, négocier autour des instruments séparés s'ils sont présents, et localiser les canaux précédemment manqués. Les microscopes aident considérablement dans ces procédures.
La chirurgie apicale (apicoectomie) devient nécessaire lorsque des lésions persistantes résistent à un traitement de retraitement conventionnel. Le chirurgien reflète un lambeau, retire l'apex de la racine et place un remplissage rétrograde. Les techniques microsurgicales modernes utilisant des pointes ultrasoniques et des scellants biocéramiques atteignent des taux de guérison de 90 %.
Quelles alternatives existent en dehors du traitement de canal radiculaire ?
L'extraction dentaire avec remplacement par des implants dentaires ou des bridges constitue l'alternative principale. L'endodontie régénérative offre une option biologique pour les dents immatures. L'observation seule risque des complications systémiques.
Les patients confrontés à des recommandations de traitement de canal radiculaire devraient comprendre toutes les options. Ces alternatives ont des implications distinctes en termes de fonction, de coût et de longévité.
Que comprend l'extraction dentaire ?
L'extraction retire l'ensemble de la dent, y compris la structure de la racine. La procédure coûte moins au départ que le traitement de canal radiculaire, mais nécessite un remplacement pour éviter le mouvement des dents adjacentes et la perte osseuse.
L'extraction fournit une résolution immédiate de la douleur et de l'infection. Le dentiste sectionne le ligament parodontal et élève la dent de l'alvéole. La guérison se produit dans les 7 à 10 jours.
Cependant, l'extraction crée de nouveaux problèmes. Les dents adjacentes s'inclinent dans l'espace. Les dents opposées s'extrudent. L'os alvéolaire se résorbe sans charge fonctionnelle. Ces changements altèrent la morsure et peuvent causer des problèmes de l'articulation temporomandibulaire.
Comment les options de remplacement se comparent-elles ?
Les implants dentaires remplacent des dents uniques sans impliquer les dents adjacentes. Les bridges nécessitent la préparation des dents voisines mais offrent un remplacement fixe immédiat. Les prothèses partielles amovibles coûtent le moins cher mais offrent une fonction compromise.
Les implants dentaires ont révolutionné le remplacement dentaire. Les dispositifs en titane s'intègrent à l'os par le biais de l'ostéo-intégration. Ils fournissent un soutien autonome sans préparer les dents adjacentes. Cependant, les implants nécessitent un volume osseux adéquat et des périodes de guérison de 3 à 6 mois.
Les bridges traditionnels nécessitent de couronner les dents adjacentes à l'espace. Le dentiste prépare ces dents de manière similaire aux préparations de couronnes uniques. Le bridge relie les couronnes sur les dents de soutien à un pontique remplaçant la dent manquante. Cette approche risque la santé à long terme des dents de soutien.
Les prothèses partielles amovibles offrent l'option la plus économique. Ces appareils s'accrochent aux dents restantes et remplacent plusieurs unités manquantes. Cependant, elles nécessitent un retrait quotidien pour le nettoyage et peuvent affecter la parole et le goût.
Quelles sont les considérations fonctionnelles et économiques ?
Préserver les dents naturelles par un traitement de canal radiculaire coûte généralement moins cher à long terme que l'extraction et la pose d'implants. Les dents naturelles offrent une proprioception supérieure et des résultats esthétiques par rapport aux remplacements artificiels.
L'analyse économique favorise la préservation des dents. Le traitement de canal radiculaire plus la pose de couronne coûte environ 50-70 % de l'extraction plus la thérapie par implant. De plus, les dents naturelles nécessitent rarement l'entretien que demandent les implants.
Fonctionnellement, le ligament parodontal entourant les dents naturelles fournit un retour sensoriel qui empêche des forces de morsure excessives. Ce mécanisme protège à la fois la dent et l'os environnant. Les implants manquent de cette boucle de rétroaction protectrice.
Quels mythes entourent l'élimination du nerf dentaire ?
Les mythes affirment que les traitements de canal "tuent" les dents, causent des maladies systémiques ou entraînent invariablement une douleur sévère. Les preuves scientifiques réfutent ces affirmations de manière définitive.
La désinformation sur la thérapie endodontique persiste malgré des décennies de recherche. S'attaquer à ces mythes aide les patients à prendre des décisions basées sur des faits plutôt que sur la peur.
Le traitement de canal tue-t-il la dent ?
Non. La dent reste vivante grâce aux tissus parodontaux environnants. Elle continue de fonctionner normalement sans la pulpe interne.
La notion selon laquelle le traitement de canal "tue" la dent reflète une mauvaise compréhension de la biologie dentaire. La dent se compose de plus que la chambre pulpaire. Le ligament parodontal reste vital après le traitement. Ce tissu fournit de la nutrition, un retour sensoriel et une attache à l'os.
La dent continue de ressentir la pression à travers le ligament parodontal. Elle maintient sa position dans l'arc. Elle résiste aux forces de mastication. Sans la pulpe, la dent manque simplement de sensation de température et de la capacité de former de la nouvelle dentine en interne.
Cette procédure cause-t-elle une douleur sévère ?
L'anesthésie moderne et les techniques rendent le traitement de canal aussi inconfortable que des plombages de routine. La plupart des patients ressentent un soulagement de la douleur préopératoire immédiatement après la procédure.
Historiquement, les traitements de canal avaient une réputation douloureuse. Cette réputation ne s'applique plus. Les anesthésiques locaux bloquent efficacement la sensation de la pulpe dans la plupart des cas. Pour les dents "chaudes" avec une inflammation sévère, des techniques d'anesthésie supplémentaires et une injection intra-osseuse fournissent une engourdissement profond.
L'inconfort postopératoire, lorsqu'il se produit, répond généralement aux analgésiques en vente libre. La procédure soulage la douleur sévère de la pulpite bien plus souvent qu'elle ne cause d'inconfort.
Les canaux radiculaires causent-ils des maladies systémiques ?
Aucune preuve scientifique ne lie les traitements de canal correctement réalisés au cancer, aux maladies cardiaques ou à d'autres conditions systémiques. Ce mythe provient de recherches discréditées il y a près d'un siècle.
La "théorie de l'infection focale" proposait que les bactéries dans la bouche causent des maladies des organes distants. Les premiers partisans affirmaient que les dents traitées par un canal radiculaire abritent des bactéries qui causent des maladies systémiques. Cette théorie a guidé des milliers d'extractions inutiles au début du 20ème siècle.
La recherche moderne réfute cette affirmation. Les traitements de canal radiculaire bien réalisés scellent complètement le système canalaire. Le système immunitaire gère la charge bactérienne minimale provenant de toute infection résiduelle. Aucune étude évaluée par des pairs ne lie les dents traitées endodontiquement à des maladies systémiques.
Quelles innovations futures transformeront l'endodontie ?
La thérapie par cellules souches, l'édition génétique, les procédures guidées par IA et les matériaux biomimétiques permettront la régénération de la pulpe biologique plutôt que son remplacement par des matériaux synthétiques. Ces avancées pourraient éventuellement éliminer le besoin d'une extraction traditionnelle du nerf dans de nombreux cas.
L'endodontie régénérative représente la frontière la plus excitante dans le domaine. Plutôt que d'enlever la pulpe et de remplir avec des matériaux inertes, les chercheurs visent à restaurer la vitalité biologique.
Comment la thérapie par cellules souches changera-t-elle le traitement ?
La transplantation de cellules souches de pulpe dentaire (CSPD) et de cellules souches provenant de dents temporaires exfoliées (SHED) régénérera le tissu pulpaire fonctionnel, restaurera la défense immunitaire et permettra le développement continu des racines dans les dents immatures.
Les essais cliniques démontrent la faisabilité de la régénération de la pulpe. Nakashima et al. (2017) ont réalisé le premier essai clinique conforme aux BPF utilisant des cellules souches de pulpe dentaire mobilisées autologues. Ils ont implanté ces cellules dans des échafaudages d'atélo-collagène avec des facteurs de croissance. Les patients ont retrouvé la sensibilité de la pulpe en quelques semaines. L'imagerie a confirmé la formation de tissu semblable à de la dentine et la vascularisation.
Xuan et al. (2018) ont mené un essai contrôlé randomisé comparant la transplantation de cellules souches à l'apexification dans des dents immatures. Le groupe de cellules souches a montré un développement radiculaire supérieur, une fermeture apicale et une formation de tissu semblable à de la pulpe. Huang et al. (2024) ont passé en revue ces avancées et ont conclu que les CSPD montrent une plus grande capacité régénérative que les cellules souches mésenchymateuses de la moelle osseuse pour les applications dentaires.
Quel rôle jouera la thérapie génique ?
L'édition génétique utilisant la technologie CRISPR/Cas9 pourrait activer des gènes dentinogéniques dans les cellules résidentes. Cette approche pourrait stimuler la régénération naturelle de la pulpe sans transplantation cellulaire.
La thérapie génique offre une approche sans cellules pour la régénération. Les chercheurs proposent d'introduire des gènes codant pour des protéines morphogénétiques osseuses (BMP) et le facteur de croissance endothélial vasculaire (VEGF) dans l'espace du canal radiculaire. Ces gènes stimuleraient les cellules souches résidentes à se différencier en odontoblastes et en cellules endothéliales.
Les approches ex vivo impliquent la transduction de cellules souches récoltées pour surexprimer des gènes régénératifs avant l'implantation. Ces cellules modifiées produisent une libération soutenue de facteurs de croissance, améliorant la formation des tissus.
Comment l'IA et la robotique amélioreront-elles les résultats ?
Les algorithmes d'apprentissage automatique prédiront les résultats des traitements et optimiseront la sélection des instruments. Les systèmes robotiques pourront réaliser le façonnage des canaux avec une précision surhumaine.
L'intelligence artificielle analyse désormais les scans CBCT pour détecter les variations de l'anatomie des canaux que l'œil humain ne remarque pas. Les applications futures guideront l'instrumentation en temps réel, alertant les dentistes des perforations imminentes ou des risques de séparation des instruments.
Les technologies d'impression 3D fabriqueront des échafaudages spécifiques aux patients correspondant aux morphologies exactes des canaux radiculaires. Ces échafaudages soutiendront la croissance cellulaire et l'intégration vasculaire.
Les matériaux biocéramiques continuent d'avancer. De nouveaux scellants se lient chimiquement à la dentine et fournissent des effets antibactériens. Ces matériaux pourraient éventuellement permettre une régénération complète de la pulpe en soutenant l'attachement et la différenciation des cellules.
Conclusion
L'élimination du nerf dentaire par le traitement de canal radiculaire est l'une des interventions les plus réussies en dentisterie. Cette procédure préserve les dents naturelles qui, autrement, nécessiteraient une extraction. Les techniques modernes atteignent des taux de survie de 97 % à 10 ans et de 68 % à 37 ans, selon des études longitudinales évaluées par des pairs.
La procédure traite les infections par biofilm bactérien dans la chambre pulpaire. Elle élimine les sources de douleur tout en maintenant la fonction dentaire. Les avancées dans l'instrumentation en nickel-titane, la visualisation microscopique et les scellants biocéramiques ont transformé ce traitement d'une procédure redoutée en une thérapie confortable et prévisible.
Les patients confrontés à cette recommandation doivent comprendre la base biologique du traitement. Le rôle de la pulpe diminue après la maturation de la dent, permettant son retrait sans compromettre la viabilité de la dent. Des alternatives existent, mais la préservation de l'anatomie naturelle par la thérapie endodontique fournit généralement la solution à long terme la plus rentable et fonctionnelle.
Les innovations futures promettent des résultats encore meilleurs. L'endodontie régénérative utilisant des cellules souches pourrait finalement restaurer la vitalité biologique plutôt que de simplement remplir des canaux vides. La thérapie génique et l'ingénierie tissulaire pourraient régénérer des complexes pulpe-dentine indiscernables des tissus naturels.
Un diagnostic précoce reste crucial. Les patients éprouvant des douleurs dentaires persistantes, une sensibilité à la température ou un gonflement devraient demander une évaluation immédiate. Un retard augmente la complexité du traitement et réduit les probabilités de succès.
Références
Carvalho, Thiago Saads, et Lussi, Adrian. "Changements morphologiques, histologiques et fonctionnels liés à l'âge dans les dents." Journal of Oral Rehabilitation, vol. 44, no. 4, 2017, pp. 291-298.
Gillen, BM, et al. "Impact du type de dent et de la procédure endodontique sur le résultat du traitement de canal radiculaire : une revue systématique." Journal of Endodontics, vol. 37, no. 4, 2011, pp. 449-457.
Gronthos, Stan, et al. "Cellules souches de pulpe dentaire humaine postnatales (DPSCs) in vitro et in vivo." Actes de l'Académie nationale des sciences, vol. 97, no. 25, 2000, pp. 13625-13630.
Huang, Y, et al. "Cellules souches mésenchymateuses pour la régénération de la pulpe dentaire : une étude comparative de différentes sources." Stem Cells International, 2024.
López-Valverde, Isabel, et al. "Survie et succès à long terme des dents après traitement endodontique primaire : une observation rétrospective de 5 à 37 ans." Investigations cliniques orales, vol. 27, no. 6, 2023, pp. 2545-2556.
Nakashima, Misako, et al. "Transplantation de cellules souches de pulpe dentaire humaine pour une régénération complète de la pulpe." Recherche et thérapie par cellules souches, vol. 8, no. 1, 2017, pp. 1-12.
Niki, Yogita, et al. "Anatomie, tête et cou, pulpe dentaire." StatPearls, StatPearls Publishing, 2025, https://www.ncbi.nlm.nih.gov/books/NBK537112/.
Svensäter, G, et Bergenholtz, G. "Biofilms dans les infections endodontiques." Sujets endodontiques, vol. 9, no. 1, 2004, pp. 27-36.
Xuan, K, et al. "Les cellules souches dentaires autologues des dents de lait régénèrent la pulpe dentaire après implantation dans des dents blessées." Médecine translationnelle en science, vol. 10, no. 455, 2018, eaaf3227.