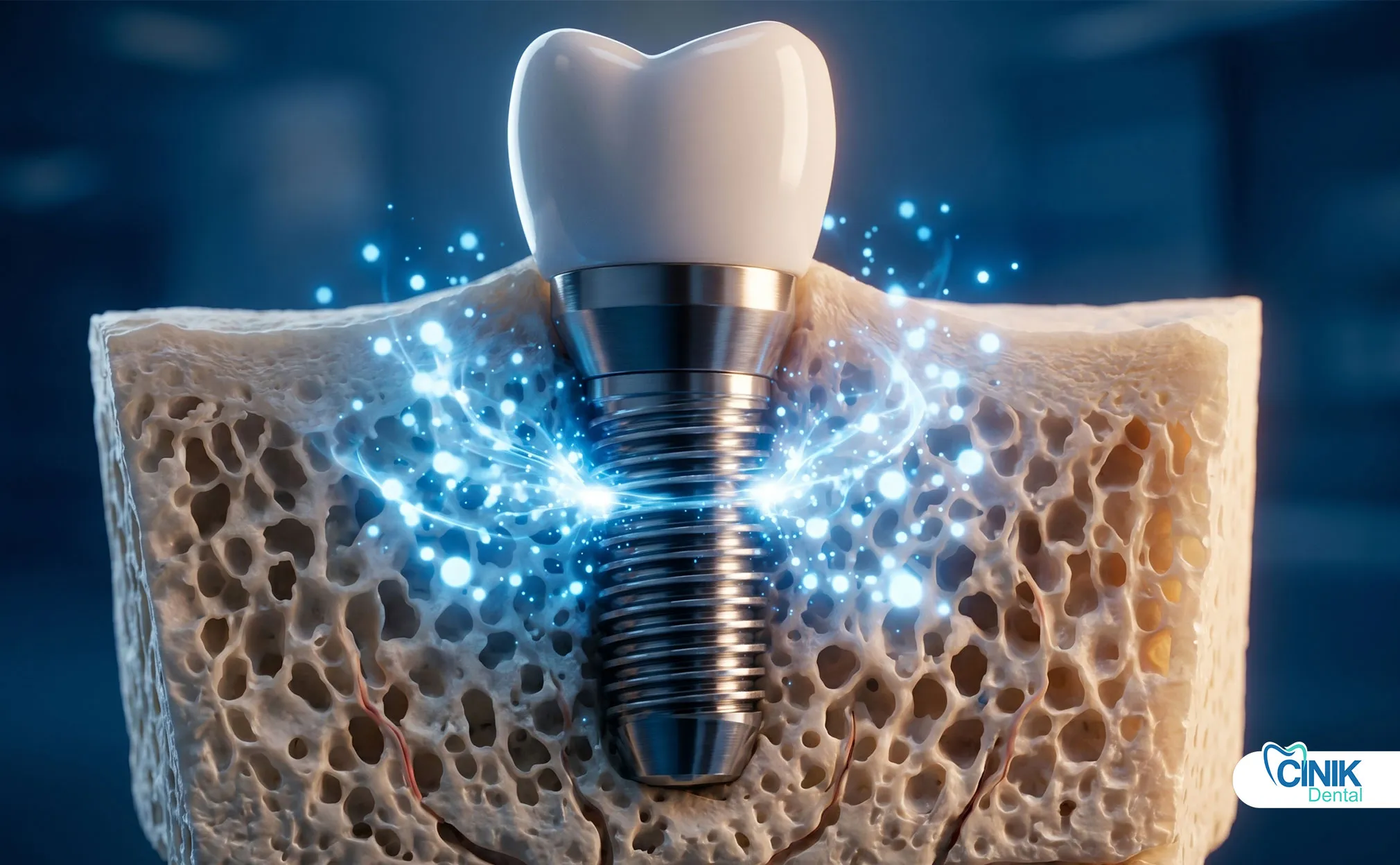
Что такое терапия экзосомами и почему это важно для зубных имплантатов?
Терапия экзосомами представляет собой прорыв в регенеративной стоматологии. Это лечение без клеток использует крошечные везикулы для ускорения заживления костей, уменьшения воспаления и улучшения показателей успеха имплантатов. В отличие от традиционных подходов с использованием стволовых клеток, терапия экзосомами доставляет факторы роста без живых клеток, устраняя риски отторжения или образования опухолей.
Зубные имплантаты служат золотым стандартом для замены зубов. Однако клиницисты сталкиваются с постоянными проблемами. У некоторых пациентов наблюдается задержка заживления. Другие страдают от периимплантного воспаления или недостаточной плотности кости. Эти осложнения ставят под угрозу стабильность и долговечность имплантатов.
Регенеративная стоматология теперь обращается к экзосомам как к решению. Эти наночастицы действуют как биологические посланники. Они переносят белки, РНК и липиды, которые стимулируют естественные процессы восстановления. Исследования показывают, что они улучшают остеоинтеграцию, критическое слияние между имплантатом и костью (Valadi et al., 2007). Эта статья рассматривает, как терапия экзосомами трансформирует имплантационную стоматологию через научные механизмы, клинические применения и будущий потенциал.
Что такое экзосомы и как они функционируют в восстановлении тканей?
Экзосомы — это внеклеточные везикулы диаметром от 30 до 150 нанометров. Клетки выпускают эти пузырьки для общения с соседними тканями. Они происходят из эндосомального пути через процесс, называемый слиянием мультивезикулярного тела. Представьте их как биологические текстовые сообщения. Одна клетка отправляет инструкции. Другая клетка получает сигнал и изменяет свое поведение.
Таблица 1: Основные компоненты экзосом и их функции
Компонент | Функция | Терапевтическое воздействие |
Белки | Сигнализация клеток | Активация путей восстановления |
миРНК | Регуляция генов | Контроль воспаления и роста костей |
мРНК | Синтез белков | Прямая регенерация тканей |
Липиды | Структура мембраны | Обеспечение стабильности и слияния клеток |
Состав варьируется в зависимости от исходной клетки. Экзосомы, полученные из мезенхимальных стволовых клеток (MSC-экзосомы), содержат более 850 белков, включая трансформирующий фактор роста-β и инсулиноподобный фактор роста (Zhang et al., 2020). Стволовые клетки зубной пульпы выделяют экзосомы, обогащенные остеогенными миРНК. Этот специализированный груз объясняет, почему экзосомы из разных источников вызывают различные эффекты заживления.
Экзосомы решают основные проблемы, связанные с терапией стволовыми клетками. Стволовые клетки могут вызывать иммунные реакции. Они могут образовывать опухоли. Они требуют строгих условий хранения. Экзосомы полностью обходят эти проблемы. Они предлагают низкую иммуногенность, высокую биосовместимость и сниженные проблемы безопасности (Shi et al., 2021). Пациенты получают регенеративные преимущества без клеточных рисков.
Как экзосомы способствуют образованию костей вокруг зубных имплантатов?
Какие механизмы усиливают остеогенез?
Экзосомы активируют несколько путей для построения костей. Они стимулируют дифференцировку остеобластов. Они увеличивают отложение костного матрикса. Они усиливают минерализацию по всему месту заживления.
Исследования Фурута и др. (2016) демонстрируют, что MSC-экзосомы способствуют заживлению переломов в моделях на мышах. Экзосомы повышают активность щелочной фосфатазы (ALP). Этот фермент служит ранним маркером образования кости. Уровни остеокальцина (OCN) также повышаются. Этот белок указывает на развитие зрелого костного матрикса.
Три основных сигнальных пути управляют этими эффектами:
Путь BMP/Smad: Экзосомы доставляют костные морфогенетические белки. Эти белки связываются с рецепторами на поверхности клеток. Они активируют транскрипционные факторы Smad. Увеличивается экспрессия Runx2 и Osterix. Образование кости ускоряется.
Путь Wnt/β-катенин: Экзосомы стабилизируют β-катенин в клетках-реципиентах. Эта молекула проникает в ядро. Она активирует гены, ответственные за пролиферацию и дифференцировку клеток. Чжан и др. (2020) обнаружили, что экзосомы MSC из пуповины человека уменьшают потерю кости через этот механизм.
Путь PI3K/AKT: Экзосомы запускают сигналы выживания в целевых клетках. Это предотвращает апоптоз в критической ранней фазе заживления. Исследования показывают, что ингибирование этого пути блокирует индуцированное экзосомами образование кости (Чен и др., 2019).
Как экзосомы улучшают кровоснабжение мест имплантации?
Ангиогенез оказывается необходимым для успешной остеоинтеграции. Костная ткань нуждается в кислороде и питательных веществах. Без адекватной васкуляризации имплантаты терпят неудачу.
Экзосомы стимулируют выработку сосудистого эндотелиального фактора роста (VEGF). Они побуждают эндотелиальные клетки формировать трубчатые структуры. Ци и др. (2016) наблюдали, что экзосомы hiPS-MSC в сочетании с β-TCP каркасами усиливают как регенерацию кости, так и ангиогенез в моделях на крысах. Сосуды проникают глубже в материал костного трансплантата. Это двойное действие, создание кости плюс создание сосудов, создает благоприятную среду для интеграции имплантата.
Какую роль играют экзосомы в контроле воспаления?
Воспаление разрушает имплантаты. Периимплантит поражает до 20% пациентов с зубными имплантатами. Традиционные антибиотики помогают, но создают проблемы с резистентностью. Экзосомы предлагают биологическое решение.
Экзосомы, полученные из стволовых клеток зубной пульпы (DPSC-EXO), подавляют провоспалительные цитокины. Они ингибируют выработку IL-1β и TNF-α. Они блокируют сигнальный путь IL-6/JAK2/STAT3 (Ли и др., 2023). Этот путь управляет разрушительным воспалением в пародонтальных тканях.
Макрофаги изменяют свое поведение после воздействия экзосом. Провоспалительные макрофаги M1 трансформируются в противовоспалительные макрофаги M2. Этот сдвиг поляризации снижает повреждение тканей. Он создает процелебную среду вокруг имплантата (Шен и др., 2020).
Где клиницисты могут применять терапию экзосомами в имплантологической стоматологии?
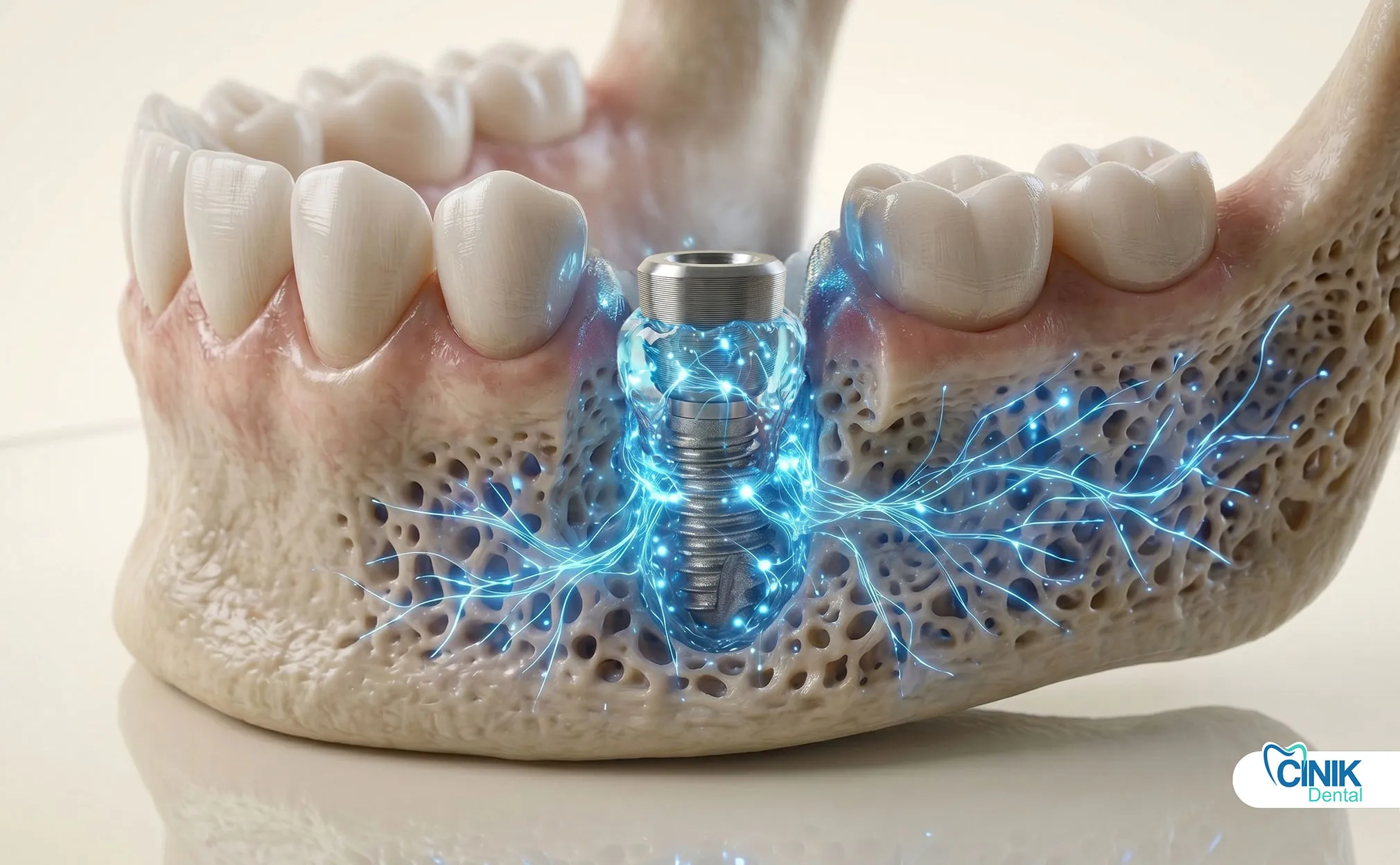
Могут ли экзосомы ускорить остеоинтеграцию в стандартных случаях имплантации?
Да. Экзосомы значительно улучшают контакт кости с имплантатом. Они ускоряют сроки интеграции. Традиционная остеоинтеграция требует от трех до шести месяцев. Терапия экзосомами может сократить этот период на 30-40% на основе доклинических данных.
Ван и др. (2020) разработали самовосстанавливающийся гидрогель, содержащий экзосомы МСК из пуповины. Материал способствовал регенерации кости в дефектах критического размера. Объемная доля кости увеличилась по сравнению с контрольными группами. Это предполагает более быструю и надежную интеграцию имплантата при наличии экзосом.
Помогают ли экзосомы пациентам с недостаточной костной тканью?
Безусловно. Регенерация альвеолярной кости представляет собой основное применение. У многих пациентов недостаточно кости для немедленной установки имплантата. Экзосомы улучшают процедуры костной пластики. Они улучшают результаты увеличения гребня. Они предотвращают резорбцию кости после удаления.
Таблица 2: Источники экзосом и их регенеративные свойства
Источник | Остеогенный потенциал | Иммуномодулирующая сила | Доступность |
МСК костного мозга | Высокий | Умеренный | Инвазивный |
Стволовые клетки зубной пульпы | Очень высокий | Очень высокий | Минимально инвазивный |
Периодонтальная связка | Высокий | Высокий | Умеренный |
Гингивальные МСК | Умеренный | Очень высокий | Легкий |
Дентальные стволовые клетки предоставляют превосходные экзосомы для оральных применений. Они выражают специфические маркеры, такие как CD24 и CD140a. Эти клетки размножаются быстрее, чем альтернативы из костного мозга. Они устойчивы к старению во время расширения культуры. Самое главное, они естественно адаптируются к оральной среде (Котова и др., 2021).
Могут ли экзосомы заживлять мягкие ткани вокруг имплантатов?
Печати мягких тканей предотвращают бактериальное вторжение. Они защищают подлежащую кость. Экзосомы ускоряют заживление гингивальных ран. Они стимулируют миграцию фибробластов и производство коллагена.
Чжоу и др. (2022) продемонстрировали, что функционализированные экзосомами каркасы улучшили интеграцию мягких тканей. Гингивальный эпителий зажил более полно. Это уменьшило послеоперационные осложнения. Это улучшило окончательные эстетические результаты для передних имплантатов.
Эффективны ли экзосомы против периимплантных заболеваний?
Исследования сильно поддерживают это применение. Периимплантит включает бактериальную инфекцию и воспалительную потерю кости. Экзосомы обеспечивают двойную защиту. Они модулируют иммунные ответы. Они также несут антимикробные пептиды.
Лэй и др. (2022) показали, что экзосомы, полученные из стволовых клеток, лечили воспалительную потерю кости в моделях периодонтита. Фракция объема кости значительно улучшилась. Количество остеокластов, положительных на тартрат-резистентную кислую фосфатазу (TRAP), уменьшилось. Это указывает на уменьшение разрушения кости.
Какие источники предоставляют лучшие экзосомы для дентальных применений?
Мезенхимальные стволовые клетки остаются основным источником. Однако дентальные ткани предлагают уникальные преимущества.
Стволовые клетки зубной пульпы (DPSCs): Эти клетки находятся внутри зубных структур. Они демонстрируют высокие темпы пролиферации. Они сохраняют сильный остеогенный потенциал даже после многократных пассировок. Экзосомы DPSCs содержат специфические микроРНК, которые способствуют ангиогенезу и нейропротекции.
Стволовые клетки периодонтальной связки (PDLSCs): Эти клетки соединяют зубы с костью. Они естественным образом регулируют гомеостаз периодонта. Их экзосомы превосходны в регенерации мягких тканей и формировании интерфейса кость-связка.
Стволовые клетки из выпавших молочных зубов человека (SHEDs): Эти клетки происходят из молочных зубов. Они демонстрируют исключительную пластичность. Они дольше других источников выражают ранние маркеры стволовых клеток. Экзосомы SHED могут предлагать превосходные нейрорегенеративные свойства.
Инженерные экзосомы: Ученые теперь загружают экзосомы специфическим грузом. Они добавляют HIF-1α для усиления ангиогенеза. Они включают miR-375 для улучшения остеогенеза (Chen et al., 2019). Эта настройка позволяет целевую терапию для конкретных осложнений имплантатов.
Какие клинические преимущества получают пациенты от терапии экзосомами?
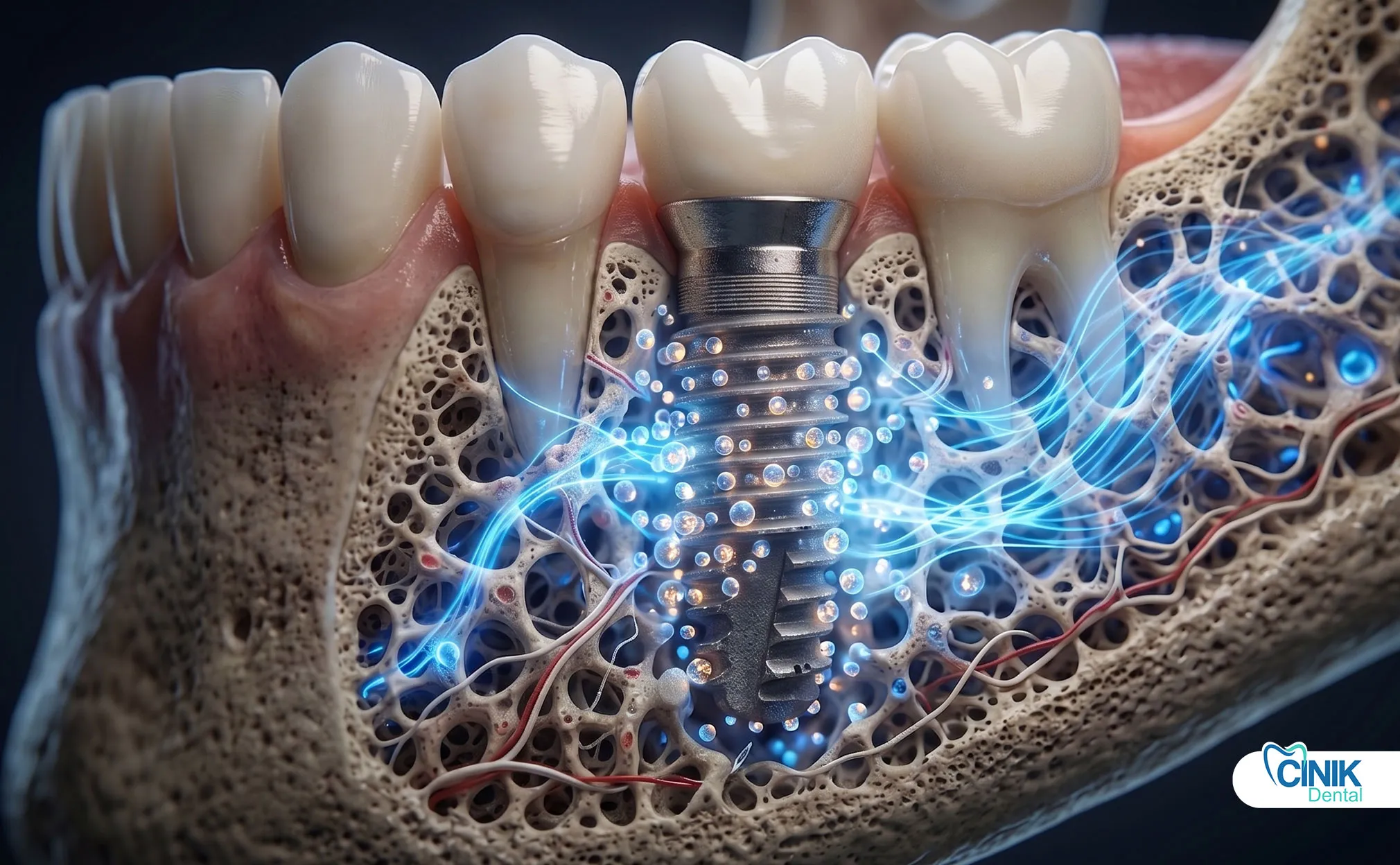
Пациенты испытывают измеримые улучшения:
Более быстрое заживление: Участки, обработанные экзосомами, показывают более раннюю минерализацию кости. Мягкие ткани закрываются быстрее. Это сокращает время между установкой имплантата и окончательной реставрацией.
Меньше боли и отека: Противовоспалительное действие снижает послеоперационный дискомфорт. Пациенты сообщают о более низких показателях боли. Им требуется меньше обезболивающих препаратов.
Более высокие показатели успеха: Ранняя интеграция предотвращает микродвижение. Это снижает риск отказа имплантата. Экзосомы могут быть особенно ценными для пациентов с диабетом, остеопорозом или курением в анамнезе, групп, традиционно считающихся высокорисковыми.
Минимально инвазивная доставка: Клиницисты применяют экзосомы через гидрогели, коллагеновые мембраны или прямую инъекцию. Дополнительная операция не требуется. Терапия легко интегрируется в стандартные протоколы имплантации.
Персонализированные возможности: Будущие лечения могут использовать экзосомы, специфичные для пациента. Клетки, извлеченные из удаленных зубов мудрости, могут предоставить персонализированные регенеративные терапии.
Какие ограничения и вызовы существуют в настоящее время?
Почему терапия экзосомами еще не широко доступна?
Пробелы в доказательствах: Большинство исследований остаются доклиническими. Исследователи провели обширные испытания на животных. Клинические испытания на людях отстают. Долгосрочные данные о выживаемости имплантатов с терапией экзосомами пока не существуют.
Проблемы стандартизации: Не существует универсального протокола для изоляции экзосом. Дифференциальное ультрацентрифугирование остается популярным, но дает переменные выходы. Методы осаждения увеличивают количество, но снижают чистоту. Микрофлюидные технологии обещают стабильность, но требуют дорогого оборудования (Miron et al., 2025).
Регуляторные препятствия: Регуляторные органы классифицируют экзосомы как биологические продукты. Они требуют обширных испытаний на безопасность. Массовое производство должно соответствовать стандартам надлежащей производственной практики. Эти требования замедляют клиническое внедрение.
Технические барьеры: Экзосомы разрушаются при хранении. Они требуют специфических температурных условий. Они теряют активность при неправильном обращении. Системы доставки должны защищать экзосомы до их достижения целевых тканей. Текущие каркасы и гидрогели предоставляют частичные решения. Необходимы лучшие носители.
Как экзосомы сравниваются с другими регенеративными методами лечения?
Таблица 3: Сравнение регенеративных терапий
Характеристика | Экзосомы | Стволовые клетки | PRP | Материалы для костных трансплантатов |
Без клеток | Да | Нет | Частично | Да |
Иммуногенность | Очень низкая | Умеренная | Низкая | Очень низкий |
Риск опухоли | Отсутствует | Низкий | Отсутствует | Отсутствует |
Концентрация факторов роста | Очень высокая | Умеренная | Умеренная | Низкая |
Сложность обработки | Умеренная | Высокая | Низкая | Низкая |
Стоимость | Умеренная | Высокая | Низкая | Переменная |
Экзосомы превосходят стволовые клетки по безопасности. Они избегают риска обязательств. Они устраняют опасения по поводу непредсказуемой дифференциации клеток in vivo. Они обеспечивают концентрацию факторов роста в три раза выше, чем у взрослых стволовых клеток, согласно последним анализам.
По сравнению с плазмой, богатой тромбоцитами (PRP), экзосомы предлагают большую стабильность. Качество PRP варьируется в зависимости от возраста и состояния здоровья пациента. Экзосомы из культивируемых стволовых клеток сохраняют стандартизированную эффективность. Они обеспечивают предсказуемые терапевтические эффекты.
Материалы для костных трансплантатов обеспечивают структурную поддержку. Экзосомы предоставляют биологические инструкции. Комбинация оказывается превосходной. Каркасы из β-ТКП, загруженные экзосомами, регенерируют кость быстрее, чем каркасы без них (Ying et al., 2020).
Какие будущие разработки повлияют на терапию экзосомами?
Персонализированные терапии экзосомами: Клиницисты будут извлекать стволовые клетки из зубных тканей пациента. Они будут культивировать эти клетки и собирать экзосомы. Этот аутологичный подход исключает все риски отторжения. Он максимизирует терапевтическую совместимость.
Интеграция умных биоматериалов: 3D-печатные имплантаты будут включать резервуары экзосом. Эти каркасы будут постепенно высвобождать везикулы. Они будут обеспечивать постоянную стимуляцию в течение всего периода заживления.
Экзосомы с генами: Ученые будут разрабатывать экзосомы, несущие специфические генетические инструкции. Они будут нацелены на пути периимплантита. Они будут ускорять регенерацию нервов в местах имплантации.
Планирование лечения на основе ИИ: Алгоритмы машинного обучения будут предсказывать оптимальные концентрации экзосом. Они будут определять идеальное время доставки. Они будут персонализировать протоколы на основе генетики пациента и качества кости.
Как клиницистам внедрять терапию экзосомами?
Выбор пациентов: Идеальные кандидаты включают пациентов с низкой плотностью костей. Курильщики и диабетики особенно выигрывают. Пациенты, которым требуется немедленная установка имплантата в местах экстракции, демонстрируют улучшенные результаты.
Противопоказания: Пациенты с активными инфекциями требуют предварительного лечения. Те, у кого есть нарушения свертываемости крови, нуждаются в тщательной оценке. Беременные пациентки должны подождать до послеродового периода из-за ограниченных данных о безопасности.
Протоколы интеграции: Клиницисты должны включать экзосомы во время установки имплантата. Они могут наносить их на место остеотомии перед установкой имплантата. Они могут пропитывать коллагеновые мембраны растворами экзосом. Они могут смешивать экзосомы с материалами для костных трансплантатов для процедур подъема синуса.
Соображения по стоимости: В настоящее время терапия экзосомами добавляет от 500 до 2000 долларов к процедурам имплантации. Цены снизятся по мере увеличения производства. Страховое покрытие остается ограниченным. Пациенты должны понимать, что это представляет собой инвестицию из собственного кармана в более быстрое заживление.
Заключение
Терапия экзосомами для зубных имплантатов предлагает мощный инструмент регенерации. Эти безклеточные везикулы ускоряют образование костной ткани. Они уменьшают воспаление. Они улучшают стабильность имплантата. Они избегают рисков, связанных с терапиями живыми клетками.
Текущие данные подтверждают их использование для улучшения остеоинтеграции. Они показывают особое обещание для регенерации костной ткани в дефицитных участках. Они предлагают решения для управления заболеваниями периимплантатов. Они плавно интегрируются с передовыми техниками имплантации.
Однако клиницисты должны признавать ограничения. Долгосрочные клинические испытания на людях остаются необходимыми. Усилия по стандартизации должны продолжаться. Регуляторные рамки нуждаются в разработке.
Область быстро развивается. Экзосомы DPSC демонстрируют превосходный потенциал для оральных применений. Инженерные техники улучшают нацеливание и эффективность. Системы доставки становятся более сложными.
Для пациентов это означает более быстрое заживление. Это означает уменьшение осложнений. Это означает более широкий круг кандидатов для лечения имплантатами. Для профессии это представляет сдвиг в сторону биологической, а не просто механической интеграции имплантатов.
Терапия экзосомами находится на пересечении клеточной биологии и клинической стоматологии. Она соединяет лабораторные открытия и уход за пациентами. Хотя это еще не является рутиной, скоро будет. Клиницисты, которые понимают эти механизмы сейчас, будут лидировать в имплантационной стоматологии завтра.
Ссылки
Chen, Shiyi, et al. "Экзосомы, полученные из человеческих мезенхимальных стволовых клеток жировой ткани с чрезмерной экспрессией miR-375, способствуют регенерации костной ткани." Cell Proliferation, vol. 52, no. 5, 2019, doi:10.1111/cpr.12669.
Fan, Linlin, et al. "Имплантат на основе полиэфирэфиркетона, функционализированный экзосомами, с иммуномодулирующими свойствами для улучшения остеоинтеграции." Bioactive Materials, vol. 6, no. 9, 2021, pp. 2754–66, doi:10.1016/j.bioactmat.2021.02.005.
Furuta, T., et al. "Экзосомы, полученные из мезенхимальных стволовых клеток, способствуют заживлению переломов в модели мыши." Stem Cells Translational Medicine, vol. 5, no. 12, 2016, pp. 1620–30, doi:10.5966/sctm.2015-0285.
Kotova, A., et al. "Сравнительный анализ стволовых клеток зубной пульпы и периодонта: различия в морфологии, функциональности, остеогенной дифференциации и протеоме." Biomedicines, vol. 9, no. 11, 2021, p. 1606, doi:10.3390/biomedicines9111606.
Lei, Fengyang, et al. "Лечение воспалительной потери костной ткани при пародонтите с помощью экзосом, полученных из стволовых клеток." Acta Biomaterialia, vol. 141, 2022, pp. 333–43, doi:10.1016/j.actbio.2021.12.035.
Li, Mei, et al. "Экзосомы, полученные из стволовых клеток зубной пульпы, регулируют противовоспалительные и остеогенные процессы в стволовых клетках периодонтальной связки и способствуют восстановлению экспериментального пародонтита у крыс." Frontiers in Bioengineering and Biotechnology, vol. 11, 2023, doi:10.3389/fbioe.2023.10441659.
Мирон, Ричард Дж., и др. "Методы изоляции экзосом, полученных из стволовых клеток зубов." Международный журнал оральной науки, 2025, doi:10.1038/s41368-025-00370-y.
Ци, С., и др. "Экзосомы, секретируемые мезенхимальными стволовыми клетками, полученными из индуцированных плюрипотентных стволовых клеток человека, восстанавливают критические дефекты костей за счет усиленной ангиогенеза и остеогенеза у остеопоротических крыс." Международный журнал биологических наук, том 12, № 7, 2016, стр. 836–49, doi:10.7150/ijbs.14809.
Шен, Чжэнхуа, и др. "Гидрогель хитозана, включающий экзосомы, полученные из стволовых клеток зубной пульпы, облегчает пародонтит у мышей через механизм, зависящий от макрофагов." Биоактивные материалы, том 5, № 4, 2020, стр. 1113–26, doi:10.1016/j.bioactmat.2020.07.002.
Ши, Цинь, и др. "Экзосомы, полученные из МСК: новая перспективная терапия остеопороза." Фронтиры клеточной и развивающейся биологии, том 9, 2021, стр. 723803, doi:10.3389/fcell.2021.723803.
Валади, Хади, и др. "Передача мРНК и микроРНК через экзосомы — это новый механизм генетического обмена между клетками." Природная клеточная биология, том 9, № 6, 2007, стр. 654–59, doi:10.1038/ncb1596.
Ван, Лин, и др. "Новый самовосстанавливающийся гидрогель, содержащий экзосомы, полученные из hucMSC, способствует регенерации костей." Фронтиры биоинженерии и биотехнологии, том 8, 2020, стр. 564731, doi:10.3389/fbioe.2020.564731.
Ин, Чанг, и др. "Экзосомы BMSC несут мутантный HIF-1α для улучшения ангиогенеза и остеогенеза в критических дефектах черепа." Фронтиры биоинженерии и биотехнологии, том 8, 2020, стр. 565561, doi:10.3389/fbioe.2020.565561.
Чжан, Шицин, и др. "Экзосомы МСК облегчают остеоартрит височно-нижнечелюстного сустава, уменьшая воспаление и восстанавливая гомеостаз матрикса." Биоматериалы, том 200, 2019, стр. 35–47, doi:10.1016/j.biomaterials.2019.02.006.
Чжоу, Е, и др. "Биомиметические костные каркасы, покрытые полидопамином и загруженные экзосомами, способствуют остеогенической дифференцировке BMSC и регенерации костей." Регенеративная терапия, том 23, 2023, стр. 25–36, doi:10.1016/j.reth.2023.03.005.