Le traitement des infections dentaires nécessite d'éliminer la source de l'infection par drainage, thérapie de canal radiculaire, ou extraction. Les antibiotiques ne servent que de thérapie adjuvante pour l'implication systémique. Une intervention précoce prévient des complications graves comme la septicémie et la nécrose tissulaire.
Qu'est-ce qu'une infection dentaire et pourquoi est-ce important ?
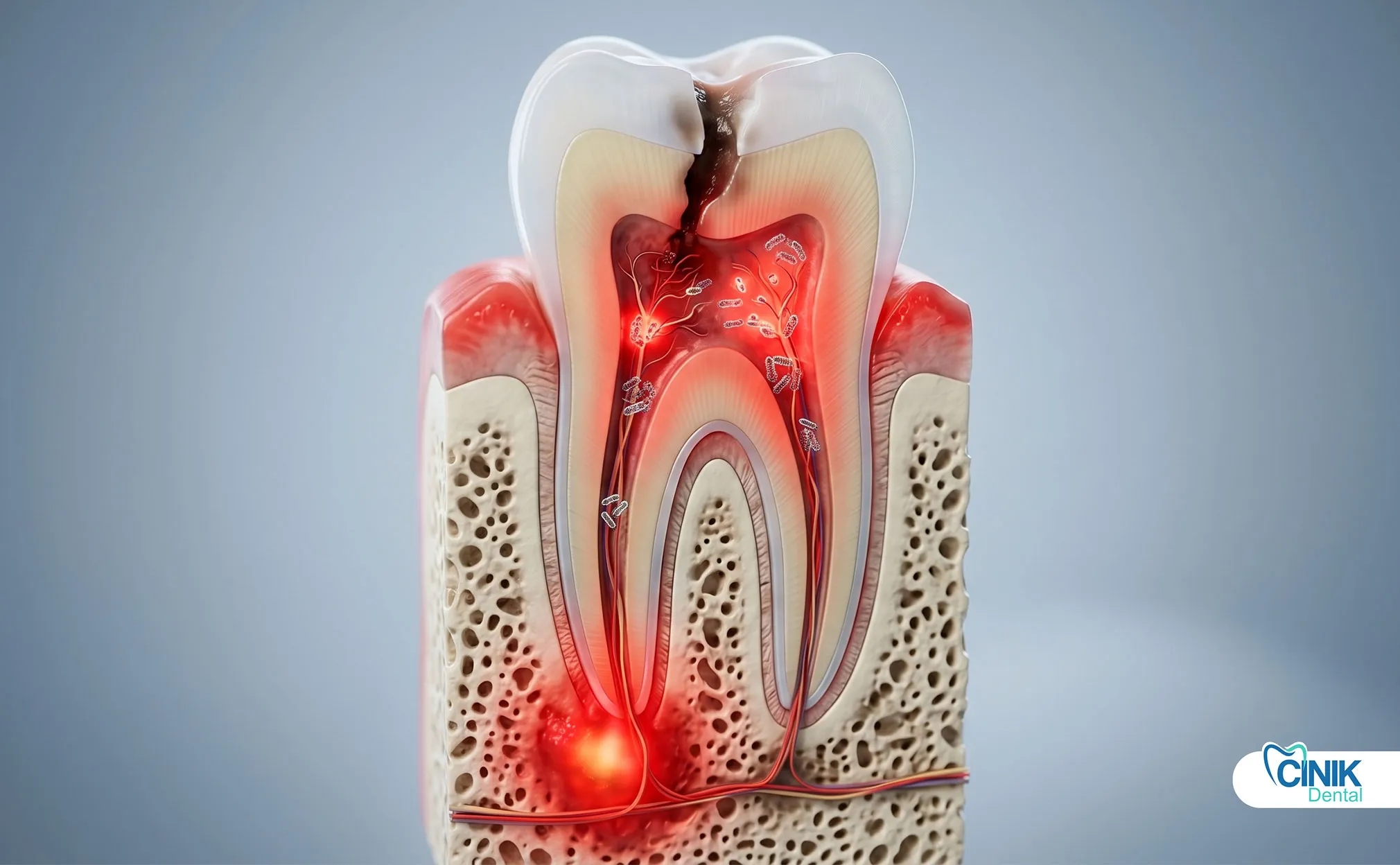
Une infection dentaire est une invasion bactérienne de la pulpe dentaire, des tissus parodentaux ou de l'os environnant. Elle provoque une douleur intense, un gonflement, et peut se propager aux espaces faciaux ou dans la circulation sanguine sans traitement rapide.
Une infection dentaire, cliniquement appelée infection odontogène, se développe lorsque des bactéries pénètrent les couches protectrices d'une dent ou des tissus gingivaux environnants. Ces infections commencent petites mais peuvent s'aggraver en conditions menaçant la vie en quelques jours. L'Organisation mondiale de la santé reconnaît les infections dentaires comme un fardeau de santé mondiale significatif, en particulier dans les populations ayant un accès limité aux soins dentaires (Petersen, 2022).
Les infections dentaires se classent en trois catégories principales en fonction de leur emplacement et de leur origine. Les abcès périapicaux se forment à la pointe de la racine lorsque le tissu pulpaire meurt à cause d'une carie profonde ou d'un traumatisme. Les abcès parodentaux se développent dans les structures de soutien d'une dent affectée par une maladie parodontal avancée. Les abcès gingivaux restent confinés à la marge gingivale, généralement causés par l'impact d'un corps étranger.
La pertinence clinique des infections dentaires va au-delà de l'inconfort oral. Des recherches publiées dans le Journal of Dental Research montrent que les infections dentaires non traitées augmentent le risque cardiovasculaire, compliquent la gestion du diabète et élèvent les marqueurs inflammatoires systémiques (Lockhart, 2019). En 2023, les services d'urgence à travers les États-Unis ont traité plus de 2 millions de cas d'infections dentaires, avec des coûts de traitement moyens dépassant 1 000 $ par visite lorsque l'hospitalisation devenait nécessaire.
Un diagnostic précoce est important car les infections dentaires suivent une progression prévisible. Les bactéries se multiplient dans l'espace confiné d'une racine dentaire ou d'une poche gingivale. La pression augmente. Les tissus gonflent. La réponse immunitaire déclenche de la fièvre et un malaise. Sans intervention, l'infection franchit les barrières locales et pénètre dans les espaces fasciaux, les canaux lymphatiques ou la circulation sanguine.
Le spectre des traitements s'étend des interventions locales aux thérapies systémiques. Les approches locales, drainage, thérapie de canal radiculaire, extraction, éliminent directement la source de l'infection. Les approches systémiques, principalement les antibiotiques, soutiennent la défense de l'organisme lorsque l'infection se propage au-delà de la dent. Le principe clé : le traitement local a la priorité. Les antibiotiques seuls ne peuvent pas stériliser un canal radiculaire infecté ou une cavité d'abcès.
Type d'infection | Emplacement | Cause principale | Traitement typique |
ABCÈS PÉRIAPICAL | Apex radiculaire | Nécrose pulpaire | Canal radiculaire ou extraction |
ABCÈS PARODONTAL | Structures de soutien | Parodontite avancée | Drainage + thérapie parodontal |
ABCÈS GINGIVAL | Marge gingivale | Impactation de corps étranger | Drainage + élimination de l'irritant |
Qu'est-ce qui cause le développement des infections dentaires ?
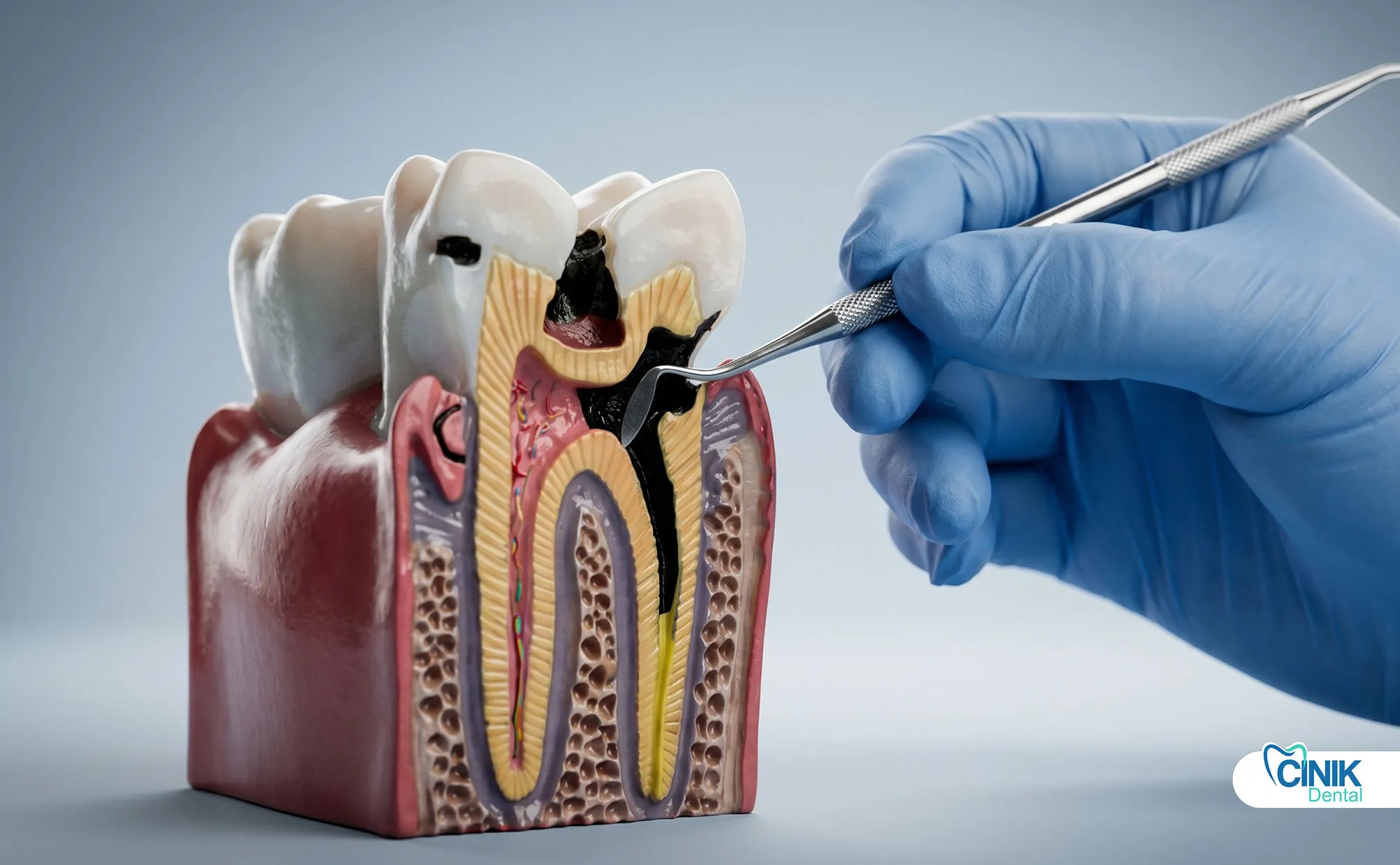
Les caries dentaires, les traumatismes, les restaurations échouées et la maladie parodontal permettent aux bactéries d'envahir la pulpe dentaire et les tissus environnants. La formation de biofilm protège les bactéries et accélère la destruction des tissus.
Comment les bactéries envahissent-elles les tissus dentaires ?
Les bactéries pénètrent par des fissures de l'émail, des cavités profondes ou des poches gingivales. Elles forment des biofilms qui résistent aux attaques immunitaires et aux antibiotiques, puis détruisent la pulpe, l'os et les tissus mous.
Les infections dentaires commencent par une colonisation bactérienne. La cavité buccale abrite plus de 700 espèces bactériennes, mais seulement une poignée provoque des infections invasives. Streptococcus mutans initie la carie dentaire en métabolisant les sucres en acide. Aggregatibacter actinomycetemcomitans et Porphyromonas gingivalis provoquent la destruction parodontal. Lorsque ces organismes franchissent les défenses de l'émail ou des gencives, ils accèdent à la pulpe dentaire, une chambre stérile contenant des nerfs et des vaisseaux sanguins.
Les caries dentaires restent la principale cause d'infection de la pulpe. Les cavités non traitées progressent à travers l'émail, la dentine, et enfin dans la chambre pulpaire. La pulpe réagit par une inflammation, mais les toxines bactériennes et la pression finissent par tuer le tissu. La pulpe nécrotique devient un terrain de reproduction pour les bactéries anaérobies.
Le traumatisme accélère le risque d'infection. Les dents fissurées, même sans fractures visibles, permettent l'entrée des bactéries. Les restaurations ratées créent des espaces microscopiques où les bactéries s'accumulent. Les traitements de canal radiculaire qui manquent des branches du canal laissent une infection résiduelle.
La maladie parodontal fournit une voie alternative. À mesure que les poches gingivales s'approfondissent, les bactéries migrent le long de la surface radiculaire. Le système immunitaire attaque à la fois les bactéries et le tissu hôte, détruisant le ligament parodontal et l'os alvéolaire. Les poches profondes dépassant 7 millimètres abritent fréquemment des bactéries formant des abcès.
La formation de biofilm complique le traitement. Les bactéries sécrètent des polysaccharides extracellulaires qui forment une matrice protectrice. Ce biofilm protège les organismes des antibiotiques, des anticorps de la salive et des cellules immunitaires. Au sein d'un biofilm, les bactéries communiquent par le biais de la détection de quorum et partagent des gènes de résistance. Les recherches de Seneviratne (2017) dans Periodontology 2000 confirment que les bactéries intégrées dans un biofilm démontrent jusqu'à 1 000 fois plus de résistance aux antibiotiques que les cellules planctoniques.
Quels sont les principaux types d'infections dentaires ?
Les abcès périapicaux affectent les pointes des racines, les abcès parodontal attaquent les structures de soutien, et les abcès gingivaux restent aux marges des gencives. Chaque type nécessite un timing et une approche de traitement différents.
Abcès périapical : Cette infection se forme à l'apex d'une racine dentaire après nécrose de la pulpe. Le pus s'accumule dans l'os entourant le bout de la racine. Les patients ressentent une douleur lancinante qui s'aggrave en position couchée. La dent semble élevée dans son alvéole. Un gonflement peut apparaître sur la peau faciale si l'infection perforent l'os. Les radiographies montrent une zone radiolucente à l'apex de la racine. La thérapie de canal radiculaire ou l'extraction résout la source de l'infection.
Abcès parodontal : Cette infection se développe dans une poche parodontal préexistante. Elle provoque une apparition rapide de douleur, de gonflement et d'écoulement purulent du bord gingival. La dent affectée présente souvent une mobilité due à la perte osseuse. Les abcès parodontaux nécessitent un drainage à travers la poche gingivale ou une incision externe. Le détartrage et le surfaçage radiculaire suivent pour réduire la profondeur de la poche.
Abcès gingival : Le type le plus superficiel, confiné au bord gingival. Les corps étrangers, l'impaction alimentaire, les poils de brosse à dents, les fragments de fil dentaire, déclenchent une infection localisée. La douleur reste modérée. Le gonflement reste limité. Le traitement consiste à retirer l'objet étranger et à permettre un drainage naturel.
Comment une infection dentaire se propage-t-elle ?
Les infections se propagent à travers les plans tissulaires locaux, les espaces fasciaux, et finalement dans la circulation sanguine. Un gonflement facial, des difficultés à avaler et de la fièvre signalent une progression dangereuse.
L'invasion tissulaire locale représente la première phase. Les bactéries et les médiateurs inflammatoires détruisent l'os et les tissus mous environnants. La cavité de l'abcès s'agrandit. La pression comprime les nerfs, provoquant une douleur intense. Des enzymes comme la collagénase décomposent les barrières de tissu conjonctif.
L'implication des espaces fasciaux marque une escalade dangereuse. Le visage et le cou contiennent de multiples compartiments de tissu conjonctif séparés par des couches fasciales. Les bactéries se déplacent le long de ces plans, créant des gonflements menaçant la vie. L'infection de l'espace submandibulaire (angine de Ludwig) peut obstruer les voies respiratoires. Le sinus caverneux, accessible par le drainage des veines faciales, présente un risque de thrombose et d'infection cérébrale.
La dissémination systémique se produit lorsque les bactéries pénètrent dans les vaisseaux sanguins. La bactériémie, la présence de bactéries dans le sang, se produit lors de procédures dentaires et même lors d'un brossage vigoureux des dents. Chez les individus en bonne santé, les cellules immunitaires éliminent la bactériémie transitoire. Chez les patients immunodéprimés ou ceux ayant des infections sévères, la bactériémie progresse vers une septicémie. L'endocardite, infection des valves cardiaques, pose un risque particulier pour les patients avec des valves prothétiques ou des dommages cardiaques antérieurs.
Phase de propagation | Emplacement | Signes d'Avertissement | Niveau de Risque |
Localisé | Dent et os immédiat | Douleur dentaire, légère enflure | Faible |
Régional | Espaces fasciaux du visage/du cou | Enflure faciale, trismus, dysphagie | Modéré-Élevé |
Systémique | Système sanguin et organes distants | Fièvre, tachycardie, hypotension, confusion | Critique |
Comment les dentistes reconnaissent-ils et diagnostiquent-ils les infections dentaires ?
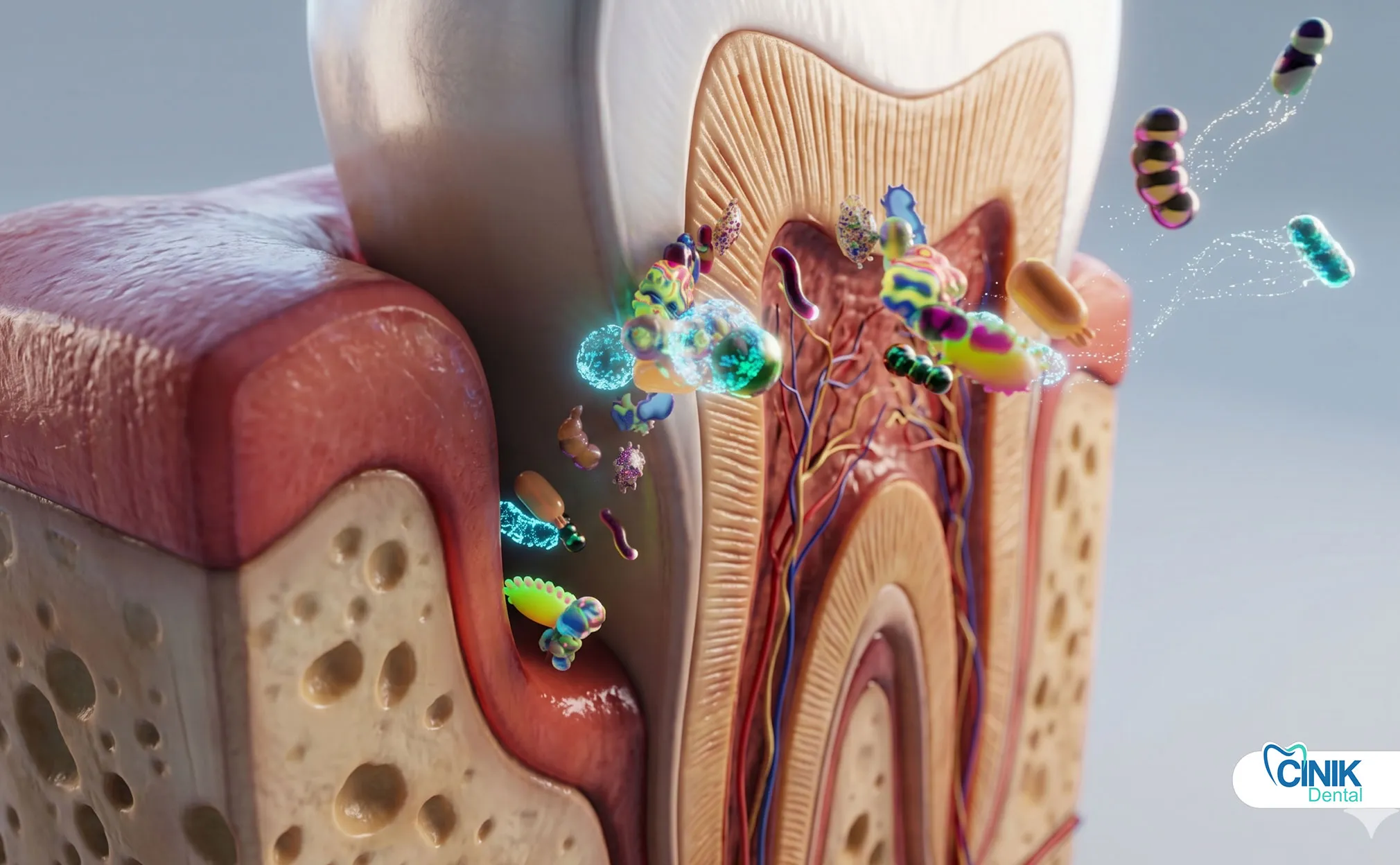
Les dentistes utilisent l'examen clinique, les symptômes du patient, l'imagerie radiographique et les tests de pulpe pour identifier le type, la gravité et l'étendue de l'infection.
Quels symptômes indiquent une infection dentaire ?
Une douleur dentaire sévère, un gonflement facial, une rougeur des gencives, une sensibilité à la température et de la fièvre indiquent une infection active nécessitant une évaluation immédiate.
La douleur sert de principal symptôme. Les dents infectées produisent une douleur profonde et lancinante que les patients décrivent comme implacable. La douleur s'intensifie avec l'exposition à la chaleur et peut brièvement diminuer avec l'application de froid en cas de pulpite précoce. Une fois que la pulpe nécrose, la sensibilité au froid disparaît mais la douleur à la pression augmente à mesure que le pus s'accumule sous la racine.
Le gonflement signale une infection avancée. Les infections précoces provoquent un gonflement des gencives intra-orales. À mesure que la pression augmente, le gonflement s'étend à la peau du visage. La peau devient rouge, chaude et tendue. Les patients peuvent signaler que le gonflement est apparu soudainement et s'est étendu au fil des heures.
Les symptômes systémiques indiquent une infection en propagation. Une fièvre supérieure à 38°C (100.4°F) suggère une mobilisation immunitaire contre une charge bactérienne significative. Un malaise, une perte d'appétit et des difficultés à ouvrir la bouche (trismus) accompagnent l'implication des espaces faciaux. Des difficultés à avaler (dysphagie) ou à respirer représentent un risque d'urgence pour les voies respiratoires.
Quels outils diagnostiques confirment les infections dentaires ?
La palpation clinique, les tests de percussion, les radiographies, les scans CBCT et les tests de vitalité pulpaire confirment la présence de l'infection, son emplacement et l'état de vitalité de la dent.
L'examen clinique fournit des indices immédiats. Les dentistes palpent les zones enflées pour évaluer la fluctuation, un gonflement mou et rempli de liquide indique une accumulation de pus. Les tests de percussion tapotent les dents avec un instrument émoussé ; les dents infectées transmettent la vibration douloureusement à travers les ligaments parodentaux enflammés. Les tests de mobilité identifient les dents avec une perte osseuse avancée due à des abcès parodentaux.
L'imagerie radiographique visualise la destruction osseuse. Les radiographies périapicales standard montrent des zones radiolucentes aux extrémités des racines indiquant une perte osseuse due à des abcès périapicaux. Les radiographies bitewing révèlent des caries profondes et des niveaux osseux parodentaux. Cependant, les radiographies 2D manquent les infections précoces et l'anatomie complexe.
La tomographie à faisceau conique (CBCT) offre une visualisation tridimensionnelle. Cette technologie détecte les abcès avant que des changements osseux visibles n'apparaissent sur les radiographies standard. Le CBCT identifie des canaux radiculaires supplémentaires, des fractures radiculaires et des schémas de propagation précis dans les espaces faciaux. Des recherches menées par Patel (2019) dans le International Endodontic Journal confirment que le CBCT détecte 40 % de lésions périapicales en plus que la radiographie conventionnelle.
Les tests de vitalité pulpaire distinguent les conditions réversibles des conditions irréversibles. Les testeurs de pulpe électrique stimulent la réponse nerveuse ; les dents non vitales ne montrent aucune sensation. Les tests à froid avec un spray réfrigérant évaluent la fonction nerveuse. Une pulpe nécrotique ne répond pas au froid, tandis qu'une pulpe vitale enflammée produit une douleur exagérée et persistante.
Quels sont les principes fondamentaux du traitement des infections dentaires ?
Éliminez d'abord la source de l'infection par drainage, traitement de canal ou extraction. Utilisez des antibiotiques uniquement lorsque l'infection se propage systématiquement. Ne comptez jamais uniquement sur les antibiotiques.
L'objectif principal du traitement des infections dentaires est le contrôle de la source. Les antibiotiques circulent dans le sang mais ne peuvent pas pénétrer dans les chambres pulpaire nécrotiques, les cavités d'abcès ou les colonies bactériennes protégées par un biofilm. La source de l'infection, une pulpe morte, du pus accumulé ou une poche parodentale malade, doit être physiquement éliminée.
Le drainage et le débridement forment la base du contrôle de la source. Une cavité d'abcès contient du pus, des toxines bactériennes et un liquide inflammatoire. L'incision et le drainage libèrent ce matériel, réduisant la pression et la charge bactérienne. La thérapie de canal radiculaire élimine le tissu pulpaire infecté de l'intérieur de la dent. L'extraction élimine toute la structure infectée.
Les approches conservatrices préservent les dents naturelles lorsque cela est possible. La thérapie de canal radiculaire sauve les dents avec des abcès périapicaux si une structure dentaire suffisante reste pour la restauration. Les abcès parodentaux répondent souvent au drainage combiné à un nettoyage en profondeur. L'extraction devient nécessaire lorsque les dents ont des fractures sous la ligne des gencives, une perte osseuse sévère, ou un échec du traitement antérieur du canal radiculaire.
Les approches chirurgicales traitent des cas complexes. L'apicoectomie, l'ablation chirurgicale de l'extrémité de la racine, sauve les dents avec une infection périapicale persistante après la thérapie de canal radiculaire. La chirurgie parodentale réduit les poches profondes qui abritent des abcès récurrents. La chirurgie en milieu hospitalier gère les infections des espaces fascials nécessitant une protection des voies respiratoires.
Aperçu clinique clé : Le traitement local prend le pas sur les antibiotiques. Un patient avec un abcès dentaire qui ne reçoit que des antibiotiques ressent un soulagement temporaire des symptômes mais fait face à une récurrence garantie. La cavité de l'abcès reste. Les bactéries se repopulent. Sans drainage ou traitement dentaire, l'infection revient, souvent avec des organismes résistants aux antibiotiques.
Quelles procédures dentaires traitent d'abord les infections ?
Les dentistes priorisent l'incision et le drainage pour les abcès, la thérapie de canal radiculaire pour les dents récupérables, et l'extraction pour les dents non restaurables. Ces procédures éliminent directement les sources d'infection.
Comment fonctionne le drainage d'un abcès ?
Le dentiste anesthésie la zone, fait une petite incision dans l'abcès et permet au pus de s'écouler. Cela réduit immédiatement la douleur et la pression tout en éliminant la charge bactérienne.
L'incision et le drainage fournissent le soulagement de douleur le plus rapide pour les abcès aigus. La procédure nécessite une anesthésie locale. Le dentiste identifie la zone de gonflement la plus fluctuant (la plus douce, la plus remplie de liquide). Une incision au scalpel, typiquement de 1 à 2 centimètres, pénètre jusqu'à la cavité de l'abcès. Le pus s'évacue sous pression. Le dentiste peut insérer un petit drain en caoutchouc pour maintenir l'ouverture pendant 24 à 48 heures.
Les avantages immédiats incluent la réduction de la pression et le soulagement de la douleur. Les patients rapportent souvent une amélioration spectaculaire en quelques heures. Le drainage élimine également l'inoculum bactérien, réduisant la charge bactérienne systémique. La procédure prend 15 à 30 minutes dans un cabinet dentaire.
Les soins post-drainage impliquent des rinçages à l'eau salée tiède pour maintenir la perméabilité du drain. Les patients continuent les antibiotiques si des symptômes systémiques existent. Un traitement dentaire définitif, canal radiculaire ou extraction, suit une fois le gonflement aigu diminué, généralement dans les 3 à 7 jours.
Quand la thérapie de canal radiculaire sauve-t-elle une dent infectée ?
La thérapie de canal radiculaire élimine la pulpe infectée, désinfecte les canaux radiculaires et scelle la dent. Elle préserve les dents naturelles lorsque suffisamment de structure reste pour la restauration de la couronne.
La thérapie de canal radiculaire traite les abcès périapicaux en éliminant le contenu de la chambre pulpaire infectée. Le dentiste crée une ouverture d'accès à travers la couronne de la dent. Des instruments retirent le tissu pulpaire, les débris nécrotiques et le biofilm bactérien du système canalaire. Des irrigants chimiques, l'hypochlorite de sodium et la chlorhexidine, désinfectent les parois du canal.
La procédure nécessite 1 à 3 rendez-vous en fonction de la gravité de l'infection. La première visite se concentre sur l'élimination de la pulpe et le drainage de l'abcès à travers la dent. Le dentiste place un médicament antibactérien à l'intérieur du canal et scelle un remplissage temporaire. La deuxième visite confirme le contrôle de l'infection avant de remplir les canaux avec de la gutta-percha, un matériau semblable au caoutchouc. Une couronne permanente restaure la force de la dent.
Les taux de réussite dépassent 90 % pour les traitements de canal radiculaire primaires. Des recherches menées par Ng (2011) dans le International Endodontic Journal rapportent 94 % de survie à 4 ans pour les dents avec des abcès périapicaux traités par thérapie de canal radiculaire et restauration de couronne. L'échec provient généralement de branches de canal manquées, de biofilm bactérien persistant ou de fuites coronaires.
Quand une dent infectée doit-elle être extraite ?
L'extraction devient nécessaire lorsque les dents présentent des fractures sous la ligne des gencives, une perte osseuse sévère, un échec de retraitement du canal radiculaire, ou une structure insuffisante pour la restauration.
L'extraction dentaire permet d'éliminer définitivement l'infection lorsque la préservation est impossible. Les fractures radiculaires verticales, qui s'étendent sous la ligne des gencives, empêchent l'étanchéité bactérienne quelle que soit le traitement. Une maladie parodontal sévère détruisant plus de 50 % de l'os de soutien rend les dents non restaurables. Un échec de retraitement du canal radiculaire, en particulier avec des lésions périapicales persistantes, peut justifier une extraction et un remplacement par implant.
La procédure d'extraction pour les dents infectées nécessite des précautions pour prévenir la propagation bactérienne. Le dentiste peut prescrire des antibiotiques préopératoires pour les patients immunodéprimés ou en cas d'infections sévères. L'anesthésie locale avec vasoconstricteur contrôle les saignements. Le dentiste élève la dent de son alvéole, retire le tissu de granulation de la base de l'alvéole et s'assure d'un débridement complet.
La guérison post-extraction prend 1 à 2 semaines pour la fermeture des tissus mous. Le remodelage osseux se poursuit pendant 3 à 6 mois. Le placement immédiat d'implants, effectué dans des cas sélectionnés, réduit le temps de traitement mais nécessite des sites d'extraction sans infection.
Note basée sur des preuves : Les procédures dentaires définitives restent essentielles car les antibiotiques ne peuvent pas éliminer les sources d'infection. Une revue systématique par Cope (2014) dans le British Dental Journal a analysé 22 essais cliniques et a conclu que les antibiotiques sans contrôle de la source n'apportent aucun bénéfice durable pour les abcès dentaires. La récurrence des symptômes se produit dans 100 % des cas dans les semaines qui suivent.
Procédure | Indication | Taux de réussite | Temps de récupération |
Incision et drainage | Abcès aigu avec gonflement fluctuant | Soulagement immédiat ; nécessite un suivi | 2-3 jours |
Thérapie de canal radiculaire | Abcès périapical, dent restaurable | 90-95 % à 5 ans | 1-2 semaines |
Extraction dentaire | Dent non restaurable, traitement échoué | 100 % d'élimination de l'infection | 1-2 semaines tissus mous |
Comment les antibiotiques soutiennent-ils le traitement des infections dentaires ?
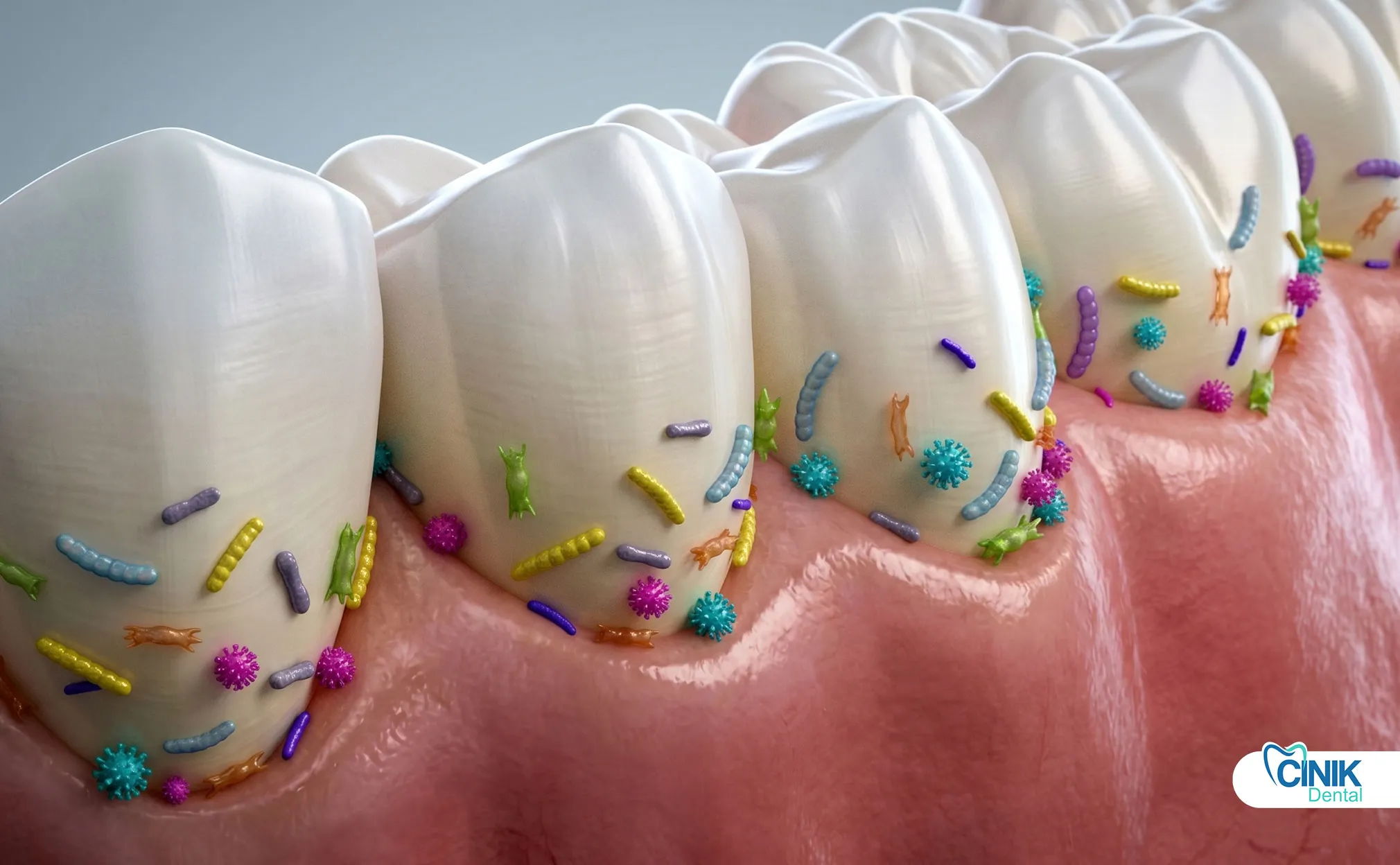
Les antibiotiques traitent les infections qui se propagent avec fièvre, cellulite faciale ou immunodépression. Ils ne remplacent jamais le drainage ou le traitement dentaire. L'amoxicilline reste le choix de première ligne.
Quand les dentistes prescrivent-ils des antibiotiques ?
Les dentistes prescrivent des antibiotiques pour des symptômes systémiques, une cellulite qui se propage, des patients immunodéprimés, ou lorsque des procédures dentaires immédiates sont impossibles.
Les antibiotiques jouent un rôle d'adjuvant dans la gestion des infections dentaires. Ils ne guérissent pas les abcès dentaires. Ils contrôlent la propagation bactérienne lorsque l'infection dépasse la capacité de confinement local. Les indications spécifiques incluent :
Implication systémique : Une fièvre supérieure à 38°C, un malaise ou une lymphadénopathie indiquent une charge bactérienne dépassant la capacité immunitaire locale. Les antibiotiques réduisent le risque de bactériémie et soutiennent la récupération systémique.
Infection en propagation : La cellulite, une rougeur diffuse de la peau sans abcès localisé, nécessite des antibiotiques car le drainage n'est pas possible. Les infections s'étendant dans les espaces fasciaux nécessitent une couverture antibiotique agressive en attendant une intervention chirurgicale.
États immunodéprimés : Les patients atteints de diabète, de VIH, sous chimiothérapie ou ayant subi des greffes d'organes font face à un risque accru de sepsis. Une intervention antibiotique précoce protège ces populations vulnérables.
Prophylaxie procédurale : Certaines conditions médicales nécessitent une couverture antibiotique avant les procédures dentaires pour prévenir l'infection à distance. Les valves cardiaques prothétiques, l'endocardite infectieuse antérieure et certains implants orthopédiques entrent dans cette catégorie.
Principe important : Les antibiotiques sont adjuvants, pas une thérapie primaire. Un patient avec un abcès dentaire localisé et sans symptômes systémiques n'a pas besoin d'antibiotiques. Le dentiste effectue le drainage et le traitement dentaire. Ajouter des antibiotiques n'apporte aucun bénéfice et contribue à la résistance.
Quels antibiotiques fonctionnent le mieux pour les infections dentaires ?
L'amoxicilline reste l'antibiotique de première intention en raison de son efficacité contre les pathogènes buccaux typiques et de son excellente tolérance. La pénicilline V sert d'alternative.
L'amoxicilline domine la prescription d'antibiotiques dentaires de première intention. Cette aminopénicilline couvre les cocci gram-positifs (Streptococcus espèces) et les anaérobies gram-négatifs (Prevotella, Fusobacterium) qui causent la plupart des infections dentaires. L'absorption orale atteint 90 %, produisant des niveaux sanguins fiables. La dose standard pour un adulte est de 500 mg trois fois par jour pendant 5 à 7 jours.
Preuves cliniques : Un essai contrôlé randomisé par Matthews (2016) dans le Journal of Antimicrobial Chemotherapy a comparé l'amoxicilline avec un placebo pour les abcès dentaires. Les deux groupes ont reçu une incision et un drainage. L'amoxicilline a réduit le gonflement post-procédure de 35 % et a raccourci la récupération de 2 jours. Cependant, les taux de guérison à 30 jours étaient identiques, confirmant que le contrôle de la source, et non les antibiotiques, détermine les résultats.
La pénicilline V offre une alternative avec un spectre plus étroit. Cette phénoxyméthylpénicilline résiste à la dégradation par l'acide gastrique, ce qui la rend adaptée à une utilisation orale. La dose typique est de 500 mg quatre fois par jour. La pénicilline V couvre la plupart des pathogènes odontogènes mais manque de couverture contre les anaérobies gram-négatifs par rapport à l'amoxicilline.
Quels antibiotiques aident lorsque les médicaments de première intention échouent ?
Le métronidazole cible les anaérobies et se combine avec l'amoxicilline pour les infections sévères. La clindamycine remplace la pénicilline chez les patients allergiques. L'azithromycine offre une autre alternative.
Le métronidazole cible spécifiquement les bactéries anaérobies obligatoires. Ces organismes dominent la pulpe nécrotique et les poches parodontales profondes. Le métronidazole seul ne couvre pas les streptocoques aérobies, donc les dentistes l'associent souvent à l'amoxicilline pour les infections sévères et mixtes. La dose est de 400 mg trois fois par jour. Les patients doivent éviter l'alcool pendant le traitement et pendant 48 heures après la fin en raison de réactions similaires au disulfirame.
La clindamycine sert les patients allergiques à la pénicilline. Cet antibiotique lincosamide couvre efficacement les organismes gram-positifs et les anaérobies. La dose est de 300 mg quatre fois par jour. Les dentistes réservent la clindamycine aux véritables allergies à la pénicilline car elle présente un risque plus élevé de Clostridioides difficile colite, une infection intestinale grave.
L'azithromycine fournit une autre alternative pour les patients allergiques à la pénicilline. Cet antibiotique macrolide offre un dosage pratique, 500 mg par jour pendant 3 jours, en raison de sa longue demi-vie tissulaire. Cependant, la résistance croissante parmi les streptocoques oraux limite sa fiabilité. Les dentistes utilisent l'azithromycine lorsque la clindamycine est contre-indiquée.
Pourquoi la résistance aux antibiotiques menace-t-elle le traitement dentaire ?
La prescription excessive d'antibiotiques dentaires accélère la résistance bactérienne. Les directives découragent désormais l'utilisation systématique d'antibiotiques pour les infections localisées sans propagation systémique.
La résistance aux antibiotiques sape la gestion des infections dentaires. Les Centers for Disease Control and Prevention identifient la prescription dentaire comme un contributeur significatif à l'utilisation inutile d'antibiotiques. Des études estiment que 30 à 50 % des prescriptions d'antibiotiques dentaires sont inutiles, données pour des conditions où le contrôle de la source suffit.
Les conséquences vont au-delà des patients individuels. Les bactéries résistantes colonisent la cavité buccale et se propagent aux membres de la famille, aux établissements de santé et aux communautés. Des souches de Streptococcus pneumoniae et de Staphylococcus aureus résistantes à la pénicilline et à la clindamycine apparaissent de plus en plus dans les infections dentaires.
Les programmes de gestion des antibiotiques ciblent la prescription excessive dentaire. L'American Dental Association a mis à jour les directives en 2019, déclarant explicitement que les antibiotiques ne sont pas indiqués pour les gonflements intra-oraux localisés sans implication systémique. Les directives soulignent : "La méthode principale pour traiter une infection dentaire devrait être le contrôle de la source."
La thérapie ciblée remplace la prescription empirique dans les cas récurrents ou complexes. La culture et le test de sensibilité identifient des bactéries spécifiques et leurs schémas de résistance. Cette approche, standard dans les milieux hospitaliers, devient de plus en plus courante dans la pratique dentaire pour les patients immunodéprimés ou en cas d'échecs de traitement.
Antibiotique | Spectre | Dose typique | Meilleur pour |
Amoxicilline | Large (aérobes + anaérobies) | 500 mg TID x 5-7 jours | Première ligne, la plupart des infections |
Pénicilline V | Étroit (aérobes) | 500 mg QID x 5-7 jours | Infections légères, préférence pour la pénicilline |
Métronidazole | Anaérobies uniquement | 400 mg TID x 5-7 jours | Associé à l'amoxicilline pour les cas graves |
Clindamycine | Aérobes + anaérobies | 300 mg QID x 5-7 jours | Allergie à la pénicilline |
Azithromycine | Large | 500 mg par jour x 3 jours | Allergie à la pénicilline, clindamycine contre-indiquée |
Comment les dentistes gèrent-ils la douleur lors du traitement des infections ?
Les AINS comme l'ibuprofène offrent un soulagement de la douleur dentaire supérieur par rapport aux opioïdes. Le paracétamol constitue une alternative pour les patients qui ne peuvent pas prendre d'AINS. L'anesthésie locale pendant les procédures élimine la douleur procédurale.
La gestion de la douleur dans les infections dentaires suit une approche multimodale. Les anti-inflammatoires non stéroïdiens (AINS) en sont la pierre angulaire. L'ibuprofène, 400-600 mg toutes les 6-8 heures, réduit l'inflammation au site de l'infection tout en fournissant une analgésie. Les recherches de Moore (2015) dans la Base de données Cochrane des revues systématiques confirment que l'ibuprofène 400 mg offre un meilleur soulagement de la douleur que la codéine 60 mg pour la douleur dentaire, avec moins d'effets secondaires.
Le paracétamol (acétaminophène) sert les patients avec des contre-indications aux AINS, une maladie ulcéreuse peptique, une thérapie anticoagulante ou une insuffisance rénale. La dose est de 500-1000 mg toutes les 6 heures, sans dépasser 3000 mg par jour. Le paracétamol n'a pas d'action anti-inflammatoire mais fournit une analgésie efficace.
La thérapie combinée améliore le contrôle de la douleur. L'alternance entre l'ibuprofène et le paracétamol maintient des niveaux de médicaments stables. Certaines études suggèrent que l'administration simultanée offre un soulagement supérieur à celui de chaque médicament seul, bien que les patients doivent suivre attentivement les intervalles de dosage pour éviter le surdosage.
La prescription d'opioïdes a considérablement diminué dans la pratique dentaire. L'épidémie d'opioïdes a incité à réévaluer les protocoles de douleur dentaire. Les directives actuelles réservent les opioïdes pour les douleurs post-chirurgicales sévères non réactives aux AINS. Lorsqu'ils sont prescrits, les dentistes limitent les quantités à 3-5 jours et les combinent avec des AINS pour réduire les besoins en opioïdes.
Les mesures de soins de soutien complètent les médicaments. L'hydratation maintient le flux de salive et soutient la fonction immunitaire. Les rinçages à l'eau salée tiède (une demi-cuillère à café de sel dans de l'eau tiède, agité pendant 30 secondes) réduisent la charge bactérienne et favorisent le drainage des poches gingivales. Les aliments mous préviennent l'irritation mécanique des tissus infectés. L'élévation de la tête pendant le sommeil réduit le flux sanguin vers les tissus faciaux enflés, diminuant ainsi la douleur lancinante.
Que se passe-t-il lorsque les infections dentaires ne sont pas traitées ?
Les infections dentaires non traitées provoquent une destruction osseuse locale, une nécrose tissulaire et des complications systémiques potentiellement fatales, y compris la septicémie, l'obstruction des voies respiratoires et l'abcès cérébral.
Quels dommages locaux les infections non traitées causent-elles ?
Les infections non traitées détruisent l'os de la mâchoire (ostéomyélite), tuent le tissu mou (nécrose) et se propagent à travers les espaces faciaux, provoquant déformation et perte fonctionnelle.
L'ostéomyélite représente une infection osseuse due à une contamination bactérienne. L'os de la mâchoire développe des zones d'os mort (séquestres) entourées de tissu enflammé. L'ostéomyélite chronique cause des douleurs persistantes, des fistules drainantes et des fractures pathologiques. Le traitement nécessite des antibiotiques prolongés (4-6 semaines) et l'ablation chirurgicale de l'os mort. La thérapie à l'oxygène hyperbare soutient la guérison dans les cas réfractaires.
La nécrose tissulaire se produit lorsque l'infection compromet l'apport sanguin. Le palais, la langue ou la peau faciale peuvent développer des zones noires et dévitalisées nécessitant un débridement chirurgical. La fasciite nécrosante, bien que rare dans les infections dentaires, détruit rapidement les plans tissulaires et nécessite une intervention chirurgicale d'urgence.
Les infections des espaces faciaux déforment l'anatomie. Les espaces submandibulaires, ptérygomandibulaires et canins gonflent de manière spectaculaire. Les patients développent une apparence de "cou de taureau" en raison de l'implication bilatérale submandibulaire. Le trismus, le blocage de la mâchoire dû à l'inflammation musculaire, empêche de manger et de parler.
Quels risques systémiques les infections dentaires créent-elles ?
Les bactéries des infections dentaires pénètrent dans la circulation sanguine, provoquant une septicémie, une infection des valves cardiaques et des abcès distants. L'obstruction des voies respiratoires due au gonflement du cou peut provoquer une suffocation.
La septicémie représente la complication systémique la plus redoutée. Les toxines bactériennes déclenchent une activation massive du système immunitaire. La fièvre, le rythme cardiaque rapide, la respiration rapide et la confusion signalent une septicémie. La pression artérielle chute. Les organes échouent. Le choc septique entraîne une mortalité de 40 % même avec un traitement en soins intensifs. Les infections dentaires causent 10-15 % de tous les cas de septicémie faciale.
L'obstruction des voies respiratoires menace la vie en quelques heures. L'angine de Ludwig, une infection bilatérale de l'espace submandibulaire, pousse la langue vers le haut et vers l'arrière. Le plancher de la bouche devient rigide. Les patients bavent, ne peuvent pas avaler leur salive et développent un stridor (respiration bruyante). Une trachéostomie d'urgence ou une intubation sécurise les voies respiratoires avant le drainage chirurgical.
L'abcès cérébral, bien que rare, suit une propagation hématogène ou une extension directe à travers les os du crâne. Les infections des dents antérieures atteignent le lobe frontal. Les infections maxillaires atteignent le lobe temporal. Les abcès cérébraux provoquent des maux de tête, des convulsions, une faiblesse focale et un état mental altéré. Le drainage neurochirurgical et des antibiotiques prolongés (6-8 semaines) traitent cette complication.
L'endocardite affecte les valves cardiaques, en particulier chez les patients ayant une maladie valvulaire préexistante ou des valves prothétiques. Streptocoques viridans provenant d'infections dentaires adhèrent à l'endocarde endommagé, formant des végétations qui embolisent vers le cerveau, les reins et les membres. Des antibiotiques prophylactiques avant les procédures dentaires préviennent cette complication chez les patients à haut risque.
Complication | Mécanisme | Risque de mortalité | Traitement requis |
Ostéomyélite | Infection osseuse et nécrose | Faible | Chirurgie + 4-6 semaines d'antibiotiques |
Sepsis | Propagation bactérienne dans le sang | 15-40% | Soins en soins intensifs, antibiotiques IV, contrôle de la source |
Angine de Ludwig | Infection submandibulaire bilatérale | 10-20% | Voie aérienne d'urgence + drainage chirurgical |
Abcès cérébral | Propagation hématogène ou directe | 10-30% | Neurochirurgie + 6-8 semaines d'antibiotiques |
Comment les populations spéciales devraient-elles recevoir des soins pour les infections dentaires ?
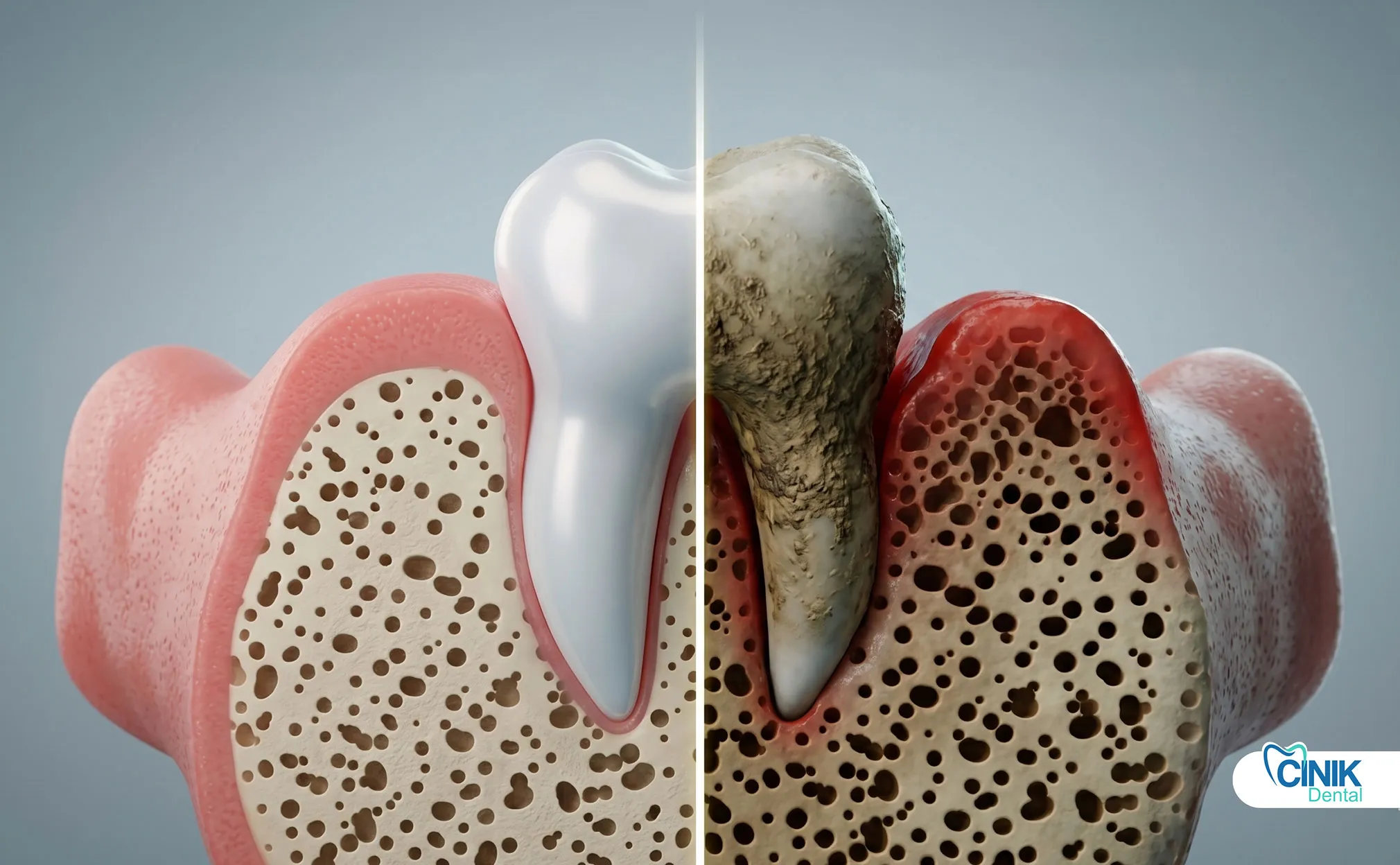
Les patients immunodéprimés, pédiatriques et âgés ont besoin d'approches de traitement modifiées, d'une intervention antibiotique précoce, d'un ajustement des doses de médicaments et d'une surveillance plus étroite.
Quels soins supplémentaires les patients immunodéprimés nécessitent-ils ?
Les patients immunodéprimés font face à un risque plus élevé de propagation systémique. Ils ont besoin d'un début d'antibiotiques plus précoce, d'une couverture plus large, d'un traitement en milieu hospitalier pour les infections modérées et d'une surveillance de récupération plus longue.
Les états immunodéprimés incluent le diabète sucré, le VIH/SIDA, la chimiothérapie, la transplantation d'organes, l'utilisation chronique de corticostéroïdes et les déficiences immunitaires héréditaires. Ces conditions altèrent la fonction des neutrophiles, la production d'anticorps ou l'immunité médiée par les cellules, défenses critiques contre les agents pathogènes dentaires.
Un risque plus élevé de propagation des infections exige une gestion agressive. Un abcès localisé chez un patient en bonne santé peut rester confiné pendant des jours. Le même abcès chez un patient chimiothérapeutique neutropénique peut progresser vers une septicémie en quelques heures. Les dentistes abaissent les seuils pour l'initiation des antibiotiques et le renvoi à l'hôpital.
L'intervention antibiotique précoce utilise une couverture à large spectre. Alors que les patients en bonne santé reçoivent de l'amoxicilline seule, les patients immunodéprimés peuvent avoir besoin d'amoxicilline-clavulanate (Augmentin) pour une couverture anaérobie améliorée, ou même d'antibiotiques intraveineux pour une admission à l'hôpital.
Le traitement en milieu hospitalier devient nécessaire pour les infections qui seraient gérées en cabinet chez des patients en bonne santé. L'accès IV permet une administration fiable des médicaments. La surveillance suit la température, les numérations de globules blancs et les marqueurs inflammatoires. Les équipes chirurgicales sont prêtes pour la gestion des voies respiratoires si une implication de l'espace fascial se développe.
Comment les dentistes ajustent-ils le traitement pour les enfants et les patients âgés ?
Les enfants nécessitent un dosage basé sur le poids et une gestion du comportement. Les patients âgés ont besoin d'une évaluation de la fonction rénale, d'un examen des interactions médicamenteuses et d'une prise en compte des comorbidités.
Les infections dentaires pédiatriques présentent des défis uniques. Les dents primaires avec des abcès périapicaux nécessitent souvent une extraction plutôt qu'une thérapie de canal radiculaire en raison de l'anatomie complexe des racines et de l'échéance d'exfoliation approchante. Les mainteneurs d'espace préviennent les complications orthodontiques après une perte prématurée de dents. Le dosage des antibiotiques suit des calculs basés sur le poids, amoxicilline 50 mg/kg/jour divisée en 3 doses.
La gestion du comportement permet un traitement chez les jeunes patients. L'anesthésie locale nécessite une technique soignée pour éviter l'injection intravasculaire chez les petits patients. La sédation ou l'anesthésie générale peut être nécessaire pour des procédures étendues. Les parents jouent des rôles cruciaux dans les soins post-traitement, garantissant la conformité aux médicaments et les modifications alimentaires.
Les patients gériatriques présentent différentes complexités. La polypharmacie augmente les risques d'interaction médicamenteuse. Les antibiotiques peuvent interagir avec la warfarine (la clindamycine et le métronidazole potentialisent les effets), les statines ou les médicaments cardiaques. Le déclin de la fonction rénale nécessite des ajustements de dose pour les médicaments éliminés par les reins comme l'amoxicilline et le métronidazole.
L'altération cognitive complique le rapport des symptômes. Les patients âgés atteints de démence peuvent ne pas communiquer efficacement la douleur. Les soignants doivent observer les changements de comportement, le refus de nourriture, le toucher du visage ou l'agitation, comme indicateurs d'infection. La planification du traitement privilégie la simplicité et la durabilité plutôt que des approches idéalistes.
Population | Considération clé | Ajustement des antibiotiques | Besoins spéciaux |
Immunodéprimé | Risque de propagation élevé | Spectre plus large, début plus précoce | Seuil de référence à l'hôpital abaissé |
Pédiatrique | Croissance et développement | Dosage basé sur le poids | Gestion du comportement, maintien de l'espace |
Gériatrique | Comorbidités, polypharmacie | Ajustement de dose rénal | Revue des interactions médicamenteuses, évaluation cognitive |
Comment les gens peuvent-ils prévenir les infections dentaires ?
Le brossage et le fil dentaire quotidiens, des contrôles dentaires réguliers tous les 6 mois, un traitement rapide des caries et la gestion des maladies des gencives préviennent les conditions qui mènent aux infections dentaires.
La prévention des infections dentaires cible les causes profondes : la carie dentaire et la maladie parodontal. Les pratiques d'hygiène buccale perturbent la formation du biofilm bactérien avant qu'il ne cause des dommages aux tissus. L'American Dental Association recommande de se brosser les dents deux fois par jour avec un dentifrice fluoré pendant 2 minutes, en utilisant une brosse à poils souples en mouvements circulaires doux au niveau de la ligne des gencives.
Le fil dentaire atteint des zones que les brosses manquent, entre les dents et en dessous des marges gingivales où les pathogènes parodontaux se colonisent. Les irrigateurs dentaires et les brosses interdentaires aident les patients ayant une dextérité manuelle limitée. Les bains de bouche contenant de la chlorhexidine ou des huiles essentielles réduisent la charge bactérienne mais ne remplacent pas le nettoyage mécanique.
Des contrôles dentaires réguliers permettent une intervention précoce. Les nettoyages professionnels éliminent le tartre qui abrite des bactéries. Les examens détectent les caries avant qu'elles n'atteignent la pulpe. Les radiographies bitewing identifient les caries interproximales invisibles à l'inspection visuelle. L'intervalle de rappel de 6 mois convient à la plupart des patients, bien que ceux présentant un risque élevé de caries ou une maladie parodontal active puissent avoir besoin d'intervalles de 3 à 4 mois.
Un traitement précoce des caries prévient l'infection de la pulpe. Les petites caries nécessitent des plombages simples. Un retard permet à la carie de s'aggraver, nécessitant finalement un traitement de canal ou une extraction. Les scellants dentaires sur les dents postérieures protègent les enfants et les adolescents de la carie de surface occlusale.
La gestion des maladies parodontales prévient les abcès parodontaux. Le détartrage et le surfaçage radiculaire (nettoyage en profondeur) éliminent le tartre des surfaces radiculaires. L'entretien parodontal tous les 3 mois contrôle la progression de la maladie. La réduction chirurgicale des poches élimine les espaces profonds où se forment les abcès.
Les modifications alimentaires soutiennent la prévention. Limiter l'exposition au sucre, en particulier les collations fréquentes et les boissons sucrées, réduit la production d'acide par Streptococcus mutans. Mâcher du chewing-gum sans sucre stimule le flux salivaire, qui neutralise l'acide et reminéralise l'émail. L'eau fluorée renforce la structure dentaire contre les attaques acides.
Quelle est la récupération attendue après le traitement d'une infection dentaire ?
La douleur s'améliore dans les 24 à 48 heures suivant le contrôle de la source. Les tissus mous guérissent en 1 à 2 semaines. La guérison osseuse prend 3 à 6 mois. Une intervention précoce produit une récupération plus rapide et plus complète.
Les délais de guérison attendus varient selon la procédure et la gravité de l'infection. Le drainage d'un abcès aigu produit un soulagement immédiat de la douleur. Le gonflement diminue en 2 à 3 jours. La petite incision guérit en une semaine. Cependant, la dent sous-jacente nécessite toujours un traitement définitif pour prévenir la récurrence.
La récupération après un traitement de canal suit un schéma prévisible. La douleur post-opératoire dure 2-3 jours, gérable avec des AINS. L'os périapical commence à guérir en quelques semaines, bien que le remplissage osseux radiographique complet nécessite 6-12 mois. La pose de la couronne finale, 2-4 semaines après l'achèvement du traitement de canal, restaure la fonction et prévient la fracture.
Les sites d'extraction guérissent par étapes. La formation de caillots sanguins se produit immédiatement. Les tissus mous se ferment en 1-2 semaines. L'os remplit l'alvéole en 3-6 mois. La pose de l'implant, lorsqu'elle est prévue, se fait généralement 3-4 mois après l'extraction pour permettre la guérison osseuse initiale.
Une intervention précoce améliore considérablement les résultats. Un abcès périapical traité dans les jours suivant l'apparition des symptômes répond à un simple traitement de canal. Un retard de plusieurs semaines permet à la destruction osseuse de s'étendre, compliquant le traitement et réduisant la probabilité de survie de la dent. Les abcès parodentaux traités rapidement préservent les dents ; un traitement retardé entraîne souvent un pronostic désespéré nécessitant une extraction.
Les facteurs affectant les résultats incluent la conformité du patient, l'état immunitaire et le suivi des soins définitifs. Les patients qui terminent les traitements antibiotiques prescrits et reviennent pour les procédures définitives programmées obtiennent de meilleurs résultats. Le tabagisme nuit à la guérison en réduisant le flux sanguin et la fonction immunitaire. Le diabète nécessite un contrôle glycémique pour une récupération optimale.
Quelles avancées façonnent le traitement futur des infections dentaires ?
De nouveaux peptides antimicrobiens ciblent les biofilms sans résistance. La désinfection assistée par laser améliore la stérilisation des canaux radiculaires. La médecine personnalisée utilise des tests génétiques pour prédire le risque d'infection et la réponse au traitement.
Les avancées en thérapie antimicrobienne s'attaquent à la résistance des biofilms. Les antibiotiques traditionnels échouent contre les bactéries protégées par biofilm. Les chercheurs développent des peptides antimicrobiens, de courts fragments de protéines qui perturbent les membranes bactériennes sans développement de résistance. Ces peptides, dérivés de molécules immunitaires naturelles, montrent un potentiel en tant qu'irrigants de canal radiculaire et traitements topiques.
La thérapie photodynamique utilise des colorants activés par la lumière pour tuer les bactéries. Le dentiste applique un agent photosensibilisant sur la zone infectée, puis l'expose à des longueurs d'onde lumineuses spécifiques. Les espèces réactives de l'oxygène détruisent les membranes et l'ADN bactérien. Cette technique stérilise les systèmes de canaux radiculaires et les poches parodontales sans antibiotiques.
Les techniques mini-invasives préservent la structure dentaire. La technologie GentleWave utilise de l'énergie multisonique et une dynamique des fluides avancée pour désinfecter l'anatomie complexe des canaux radiculaires avec un minimum d'instrumentation. Le traitement de canal assisté par laser vaporise les tissus infectés et stérilise simultanément les parois du canal.
Les soins dentaires personnalisés tirent parti de l'analyse génétique et du microbiome. Les tests génétiques identifient les patients présentant des déficiences immunitaires innées prédisposant à des infections sévères. Le profilage du microbiome oral prédit le risque de maladie parodontal et guide la thérapie probiotique ciblée. La pharmacogénomique détermine la sélection optimale des antibiotiques en fonction du métabolisme individuel.
L'endodontie régénérative représente un changement de paradigme. Au lieu d'enlever la pulpe et de remplir les canaux avec un matériau inerte, cette approche encourage la régénération du tissu pulpaire en utilisant des cellules souches et des facteurs de croissance. Les dents immatures avec des pulpes infectées peuvent continuer leur développement radiculaire, produisant des dents plus fortes et plus durables. Les recherches de Galler (2021) dans le Journal of Endodontics démontrent une maturation radiculaire continue dans 80 % des dents permanentes immatures traitées.
Questions Fréquemment Posées Sur le Traitement des Infections Dentaires
Toutes les Infections Dentaires Nécessitent-elles des Antibiotiques ?
Non. Les abcès dentaires localisés sans fièvre ni gonflement facial nécessitent uniquement un contrôle de la source, un drainage, un traitement de canal ou une extraction. Les antibiotiques n'aident que lorsque l'infection se propage systématiquement.
La misconception selon laquelle chaque infection dentaire nécessite des antibiotiques entraîne une surprescription. Les directives cliniques de l'American Dental Association et du British National Institute for Health and Care Excellence stipulent explicitement que les antibiotiques ne sont pas nécessaires pour la plupart des infections dentaires localisées. Les procédures de contrôle de la source éliminent directement l'infection. Ajouter des antibiotiques n'apporte aucun bénéfice et contribue à la résistance.
Les antibiotiques deviennent nécessaires lorsque les patients montrent une implication systémique. Fièvre, malaise, lymphadénopathie ou cellulite en expansion indiquent une charge bactérienne dépassant la contenance locale. Les patients immunodéprimés peuvent avoir besoin d'un début d'antibiotiques plus précoce. Lorsque les dentistes ne peuvent pas effectuer un contrôle immédiat de la source en raison de problèmes d'accès au patient, les antibiotiques servent de ponts temporaires vers des soins définitifs.
Combien de Temps Prend le Traitement des Infections Dentaires ?
Le drainage des abcès aigus fournit un soulagement immédiat. La thérapie de canal nécessite 1 à 3 rendez-vous sur 1 à 2 semaines. L'extraction guérit en 1 à 2 semaines. Les traitements antibiotiques durent 5 à 7 jours.
La durée du traitement dépend de la gravité de l'infection et de l'approche choisie. Le drainage simple d'un abcès prend 30 minutes dans le cabinet dentaire. La douleur s'améliore en quelques heures. Cependant, le patient doit revenir pour un traitement dentaire définitif dans les jours qui suivent pour prévenir la récurrence.
La thérapie de canal s'étend généralement sur deux rendez-vous. La première visite enlève la pulpe infectée et place un médicament antibactérien. La deuxième visite, 1 à 2 semaines plus tard, remplit et scelle les canaux. Un troisième rendez-vous place la couronne permanente 2 à 4 semaines plus tard. Temps total de traitement : 4 à 8 semaines pour une restauration complète.
L'extraction fournit la solution définitive la plus rapide. La procédure prend 20 à 40 minutes. Les tissus mous guérissent en 1 à 2 semaines. Si un remplacement par implant est prévu, le délai s'étend à 3 à 6 mois pour la guérison osseuse avant la pose de l'implant.
Les traitements antibiotiques restent courts. Cinq à sept jours suffisent pour les infections dentaires, contrairement aux traitements prolongés nécessaires pour les infections des tissus profonds ou osseuses. Les patients doivent terminer le traitement complet même si les symptômes s'améliorent plus tôt pour prévenir la récurrence et la résistance.
Les infections dentaires peuvent-elles guérir d'elles-mêmes ?
Non. Les infections dentaires nécessitent une intervention professionnelle. Le corps ne peut pas éliminer les sources d'infection à l'intérieur des dents ou des cavités d'abcès. Un traitement retardé augmente le risque de complications.
Occasionnellement, un abcès se rompt spontanément, drainant du pus et soulageant temporairement la pression. Les patients peuvent interpréter cela comme une "guérison". Cependant, la source de l'infection, la pulpe nécrotique, la carie profonde ou la poche parodontal, demeure. Les bactéries se réinstallent. L'abcès récidive, souvent avec des organismes plus résistants.
L'environnement clos d'une racine dentaire ou d'une cavité d'abcès empêche l'accès du système immunitaire. Les neutrophiles et les anticorps ne peuvent pas pénétrer efficacement dans les tissus nécrotiques ou le pus épais. Les antibiotiques circulant dans le sang ne peuvent pas atteindre les bactéries dans ces espaces avasculaires. Seule l'élimination mécanique, le drainage, le traitement de canal ou l'extraction élimine l'infection.
Rares sont les infections chroniques de bas grade qui persistent pendant des mois sans symptômes aigus. Ces infections "silencieuses" détruisent néanmoins l'os et libèrent des médiateurs inflammatoires dans la circulation sanguine. Elles contribuent à des problèmes de santé systémiques sans provoquer de douleur notable. Des radiographies dentaires régulières détectent ces infections cachées.
Quand une personne doit-elle demander des soins d'urgence pour une infection dentaire ?
Demandez des soins d'urgence en cas de difficulté à respirer ou à avaler, de gonflement facial se propageant rapidement, de fièvre supérieure à 39°C (102°F), de confusion ou d'implication oculaire due à des infections dentaires supérieures.
Les signes d'alerte d'urgence indiquent une progression mettant en danger la vie. Un compromis des voies respiratoires dû à un gonflement sous-mandibulaire ou du plancher de la bouche nécessite une évaluation immédiate aux urgences. Les patients qui ne peuvent pas avaler leur propre salive, qui développent une respiration bruyante (stridor) ou qui sentent leur gorge se fermer ont besoin d'une gestion d'urgence des voies respiratoires.
Une cellulitis se propageant rapidement, un gonflement qui s'étend visiblement en quelques heures, suggère une souche bactérienne agressive ou une immunité compromise. Des antibiotiques IV et un drainage chirurgical possible deviennent nécessaires. Un gonflement facial traversant la ligne médiane ou impliquant les deux côtés indique une propagation bilatérale.
La toxicité systémique signale une septicémie. Une forte fièvre, un rythme cardiaque rapide (plus de 100 battements par minute), une respiration rapide (plus de 20 respirations par minute) et un état mental altéré nécessitent des soins d'urgence. Ces patients ont besoin de cultures sanguines, de liquides IV et d'antibiotiques à large spectre dans un cadre de soins intensifs.
L'implication oculaire due à des infections dentaires supérieures menace la vision. Un gonflement autour de l'œil, une vision double ou une incapacité à bouger l'œil indique une cellulitis orbitaire. Cette complication, résultant d'infections dentaires maxillaires se propageant à travers un os mince dans l'orbite, nécessite une consultation d'urgence en ophtalmologie et en ORL.
Symptôme | Action requise | Délai |
Mal de dents avec léger gonflement | Rendez-vous dentaire | Dans les 24-48 heures |
Gonflement facial, fièvre | Soins dentaires ou médicaux urgents | Le même jour |
Difficulté à respirer/avaler | Service des urgences | Immédiatement |
Gonflement de l'œil, changements de vision | Service des urgences | Immédiatement |
Confusion, forte fièvre, rythme cardiaque rapide | Service des urgences/911 | Immédiatement |
Conclusion : Pourquoi une action précoce sauve des dents et des vies
Les infections dentaires nécessitent un contrôle rapide de la source par drainage, traitement de canal ou extraction. Les antibiotiques jouent un rôle de soutien pour la propagation systémique. La prévention par des soins réguliers évite la douleur, le coût et le danger des infections avancées.
Le traitement des infections dentaires repose sur des principes clairs. Éliminer la source de l'infection. Drainer le pus et les tissus nécrotiques. Préserver les dents naturelles lorsque cela est possible. Extraire lorsque nécessaire. Utiliser les antibiotiques judicieusement, uniquement en cas d'implication systémique ou lorsque les procédures doivent être retardées.
Les preuves soutiennent de manière écrasante cette approche. Les antibiotiques seuls échouent car ils ne peuvent pas atteindre les bactéries dans les chambres pulpaire nécrotiques et les cavités d'abcès. Les organismes protégés par le biofilm résistent à la pénétration des médicaments. Seule l'élimination mécanique des tissus infectés produit une guérison.
Un diagnostic précoce prévient les complications. Une petite lésion périapicale sur une radiographie avertit d'un abcès imminent. Une poche parodontal profonde signale un risque d'abcès. Traiter ces conditions avant le développement de symptômes aigus permet de sauver des dents, de l'argent et la santé.
Une utilisation équilibrée des antibiotiques protège les patients individuels et la santé publique. Chaque prescription inutile contribue à la résistance. Les dentistes qui suivent les directives de gestion, prescrivant uniquement pour les cas indiqués, choisissant des médicaments de première ligne à spectre étroit et limitant la durée, préservent l'efficacité des antibiotiques pour les générations futures.
L'intégration du traitement clinique et de la prévention offre les meilleurs résultats. Les patients qui combinent des visites dentaires régulières avec des soins à domicile quotidiens développent rarement des infections. Lorsque des infections surviennent, ils recherchent rapidement des soins plutôt que de supporter la douleur ou d'espérer une résolution spontanée.
L'avenir du traitement des infections dentaires semble prometteur. Les thérapies ciblant le biofilm, les techniques régénératives et les approches de médecine personnalisée amélioreront les résultats tout en réduisant la dépendance aux antibiotiques. Cependant, le principe fondamental reste inchangé : identifier la source, éliminer l'infection et restaurer la santé.
Références
Cope, Anwen L., et al. "Utilisation des antibiotiques en pratique dentaire : une revue systématique." British Dental Journal, vol. 216, no. 9, 2014, pp. 523-30.
Galler, Kerstin M., et al. "Procédures endodontiques régénératives pour le traitement de la nécrose pulpaire dans les dents permanentes immatures : une revue systématique." Journal of Endodontics, vol. 47, no. 8, 2021, pp. 1193-202.
Lockhart, Peter B., et al. "Mauvaise santé bucco-dentaire comme condition chronique, potentiellement infectieuse et inflammatoire." Journal of Dental Research, vol. 98, no. 10, 2019, pp. 1073-80.
Matthews, David C., et al. "Antibiotiques pour les abcès dentaires aigus : une revue systématique." Journal of Antimicrobial Chemotherapy, vol. 71, no. 3, 2016, pp. 564-71.
Moore, R. Andrew, et al. "Médicaments anti-inflammatoires non stéroïdiens pour la douleur dentaire aiguë." Cochrane Database of Systematic Reviews, no. 12, 2015, CD004978.
Ng, Yuan-Ling, et al. "Résultat du traitement endodontique primaire : revue systématique de la littérature." International Endodontic Journal, vol. 44, no. 7, 2011, pp. 597-612.
Patel, Shanon, et al. "Tomographie par faisceau conique en endodontie." Journal International d'Endodontie, vol. 52, no. 9, 2019, pp. 1248-64.
Petersen, Poul Erik. "Politique mondiale de l'Organisation mondiale de la santé pour l'amélioration de la santé bucco-dentaire." Journal International d'Odontologie, vol. 72, no. 4, 2022, pp. 302-07.
Seneviratne, Chaminda J., et al. "Biofilm de plaque dentaire : un biofilm archétypal." Parodontologie 2000, vol. 75, no. 1, 2017, pp. 34-44.