Лечение зубной инфекции требует удаления источника инфекции через дренаж, лечение корневых каналов или экстракцию. Антибиотики служат только вспомогательной терапией при системном вовлечении. Раннее вмешательство предотвращает серьезные осложнения, такие как сепсис и некроз тканей.
Что такое зубная инфекция и почему это важно?
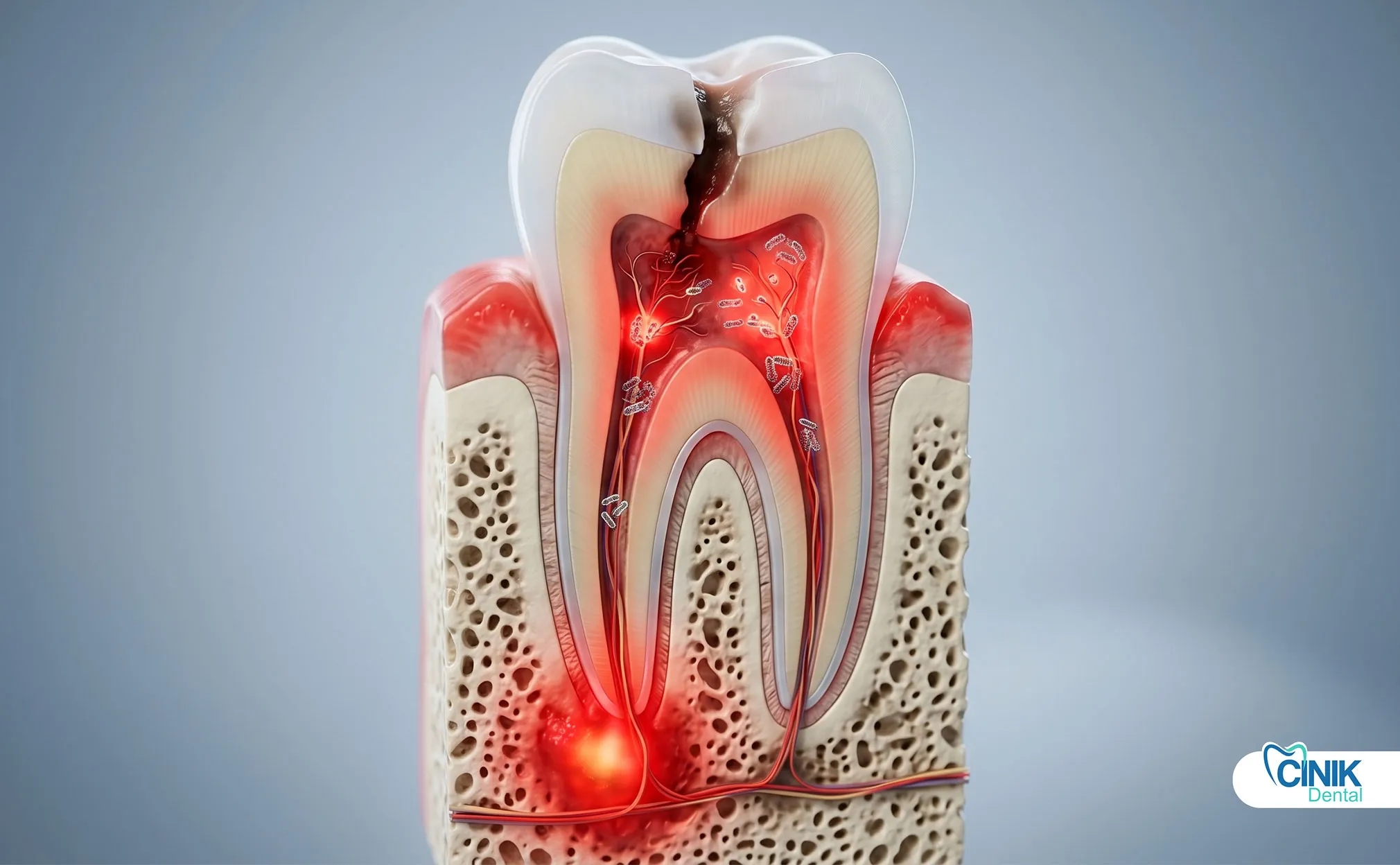
Зубная инфекция — это бактериальное вторжение в пульпу зуба, периодонтальные ткани или окружающую кость. Она вызывает сильную боль, отек и может распространиться на лицевые пространства или в кровоток без своевременного лечения.
Зубная инфекция, клинически называемая одонтогенной инфекцией, развивается, когда бактерии проникают в защитные слои зуба или окружающей десны. Эти инфекции начинаются с небольших проявлений, но могут перерасти в угрожающие жизни состояния в течение нескольких дней. Всемирная организация здравоохранения признает зубные инфекции значительной глобальной проблемой здравоохранения, особенно в популяциях с ограниченным доступом к стоматологической помощи (Петерсен, 2022).
Зубные инфекции делятся на три основные категории в зависимости от местоположения и происхождения. Периапикальные абсцессы образуются на кончике корня, когда пульпальная ткань погибает от глубокого кариеса или травмы. Периодонтальные абсцессы развиваются в поддерживающих структурах зуба, пораженных запущенным заболеванием десен. Гингивальные абсцессы остаются ограниченными краем десны, обычно вызванные импакцией инородного тела.
Клиническое значение зубных инфекций выходит за рамки орального дискомфорта. Исследования, опубликованные в Journal of Dental Research, показывают, что нелеченые зубные инфекции увеличивают риск сердечно-сосудистых заболеваний, осложняют управление диабетом и повышают системные воспалительные маркеры (Локхарт, 2019). В 2023 году отделения неотложной помощи по всей территории Соединенных Штатов лечили более 2 миллионов случаев зубных инфекций, при этом средние затраты на лечение превышали 1,000 долларов за визит, когда госпитализация становилась необходимой.
Раннее диагностирование имеет значение, потому что зубные инфекции следуют предсказуемой прогрессии. Бактерии размножаются в ограниченном пространстве корня зуба или кармана десны. Давление нарастает. Ткань отекает. Иммунный ответ вызывает лихорадку и недомогание. Без вмешательства инфекция преодолевает местные барьеры и проникает в фасциальные пространства, лимфатические каналы или кровоток.
Спектр лечения охватывает местные вмешательства и системные терапии. Местные подходы, дренаж, лечение корневых каналов, экстракция, устраняют источник инфекции напрямую. Системные подходы, в первую очередь антибиотики, поддерживают защиту организма, когда инфекция распространяется за пределы зуба. Ключевой принцип: местное лечение имеет приоритет. Антибиотики одни не могут стерилизовать инфицированный корневой канал или полость абсцесса.
Тип инфекции | Место | Основная причина | Типичное лечение |
Периапикальный абсцесс | Апекс корня | Некроз пульпы | Лечение корневого канала или удаление |
Периодонтальный абсцесс | Поддерживающие структуры | Запущенный периодонтит | Дренаж + периодонтальная терапия |
Гингивальный абсцесс | Края десны | Засорение инородным телом | Дренаж + удаление раздражителя |
Что вызывает развитие стоматологических инфекций?
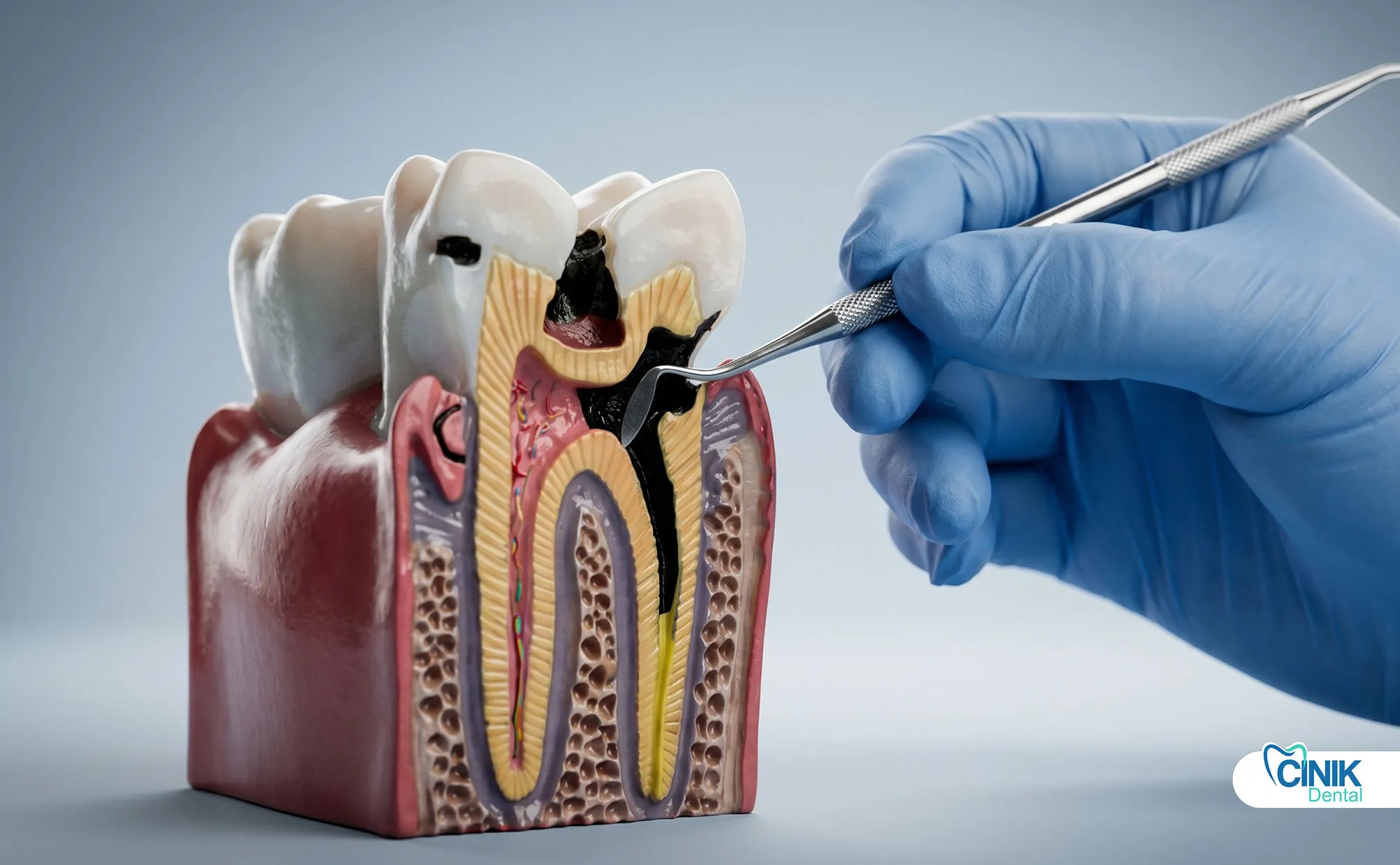
Зубной кариес, травмы, неудачные реставрации и периодонтальные заболевания позволяют бактериям проникать в пульпу зуба и окружающие ткани. Образование биопленки защищает бактерии и ускоряет разрушение тканей.
Как бактерии проникают в стоматологические ткани?
Бактерии проникают через трещины эмали, глубокие полости или карманы десен. Они образуют биопленки, которые сопротивляются иммунным атакам и антибиотикам, а затем разрушают пульпу, кость и мягкие ткани.
Зубные инфекции начинаются с бактериальной колонизации. В полости рта обитает более 700 видов бактерий, но только несколько из них вызывают инвазивные инфекции. Streptococcus mutans инициирует кариес, метаболизируя сахара в кислоту. Aggregatibacter actinomycetemcomitans и Porphyromonas gingivalis приводят к разрушению пародонта. Когда эти организмы нарушают защиту эмали или десен, они получают доступ к пульпе зуба, стерильной камере, содержащей нервы и кровеносные сосуды.
Зубной кариес остается основной причиной инфекции пульпы. Леченные полости прогрессируют через эмаль, дентин и, наконец, в камеру пульпы. Пульпа реагирует воспалением, но бактериальные токсины и давление в конечном итоге убивают ткань. Некротическая пульпа становится рассадником для анаэробных бактерий.
Травма ускоряет риск инфекции. Трещины в зубах, даже без видимых трещин, позволяют бактериям проникать. Неудачные реставрации создают микроскопические зазоры, где накапливаются бактерии. Лечение корневых каналов, которое пропускает ветви канала, оставляет остаточную инфекцию.
Пародонтит предоставляет альтернативный путь. По мере углубления карманов десен бактерии мигрируют вниз по поверхности корня. Иммунная система атакует как бактерии, так и ткани хозяина, разрушая периодонтальную связку и альвеолярную кость. Глубокие карманы, превышающие 7 миллиметров, часто содержат образующие абсцессы бактерии.
Образование биопленки усложняет лечение. Бактерии выделяют экстрацеллюлярные полисахариды, которые образуют защитную матрицу. Эта биопленка защищает организмы от антибиотиков, антител слюны и иммунных клеток. Внутри биопленки бактерии общаются через кворм-сенсинг и обмениваются генами устойчивости. Исследования Сеневаратне (2017) в Periodontology 2000 подтверждают, что бактерии, встроенные в биопленку, демонстрируют до 1,000-кратной большей устойчивости к антибиотикам, чем планктонные клетки.
Каковы основные типы зубных инфекций?
Периапикальные абсцессы поражают кончики корней, периодонтальные абсцессы атакуют поддерживающие структуры, а десневые абсцессы остаются на краях десен. Каждый тип требует разного времени и подхода к лечению.
Периапикальный абсцесс: Эта инфекция образуется на верхушке корня зуба после некроза пульпы. Гной накапливается в кости, окружающей кончик корня. Пациенты испытывают пульсирующую боль, которая усиливается в положении лежа. Зуб кажется приподнятым в своем лунке. Отек может появиться на лицевой коже, если инфекция перфорирует кость. Рентгеновские снимки показывают радиолюцентную область на верхушке корня. Лечение корневых каналов или удаление зуба устраняет источник инфекции.
Периодонтальный абсцесс: Эта инфекция развивается в уже существующем периодонтальном кармане. Она вызывает быстрое появление боли, отека и гнойных выделений из края десны. Затронутый зуб часто имеет подвижность из-за потери кости. Периодонтальные абсцессы требуют дренажа через десневой карман или внешнего разреза. После этого проводится чистка и планирование корней для уменьшения глубины кармана.
Десневой абсцесс: Самый поверхностный тип, ограниченный краем десны. Инородные тела, застревание пищи, щетинки зубной щетки, фрагменты зубной нити вызывают локализованную инфекцию. Боль остается умеренной. Отек остается ограниченным. Лечение включает удаление инородного объекта и обеспечение естественного дренажа.
Как распространяется стоматологическая инфекция?
Инфекции распространяются через местные тканевые плоскости, фасциальные пространства и в конечном итоге в кровоток. Отек лица, затрудненное глотание и лихорадка сигнализируют о опасном прогрессировании.
Местное вторжение в ткани представляет собой первую фазу. Бактерии и воспалительные медиаторы разрушают окружающую кость и мягкие ткани. Полость абсцесса увеличивается. Давление сжимает нервы, вызывая интенсивную боль. Ферменты, такие как коллагеназа, разрушают барьеры соединительной ткани.
Участие фасциального пространства отмечает опасное обострение. Лицо и шея содержат множество compartments соединительной ткани, разделенных фасциальными слоями. Бактерии движутся вдоль этих плоскостей, создавая угрожающие жизни отеки. Инфекция поднижнечелюстного пространства (ангина Людвига) может заблокировать дыхательные пути. Пещеристый синус, доступный через дренаж лицевой вены, рискует тромбообразованием и инфекцией мозга.
Системное распространение происходит, когда бактерии попадают в кровеносные сосуды. Бактериемия, наличие бактерий в крови, происходит во время стоматологических процедур и даже при энергичной чистке зубов. У здоровых людей иммунные клетки очищают транзиторную бактериемию. У пациентов с иммунодефицитом или тяжелыми инфекциями бактериемия прогрессирует до сепсиса. Эндокардит, инфекция сердечных клапанов, представляет особый риск для пациентов с протезированными клапанами или предыдущими повреждениями сердца.
Стадия распространения | Местоположение | Предупреждающие знаки | Уровень риска |
Локализованный | Зуб и ближайшая кость | Зубная боль, легкая опухоль | Низкий |
Региональный | Фасциальные пространства лица/шеи | Отечность лица, тризм, дисфагия | Умеренный-Высокий |
Системный | Кровеносная система и удаленные органы | Лихорадка, тахикардия, гипотензия, спутанность сознания | Критический |
Как стоматологи распознают и диагностируют стоматологические инфекции?
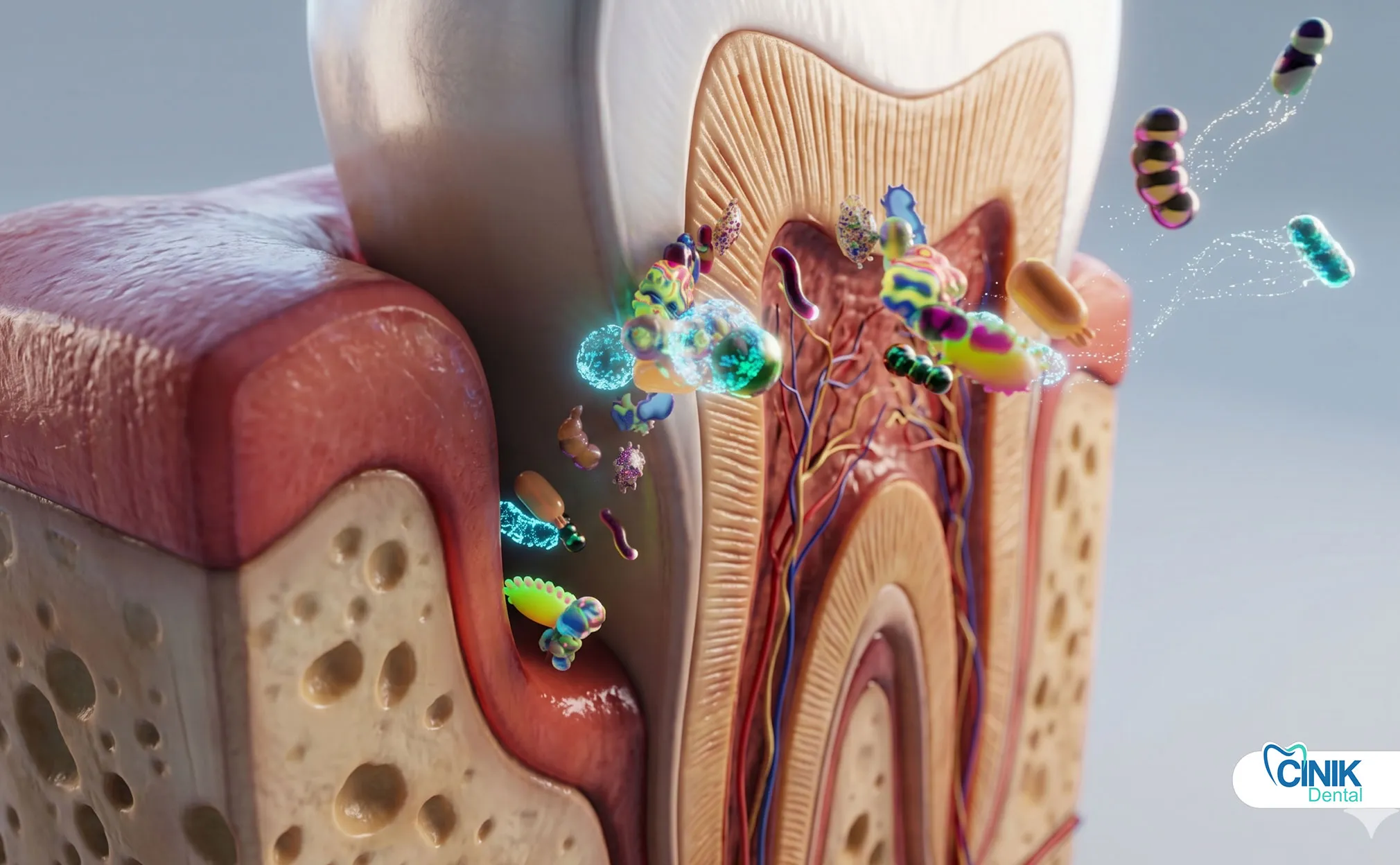
Стоматологи используют клинический осмотр, симптомы пациента, рентгенографическое изображение и тестирование пульпы для определения типа, степени тяжести и распространенности инфекции.
Какие симптомы указывают на стоматологическую инфекцию?
Сильная пульсирующая зубная боль, отечность лица, покраснение десен, чувствительность к температуре и лихорадка указывают на активную инфекцию, требующую немедленной оценки.
Боль является основным симптомом. Инфицированные зубы вызывают глубокую, пульсирующую боль, которую пациенты описывают как невыносимую. Боль усиливается при воздействии тепла и может временно уменьшаться при приложении холода на ранних стадиях пульпита. Как только пульпа некротизируется, чувствительность к холоду исчезает, но боль от давления усиливается по мере накопления гноя под корнем.
Отек сигнализирует о прогрессирующей инфекции. Ранние инфекции вызывают отек десен в полости рта. По мере увеличения давления отек распространяется на кожу лица. Кожа становится красной, теплой и напряженной. Пациенты могут сообщать, что отек появился внезапно и увеличивался в течение нескольких часов.
Системные симптомы указывают на распространение инфекции. Температура выше 38°C (100.4°F) свидетельствует о мобилизации иммунной системы против значительной бактериальной нагрузки. Недомогание, потеря аппетита и затруднение открытия рта (трисмус) сопровождают вовлечение фасциального пространства. Затруднение глотания (дисфагия) или дыхания представляет собой риск для дыхательных путей.
Какие диагностические инструменты подтверждают стоматологические инфекции?
Клиническое пальпирование, перкуссионное тестирование, рентгенография, КТ с конусным лучом и электрические тесты пульпы подтверждают наличие инфекции, ее локализацию и состояние жизнеспособности зуба.
Клиническое обследование предоставляет немедленные подсказки. Стоматологи пальпируют опухшие участки, чтобы оценить флуктуацию; мягкий, заполненный жидкостью отек указывает на накопление гноя. Перкуссионное тестирование стучит по зубам тупым инструментом; инфицированные зубы передают вибрацию болезненно через воспаленные периодонтальные связки. Тестирование подвижности выявляет зубы с выраженной потерей костной ткани из-за периодонтальных абсцессов.
Рентгеновская визуализация показывает разрушение кости. Стандартные перiapical рентгенограммы показывают радиолюцентные области на кончиках корней, указывая на потерю кости из-за перiapical абсцессов. Байтвинговые рентгенограммы выявляют глубокие кариесы и уровни костной ткани периодонта. Однако 2D рентгенограммы пропускают ранние инфекции и сложную анатомию.
Компьютерная томография с конусным лучом (КТ с КЛ) предлагает трехмерную визуализацию. Эта технология обнаруживает абсцессы до появления видимых изменений в кости на стандартных рентгенограммах. КТ с КЛ выявляет дополнительные корневые каналы, переломы корней и точные схемы распространения в фасциальные пространства. Исследование Пателя (2019) в International Endodontic Journal подтверждает, что КТ с КЛ обнаруживает на 40% больше перiapical поражений, чем традиционная рентгенография.
Тестирование жизнеспособности пульпы различает обратимые и необратимые состояния. Электрические тестеры пульпы стимулируют нервный ответ; нежизнеспособные зубы не показывают ощущения. Холодное тестирование с помощью охлаждающего спрея оценивает функцию нерва. Некротическая пульпа не реагирует на холод, в то время как воспаленная жизнеспособная пульпа вызывает чрезмерную, длительную боль.
Каковы основные принципы лечения стоматологических инфекций?
Сначала удалите источник инфекции через дренаж, корневой канал или экстракцию. Используйте антибиотики только тогда, когда инфекция распространяется системно. Никогда не полагайтесь только на антибиотики.
Основная цель лечения стоматологических инфекций — контроль источника. Антибиотики циркулируют в крови, но не могут проникнуть в некротические камеры пульпы, полости абсцессов или колонии бактерий, защищенные биопленкой. Источник инфекции, мертвая пульпа, накопленный гной или больной периодонтальный карман, должен быть физически устранен.
Дренаж и дебридмент составляют основу контроля источника. Полость абсцесса содержит гной, бактериальные токсины и воспалительную жидкость. Разрез и дренаж освобождают этот материал, уменьшая давление и бактериальную нагрузку. Лечение корневых каналов удаляет инфицированную пульповую ткань изнутри зуба. Экстракция устраняет всю инфицированную структуру.
Консервативные подходы сохраняют натуральные зубы, когда это возможно. Лечение корневых каналов сохраняет зубы с периапикальными абсцессами, если достаточно структуры зуба остается для восстановления. Периодонтальные абсцессы часто реагируют на дренаж в сочетании с глубокой чисткой. Экстракция становится необходимой, когда зубы имеют переломы ниже линии десны, серьезную потерю костной ткани или неудачное предыдущее лечение корневых каналов.
Хирургические подходы решают сложные случаи. Апикоэктомия, хирургическое удаление корневой части, сохраняет зубы с устойчивой периапикальной инфекцией после лечения корневых каналов. Периодонтальная хирургия уменьшает глубокие карманы, в которых обитают рецидивирующие абсцессы. Госпитальная хирургия управляет инфекциями фасциального пространства, требующими защиты дыхательных путей.
Ключевое клиническое понимание: местное лечение имеет приоритет над антибиотиками. Пациент с зубным абсцессом, который получает только антибиотики, испытывает временное облегчение симптомов, но сталкивается с гарантированным рецидивом. Полость абсцесса остается. Бактерии повторно колонизируют. Без дренажа или лечения зуба инфекция возвращается, часто с антибиотикоустойчивыми организмами.
Какие стоматологические процедуры лечат инфекции в первую очередь?
Стоматологи приоритизируют разрез и дренаж для абсцессов, лечение корневых каналов для зубов, которые можно спасти, и экстракцию для зубов, которые нельзя восстановить. Эти процедуры непосредственно устраняют источники инфекции.
Как работает дренаж абсцесса?
Стоматолог обезболивает область, делает небольшой разрез в абсцессе и позволяет гною вытекать. Это немедленно уменьшает боль и давление, удаляя бактериальную нагрузку.
Разрез и дренаж обеспечивают самое быстрое облегчение боли при острых абсцессах. Процедура требует местной анестезии. Стоматолог определяет наиболее флуктуирующую (самую мягкую, наиболее заполненную жидкостью) область отека. Разрез скальпелем, обычно 1-2 сантиметра, проникает в полость абсцесса. Гной эвакуируется под давлением. Стоматолог может вставить небольшой резиновый дренаж, чтобы поддерживать открытие в течение 24-48 часов.
Немедленные преимущества включают уменьшение давления и облегчение боли. Пациенты часто сообщают о резком улучшении в течение нескольких часов. Дренаж также удаляет бактериальный инокулят, уменьшая системную бактериальную нагрузку. Процедура занимает 15-30 минут в стоматологическом кабинете.
Уход после дренажа включает теплые солевые полоскания для поддержания проходимости дренажа. Пациенты продолжают принимать антибиотики, если существуют системные симптомы. Окончательное лечение зуба, лечение корневых каналов или экстракция, следует после того, как острое воспаление утихнет, обычно в течение 3-7 дней.
Когда лечение корневых каналов спасает инфицированный зуб?
Лечение корневых каналов удаляет инфицированную пульпу, дезинфицирует корневые каналы и запечатывает зуб. Оно сохраняет натуральные зубы, когда достаточно структуры для восстановления коронки.
Лечение корневых каналов устраняет периапикальные абсцессы, удаляя содержимое инфицированной пульповой камеры. Стоматолог создает доступное отверстие через коронку зуба. Инструменты удаляют пульповую ткань, некротические остатки и бактериальную биопленку из системы каналов. Химические ирригаторы, гипохлорит натрия и хлоргексидин, дезинфицируют стенки каналов.
Процедура требует 1-3 визитов в зависимости от тяжести инфекции. Первый визит сосредоточен на удалении пульпы и дренировании абсцесса через зуб. Стоматолог помещает антибактериальное средство внутри канала и запечатывает временной пломбой. Второй визит подтверждает контроль инфекции перед заполнением каналов гуттаперчей, резинообразным материалом. Постоянная коронка восстанавливает прочность зуба.
Успехи превышают 90% для первичных лечений корневых каналов. Исследование Нга (2011) в International Endodontic Journal сообщает о 94% выживаемости через 4 года для зубов с периапикальными абсцессами, леченными терапией корневых каналов и восстановлением коронки. Неудачи обычно возникают из-за пропущенных ветвей канала, устойчивой бактериальной биопленки или коронального протекания.
Когда необходимо удалить инфицированный зуб?
Удаление становится необходимым, когда зубы имеют трещины ниже линии десны, серьезную потерю костной ткани, неудачное повторное лечение корневых каналов или недостаточную структуру для восстановления.
Удаление зуба обеспечивает окончательное устранение инфекции, когда сохранение невозможно. Вертикальные переломы корня, которые простираются ниже линии десны, препятствуют бактериальной герметизации независимо от лечения. Серьезное пародонтальное заболевание, уничтожающее более 50% поддерживающей кости, делает зубы не подлежащими восстановлению. Неудачное повторное лечение корневых каналов, особенно с устойчивыми периапикальными поражениями, может потребовать удаления и замены имплантом.
Процедура удаления инфицированных зубов требует осторожности, чтобы предотвратить распространение бактерий. Стоматолог может назначить предоперационные антибиотики для иммунокомпрометированных пациентов или при серьезных инфекциях. Местная анестезия с вазоконстриктором контролирует кровотечение. Стоматолог поднимает зуб из лунки, удаляет грануляционную ткань из основания лунки и обеспечивает полное очищение.
Заживление после удаления занимает 1-2 недели для закрытия мягких тканей. Ремоделирование кости продолжается в течение 3-6 месяцев. Немедленная установка импланта, проводимая в отдельных случаях, сокращает время лечения, но требует участков удаления без инфекции.
Запись на основе доказательств: Окончательные стоматологические процедуры остаются необходимыми, поскольку антибиотики не могут устранить источники инфекции. Систематический обзор Коупа (2014) в British Dental Journal проанализировал 22 клинических испытания и пришел к выводу, что антибиотики без контроля источника не обеспечивают устойчивой пользы для стоматологических абсцессов. Рецидив симптомов происходит в 100% случаев в течение нескольких недель.
Процедура | Показание | Уровень успеха | Время восстановления |
Разрез и дренирование | Острый абсцесс с колеблющейся опухолью | Немедленное облегчение; требуется последующее наблюдение | 2-3 дня |
Лечение корневых каналов | Периапикальный абсцесс, восстанавливаемый зуб | 90-95% через 5 лет | 1-2 недели |
Удаление зуба | Не восстанавливаемый зуб, неудачное повторное лечение | 100% устранение инфекции | 1-2 недели мягких тканей |
Как антибиотики поддерживают лечение инфекций зубов?
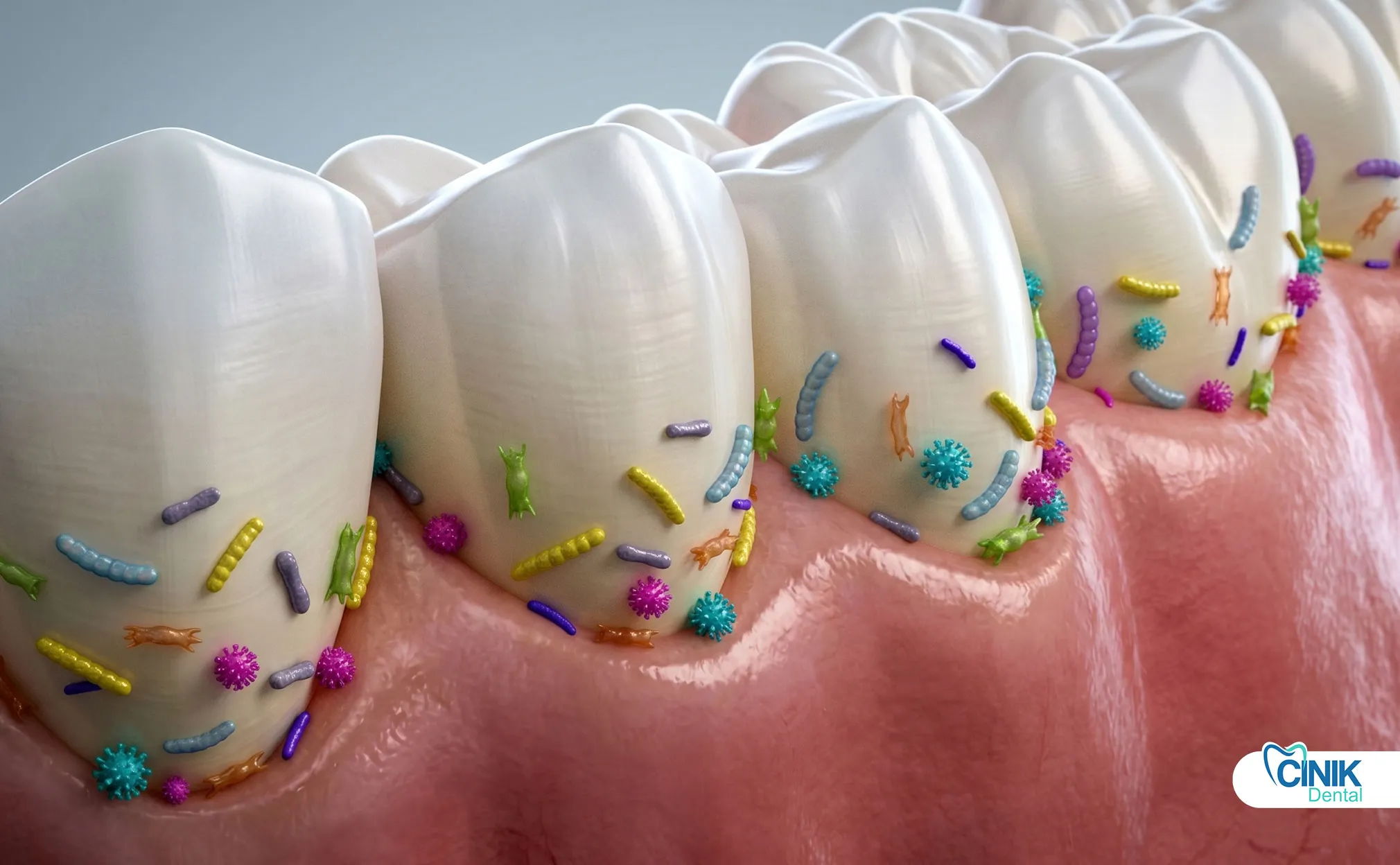
Антибиотики лечат распространяющиеся инфекции с лихорадкой, лицевым целлюлитом или иммунодефицитом. Они никогда не заменяют дренаж или лечение зубов. Амоксициллин остается препаратом первой линии.
Когда стоматологи назначают антибиотики?
Стоматологи назначают антибиотики при системных симптомах, распространяющемся целлюлите, у пациентов с иммунодефицитом или когда немедленные стоматологические процедуры невозможны.
Антибиотики играют вспомогательную роль в управлении инфекциями в стоматологии. Они не лечат зубные абсцессы. Они контролируют распространение бактерий, когда инфекция превышает местное сдерживание. Конкретные показания включают:
Системное вовлечение: Лихорадка выше 38°C, недомогание или лимфаденопатия указывают на превышение бактериальной нагрузки над местной иммунной способностью. Антибиотики снижают риск бактериемии и поддерживают системное восстановление.
Распространяющаяся инфекция: Целлюлит, диффузное покраснение кожи без локализованного абсцесса требует антибиотиков, так как дренирование невозможно. Инфекции, проникающие в фасциальные пространства, нуждаются в агрессивном антибиотикотерапии в ожидании хирургического вмешательства.
Иммунокомпрометированные состояния: Пациенты с диабетом, ВИЧ, химиотерапией или пересадкой органов сталкиваются с более высоким риском сепсиса. Ранняя антибиотикотерапия защищает эти уязвимые группы населения.
Процедурная профилактика: Определенные медицинские состояния требуют антибиотикотерапии перед стоматологическими процедурами для предотвращения инфекции на удаленных участках. Протезные сердечные клапаны, предыдущий инфекционный эндокардит и некоторые ортопедические имплантаты попадают в эту категорию.
Важный принцип: Антибиотики являются вспомогательными, а не основным лечением. Пациент с локализованным зубным абсцессом и без системных симптомов не нуждается в антибиотиках. Стоматолог проводит дренирование и лечение зуба. Добавление антибиотиков не приносит пользы и способствует развитию резистентности.
Какие антибиотики лучше всего подходят для лечения стоматологических инфекций?
Амоксициллин остается антибиотиком первой линии благодаря своей эффективности против типичных оральных патогенов и отличной переносимости. Пенициллин V служит альтернативой.
Амоксициллин доминирует в назначении антибиотиков первой линии в стоматологии. Этот аминопенициллин покрывает грамположительные кокки (Streptococcus виды) и грамнегативные анаэробы (Prevotella, Fusobacterium), которые вызывают большинство стоматологических инфекций. Оральное всасывание достигает 90%, обеспечивая надежные уровни в крови. Стандартная доза для взрослых составляет 500 мг три раза в день в течение 5-7 дней.
Клинические доказательства: Рандомизированное контролируемое исследование, проведенное Мэттьюсом (2016) в Journal of Antimicrobial Chemotherapy, сравнивало амоксициллин с плацебо для лечения зубных абсцессов. Обе группы получили разрез и дренирование. Амоксициллин снизил отек после процедуры на 35% и сократил время восстановления на 2 дня. Однако показатели излечения на 30-й день были идентичны, что подтверждает, что контроль источника, а не антибиотики, определяет результаты.
Пенициллин V предоставляет альтернативу с более узким спектром. Этот феноксиметилпенициллин устойчив к разрушению желудочной кислотой, что делает его подходящим для перорального применения. Типичная доза составляет 500 мг четыре раза в день. Пенициллин V покрывает большинство одонтогенных патогенов, но не охватывает грамнегативные анаэробы по сравнению с амоксициллином.
Какие антибиотики помогают, когда препараты первой линии неэффективны?
Метронидазол нацелен на анаэробы и комбинируется с амоксициллином для лечения тяжелых инфекций. Клиндамицин заменяет пенициллин у аллергиков. Азитромицин предлагает еще одну альтернативу.
Метронидазол специально нацелен на облигатные анаэробные бактерии. Эти организмы доминируют в некротической пульпе и глубоких пародонтальных карманах. Метронидазол сам по себе не покрывает аэробные стрептококки, поэтому стоматологи часто комбинируют его с амоксициллином для тяжелых смешанных инфекций. Доза составляет 400 мг три раза в день. Пациенты должны избегать алкоголя во время лечения и в течение 48 часов после его завершения из-за реакций, подобных дисульфираму.
Клиндамицин предназначен для пациентов с аллергией на пенициллин. Этот линкозамидный антибиотик эффективно покрывает грамположительные организмы и анаэробы. Доза составляет 300 мг четыре раза в день. Стоматологи резервируют клиндамицин для истинных аллергий на пенициллин, поскольку он несет более высокий риск колита, вызванного Clostridioides difficile, серьезной кишечной инфекции.
Азитромицин предоставляет еще одну альтернативу для пациентов с аллергией на пенициллин. Этот макролидный антибиотик предлагает удобное дозирование, 500 мг в день в течение 3 дней, благодаря своему длинному тканевому полу-жизни. Однако растущая резистентность среди оральных стрептококков ограничивает его надежность. Стоматологи используют азитромицин, когда клиндамицин противопоказан.
Почему резистентность к антибиотикам угрожает стоматологическому лечению?
Чрезмерное назначение стоматологических антибиотиков ускоряет бактериальную резистентность. Рекомендации теперь не советуют рутинное использование антибиотиков для локализованных инфекций без системного распространения.
Резистентность к антибиотикам подрывает управление стоматологическими инфекциями. Центры по контролю и профилактике заболеваний определяют стоматологическое назначение как значительный фактор ненужного использования антибиотиков. Исследования оценивают, что 30-50% стоматологических рецептов на антибиотики являются ненужными, назначенными для состояний, где достаточно только контроля источника.
Последствия выходят за рамки отдельных пациентов. Устойчивые бактерии колонизируют полость рта и распространяются на членов семьи, медицинские учреждения и сообщества. Штаммы Streptococcus pneumoniae и Staphylococcus aureus, устойчивые к пенициллину и клиндамицину, все чаще появляются в стоматологических инфекциях.
Программы управления антибиотиками нацелены на чрезмерное назначение антибиотиков в стоматологии. Американская стоматологическая ассоциация обновила рекомендации в 2019 году, четко указав, что антибиотики не показаны для локализованных интраоральных отеков без системного вовлечения. Рекомендации подчеркивают: "Основным методом лечения стоматологической инфекции должен быть контроль источника."
Целевая терапия заменяет эмпирическое назначение в рецидивирующих или сложных случаях. Культура и тестирование на чувствительность определяют конкретные бактерии и их паттерны резистентности. Этот подход, стандартный в больничных условиях, становится все более распространенным в стоматологической практике для иммунокомпрометированных пациентов или при неудачах лечения.
Антибиотик | Спектр | Типичная доза | Лучше всего для |
Амоксициллин | Широкий (аэробы + анаэробы) | 500 мг 3 раза в день на 5-7 дней | Первый выбор, большинство инфекций |
Пенициллин V | Узкий (аэробы) | 500 мг 4 раза в день на 5-7 дней | Легкие инфекции, предпочтение пенициллину |
Метронидазол | Только анаэробы | 400 мг 3 раза в день на 5-7 дней | В комбинации с амоксициллином для тяжелых случаев |
Клиндамицин | Аэробы + анаэробы | 300 мг 4 раза в день на 5-7 дней | Аллергия на пенициллин |
Азитромицин | Широкий | 500 мг в день x 3 дня | Аллергия на пенициллин, клиндамицин противопоказан |
Как стоматологи управляют болью при лечении инфекций?
НПВП, такие как ибупрофен, обеспечивают более эффективное облегчение зубной боли по сравнению с опиоидами. Парацетамол предлагает альтернативу для пациентов, которые не могут принимать НПВП. Местная анестезия во время процедур устраняет болевые ощущения.
Управление болью при зубных инфекциях основывается на многомодальном подходе. Нестероидные противовоспалительные препараты (НПВП) составляют основу. Ибупрофен, 400-600 мг каждые 6-8 часов, уменьшает воспаление в месте инфекции, обеспечивая анальгезию. Исследование Мура (2015) в Cochrane Database of Systematic Reviews подтверждает, что ибупрофен 400 мг обеспечивает лучшее облегчение боли, чем кодеин 60 мг при зубной боли, с меньшим количеством побочных эффектов.
Парацетамол (ацетаминофен) подходит пациентам с противопоказаниями к НПВП, язвенной болезнью, терапией антикоагулянтами или нарушением функции почек. Доза составляет 500-1000 мг каждые 6 часов, не превышая 3000 мг в день. Парацетамол не обладает противовоспалительным действием, но обеспечивает эффективную анальгезию.
Комбинированная терапия улучшает контроль боли. Чередование ибупрофена и парацетамола поддерживает стабильный уровень препаратов. Некоторые исследования предполагают, что одновременное применение обеспечивает лучшее облегчение, чем любой из препаратов по отдельности, хотя пациенты должны внимательно отслеживать интервалы дозирования, чтобы избежать передозировки.
Назначение опиоидов резко сократилось в стоматологической практике. Эпидемия опиоидов побудила пересмотреть протоколы лечения зубной боли. Текущие рекомендации оставляют опиоиды для тяжелой послеоперационной боли, не поддающейся НПВП. При назначении стоматологи ограничивают количество до 3-5 дней и комбинируют с НПВП, чтобы снизить потребность в опиоидах.
Поддерживающие меры дополняют медикаментозное лечение. Гидратация поддерживает поток слюны и поддерживает иммунную функцию. Теплые солевые полоскания (половина чайной ложки соли в теплой воде, полощут 30 секунд) уменьшают бактериальную нагрузку и способствуют дренированию из карманов десен. Мягкая пища предотвращает механическое раздражение инфицированных тканей. Поднятие головы во время сна уменьшает кровоток к опухшим лицевым тканям, снижая пульсирующую боль.
Что происходит, когда зубные инфекции не лечатся?
Нелеченые зубные инфекции вызывают локальное разрушение костей, некроз тканей и потенциально смертельные системные осложнения, включая сепсис, обструкцию дыхательных путей и абсцесс мозга.
Какой локальный ущерб причиняют нелеченые инфекции?
Нелеченые инфекции разрушают челюстную кость (остеомиелит), убивают мягкие ткани (некроз) и распространяются через лицевые пространства, вызывая деформацию и функциональные потери.
Остеомиелит представляет собой инфекцию кости, вызванную бактериальным заражением. Челюстная кость развивает участки мертвой кости (секуестры), окруженные воспаленной тканью. Хронический остеомиелит вызывает постоянную боль, дренирующие свищи и патологические переломы. Лечение требует длительного применения антибиотиков (4-6 недель) и хирургического удаления мертвой кости. Гипербарическая оксигенотерапия поддерживает заживление в рефрактерных случаях.
Некроз тканей происходит, когда инфекция нарушает кровоснабжение. Нёбо, язык или кожа лица могут развивать черные, обескровленные участки, требующие хирургического удаления некротической ткани. Некротизирующий фасциит, хотя и редок при стоматологических инфекциях, быстро разрушает тканевые планы и требует экстренного хирургического вмешательства.
Инфекции лицевых пространств искажают анатомию. Подчелюстные, крыловидно-челюстные и собачьи пространства значительно опухают. У пациентов развивается "бычья шея" из-за двустороннего поражения подчелюстной области. Тризис, блокировка челюсти из-за воспаления мышц, мешает есть и говорить.
Какие системные риски создают стоматологические инфекции?
Бактерии из стоматологических инфекций попадают в кровоток, вызывая сепсис, инфекцию сердечных клапанов и отдаленные абсцессы. Обструкция дыхательных путей из-за отека шеи может привести к удушью.
Сепсис представляет собой наиболее страшное системное осложнение. Бактериальные токсины вызывают массовую активацию иммунной системы. Лихорадка, учащенное сердцебиение, учащенное дыхание и спутанность сознания сигнализируют о сепсисе. Артериальное давление падает. Органы отказывают. Септический шок несет 40% смертности даже при интенсивной терапии. Стоматологические инфекции вызывают 10-15% всех случаев лицевого сепсиса.
Обструкция дыхательных путей угрожает жизни в течение нескольких часов. Ангина Людвига, инфекция двустороннего подчелюстного пространства, поднимает язык вверх и назад. Дно рта становится жестким. Пациенты слюнотечат, не могут глотать слюну и развивают стридор (шумное дыхание). Экстренная трахеостомия или интубация обеспечивают проходимость дыхательных путей перед хирургическим дренированием.
Абсцесс мозга, хотя и редок, возникает после гематогенного распространения или прямого распространения через кости черепа. Инфекции фронтальных зубов достигают лобной доли. Максиллярные инфекции достигают височной доли. Абсцессы мозга вызывают головную боль, судороги, очаговую слабость и измененное психическое состояние. Нейрохирургическое дренирование и длительное применение антибиотиков (6-8 недель) лечат это осложнение.
Эндокардит поражает сердечные клапаны, особенно у пациентов с предшествующими заболеваниями клапанов или протезированными клапанами. Viridans streptococci из стоматологических инфекций прилипают к поврежденному эндокарду, образуя вегетации, которые эмболизируются в мозг, почки и конечности. Профилактические антибиотики перед стоматологическими процедурами предотвращают это осложнение у пациентов с высоким риском.
Осложнение | Механизм | Риск смертности | Требуемое лечение |
Остеомиелит | Инфекция и некроз кости | Низкий | Хирургия + 4-6 недель антибиотиков |
Сепсис | Бактериальное распространение в крови | 15-40% | Уход в реанимации, внутривенные антибиотики, контроль источника |
Ангина Людвига | Двусторонняя субмандибулярная инфекция | 10-20% | Экстренная проходимость дыхательных путей + хирургический дренаж |
Абсцесс мозга | Гематогенное или прямое распространение | 10-30% | Нейрохирургия + 6-8 недель антибиотиков |
Как специальные группы населения должны получать лечение инфекций зубов?
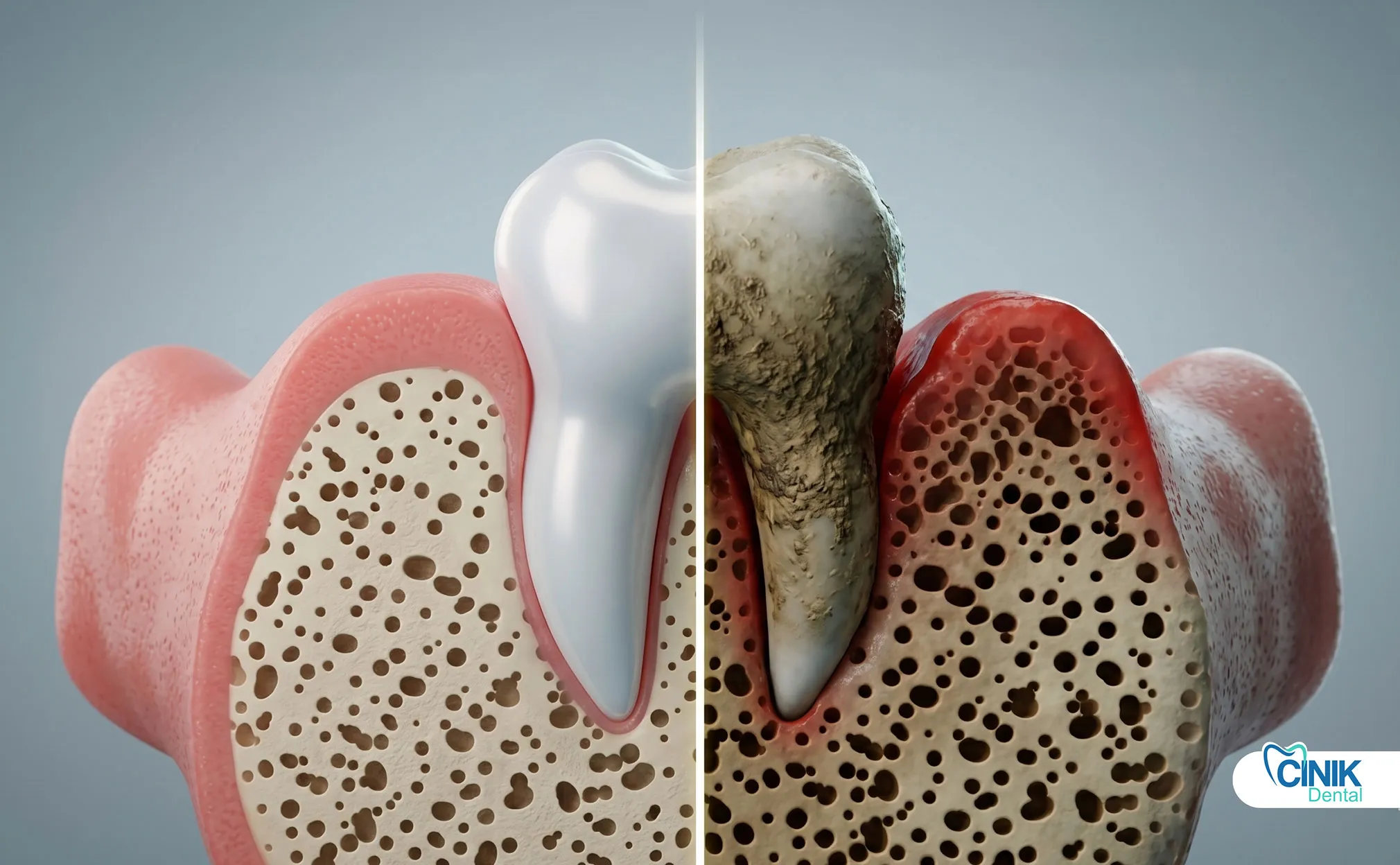
Иммунокомпрометированные, педиатрические и пожилые пациенты нуждаются в модифицированных подходах к лечению, более раннем вмешательстве антибиотиков, корректировке дозировки препаратов и более тщательном мониторинге.
Какую дополнительную заботу требуют иммунокомпрометированные пациенты?
Иммунокомпрометированные пациенты сталкиваются с более высоким риском системного распространения. Им необходимо более раннее начало антибиотикотерапии, более широкий охват, лечение в стационаре при умеренных инфекциях и более длительный мониторинг восстановления.
Иммунокомпрометированные состояния включают сахарный диабет, ВИЧ/СПИД, химиотерапию, трансплантацию органов, хроническое применение кортикостероидов и наследственные иммунодефициты. Эти состояния нарушают функцию нейтрофилов, выработку антител или клеточный иммунитет, что является критической защитой от стоматологических патогенов.
Более высокий риск распространения инфекции требует агрессивного управления. Локальный абсцесс у здорового пациента может оставаться ограниченным в течение нескольких дней. Тот же абсцесс у пациента с нейтропенией, получающего химиотерапию, может прогрессировать до сепсиса в течение нескольких часов. Стоматологи снижают пороги для начала антибиотикотерапии и направления в стационар.
Раннее вмешательство антибиотиками использует более широкий спектр охвата. В то время как здоровые пациенты получают только амоксициллин, иммунокомпрометированные пациенты могут нуждаться в амоксициллин-клавуланате (Аугментин) для улучшенного охвата анаэробов или даже в внутривенных антибиотиках для госпитализации.
Лечение в стационаре становится необходимым для инфекций, которые могли бы лечиться в офисе у здоровых пациентов. Внутривенный доступ обеспечивает надежную доставку препаратов. Мониторинг отслеживает температуру, количество лейкоцитов и воспалительные маркеры. Хирургические бригады готовы к управлению дыхательными путями, если возникает вовлечение фасциального пространства.
Как стоматологи корректируют лечение для детей и пожилых пациентов?
Детям требуется дозировка на основе веса и управление поведением. Пожилым пациентам необходимо оценивать функцию почек, проверять взаимодействие препаратов и учитывать сопутствующие заболевания.
Педиатрические стоматологические инфекции представляют собой уникальные проблемы. Молочные зубы с периапикальными абсцессами часто требуют удаления, а не эндодонтической терапии из-за сложной анатомии корней и приближающегося срока их выпадения. Удерживатели пространства предотвращают ортодонтические осложнения после преждевременной потери зуба. Дозировка антибиотиков рассчитывается на основе веса, амоксициллин 50 мг/кг/день, разделенный на 3 дозы.
Управление поведением позволяет проводить лечение у молодых пациентов. Местная анестезия требует тщательной техники, чтобы избежать интраваскулярной инъекции у маленьких пациентов. Седация или общая анестезия могут быть необходимы для обширных процедур. Родители играют ключевую роль в постлечебном уходе, обеспечивая соблюдение режима приема лекарств и изменения в диете.
Гериатрические пациенты представляют собой различные сложности. Полипрагмазия увеличивает риски взаимодействия лекарств. Антибиотики могут взаимодействовать с варфарином (клиндамицин и метронидазол усиливают эффекты), статинами или сердечными препаратами. Снижение функции почек требует корректировки дозы для препаратов, выводимых почками, таких как амоксициллин и метронидазол.
Когнитивные нарушения усложняют сообщение о симптомах. Пожилые пациенты с деменцией могут неэффективно сообщать о боли. Опекуны должны наблюдать за изменениями в поведении, отказом от еды, прикосновениями к лицу или беспокойством как индикаторами инфекции. Планирование лечения ставит простоту и долговечность выше идеалистических подходов.
Популяция | Ключевое соображение | Корректировка антибиотиков | Специальные потребности |
Иммунокомпрометированные | Высокий риск распространения | Широкий спектр, раннее начало | Порог направления в больницу снижен |
Педиатрия | Рост и развитие | Дозировка по весу | Управление поведением, поддержание пространства |
Гериатрия | Сопутствующие заболевания, полипрагмазия | Корректировка дозы для почек | Обзор взаимодействия лекарств, когнитивная оценка |
Как люди могут предотвратить стоматологические инфекции?
Ежедневная чистка зубов и использование зубной нити, регулярные стоматологические осмотры каждые 6 месяцев, своевременное лечение кариеса и управление заболеваниями десен предотвращают условия, ведущие к стоматологическим инфекциям.
Профилактика стоматологических инфекций нацелена на коренные причины: кариес и пародонтоз. Практики гигиены полости рта нарушают образование бактериальной биопленки до того, как она вызовет повреждение тканей. Американская стоматологическая ассоциация рекомендует чистить зубы дважды в день фторсодержащей зубной пастой в течение 2 минут, используя мягкую щетку круговыми движениями вдоль линии десен.
Использование зубной нити достигает участков, которые пропускают щетки, между зубами и ниже краев десен, где колонизируются патогены пародонта. Ирригаторы и межзубные щетки помогают пациентам с ограниченной ручной моторикой. Полоскания рта, содержащие хлоргексидин или эфирные масла, уменьшают бактериальную нагрузку, но не заменяют механическую чистку.
Регулярные стоматологические осмотры позволяют проводить раннее вмешательство. Профессиональная чистка удаляет зубной камень (зубной налет), который содержит бактерии. Осмотры выявляют кариес до того, как он достигнет пульпы. Байтвинговые рентгеновские снимки выявляют межзубной кариес, невидимый при визуальном осмотре. Интервал в 6 месяцев подходит большинству пациентов, хотя тем, у кого высокий риск кариеса или активное заболевание пародонта, могут понадобиться интервалы в 3-4 месяца.
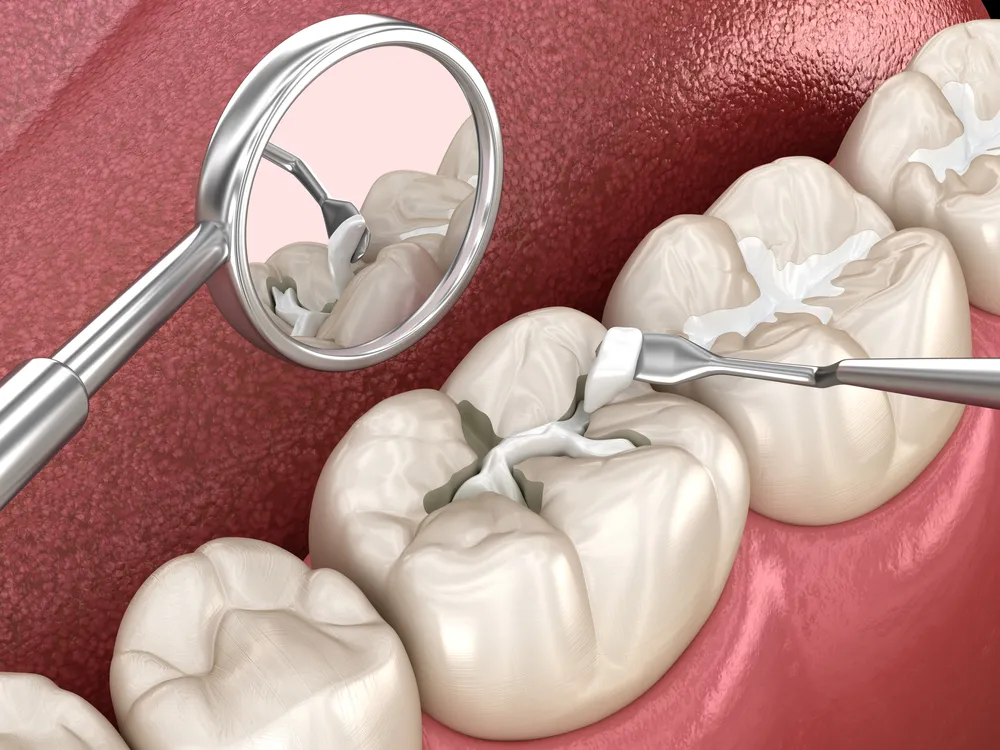
Своевременное лечение кариеса предотвращает инфекцию пульпы. Небольшие кариозные полости требуют простых пломб. Задержка позволяет кариесу углубляться, в конечном итоге требуя лечения корневых каналов или удаления зуба. ЗубныеSealants на задних зубах защищают детей и подростков от кариеса на жевательной поверхности.
Управление заболеванием пародонта предотвращает пародонтальные абсцессы. Скалирование и планирование корней (глубокая чистка) удаляет зубной камень с корневых поверхностей. Пародонтальное обслуживание каждые 3 месяца контролирует прогрессирование заболевания. Хирургическое уменьшение карманов устраняет глубокие пространства, где образуются абсцессы.
Изменения в диете поддерживают профилактику. Ограничение потребления сахара, особенно частые перекусы и сладкие напитки, снижает продукцию кислоты Streptococcus mutans. Жевание безсахарной жевательной резинки стимулирует слюноотделение, что нейтрализует кислоту и реминерализует эмаль. Фторированная вода укрепляет структуру зубов против кислотной атаки.
Каковы ожидаемые сроки восстановления после лечения стоматической инфекции?
Боль улучшается в течение 24-48 часов после контроля источника. Мягкие ткани заживают за 1-2 недели. Заживление кости занимает 3-6 месяцев. Раннее вмешательство приводит к более быстрому и полному восстановлению.
Ожидаемые сроки заживления варьируются в зависимости от процедуры и тяжести инфекции. Дренирование острого абсцесса обеспечивает немедленное облегчение боли. Отек уменьшается в течение 2-3 дней. Небольшой разрез заживает в течение недели. Однако подлежащий зуб все еще требует окончательного лечения для предотвращения рецидива.
Восстановление после лечения корневых каналов следует предсказуемому паттерну. Послеоперационная болезненность длится 2-3 дня, управляемая НПВП. Периапикальная кость начинает заживать в течение нескольких недель, хотя полное радиографическое заполнение кости требует 6-12 месяцев. Установка финальной коронки, через 2-4 недели после завершения лечения корневых каналов, восстанавливает функцию и предотвращает перелом.
Места удаления заживают поэтапно. Формирование кровяного сгустка происходит немедленно. Мягкие ткани закрываются в течение 1-2 недель. Кость заполняет лунку в течение 3-6 месяцев. Установка имплантата, когда это запланировано, обычно происходит через 3-4 месяца после удаления, чтобы позволить начальному заживлению кости.
Раннее вмешательство значительно улучшает результаты. Периапикальный абсцесс, леченный в течение нескольких дней после появления симптомов, реагирует на простое лечение корневых каналов. Задержка на недели позволяет разрушению кости расширяться, усложняя лечение и снижая вероятность выживания зуба. Периодонтальные абсцессы, леченные своевременно, сохраняют зубы; задержанное лечение часто приводит к безнадежному прогнозу, требующему удаления.
Факторы, влияющие на результаты, включают соблюдение пациентом рекомендаций, иммунный статус и выполнение окончательной терапии. Пациенты, которые завершают назначенные курсы антибиотиков и возвращаются для запланированных окончательных процедур, испытывают лучшие результаты. Курение ухудшает заживление, снижая кровоток и иммунную функцию. Диабет требует контроля гликемии для оптимального восстановления.
Какие достижения формируют будущее лечения стоматологических инфекций?
Новые антимикробные пептиды нацелены на биопленки без развития резистентности. Лазерная дезинфекция улучшает стерилизацию корневых каналов. Персонализированная медицина использует генетическое тестирование для предсказания риска инфекции и реакции на лечение.
Достижения в антимикробной терапии решают проблему резистентности биопленок. Традиционные антибиотики неэффективны против бактерий, защищенных биопленками. Исследователи разрабатывают антимикробные пептиды, короткие фрагменты белков, которые нарушают мембраны бактерий без развития резистентности. Эти пептиды, полученные из природных иммунных молекул, показывают перспективы в качестве ирригантов для корневых каналов и местных средств лечения.
Фотодинамическая терапия использует светочувствительные красители для уничтожения бактерий. Стоматолог наносит фотосенсибилизирующее вещество на зараженную область, а затем подвергает ее воздействию определенных длин волн света. Реактивные кислородные виды уничтожают мембраны бактерий и ДНК. Эта техника стерилизует системы корневых каналов и пародонтальные карманы без антибиотиков.
Минимально инвазивные методы сохраняют структуру зуба. Технология GentleWave использует мультисоническую энергию и современные динамические жидкости для дезинфекции сложной анатомии корневых каналов с минимальным инструментарием. Лазерное лечение корневых каналов одновременно испаряет инфицированные ткани и стерилизует стенки канала.
Персонализированная стоматологическая помощь использует генетический и микробиомный анализ. Генетическое тестирование выявляет пациентов с врожденными иммунными дефицитами, предрасполагающими к тяжелым инфекциям. Профилирование орального микробиома предсказывает риск пародонтальных заболеваний и направляет на целевую пробиотическую терапию. Фармакогеномика определяет оптимальный выбор антибиотиков на основе индивидуального метаболизма.
Регенеративная эндодонтия представляет собой парадигмальный сдвиг. Вместо удаления пульпы и заполнения каналов инертным материалом, этот подход способствует регенерации пульповой ткани с использованием стволовых клеток и факторов роста. Незрелые зубы с инфицированной пульпой могут продолжать развитие корня, производя более крепкие и долговечные зубы. Исследования Галлер (2021) в Журнале эндодонтии демонстрируют продолжение созревания корня у 80% обработанных незрелых постоянных зубов.
Часто задаваемые вопросы о лечении инфекций зубов
Требуют ли все зубные инфекции антибиотиков?
Нет. Локализованные зубные абсцессы без температуры или отека лица требуют лишь контроля источника, дренажа, корневого канала или удаления. Антибиотики помогают только при системном распространении инфекции.
Неправильное представление о том, что каждая зубная инфекция требует антибиотиков, приводит к чрезмерному назначению. Клинические рекомендации Американской стоматологической ассоциации и Британского национального института здоровья и ухода за пациентами четко указывают, что антибиотики не нужны для большинства локализованных зубных инфекций. Процедуры контроля источника устраняют инфекцию непосредственно. Добавление антибиотиков не приносит пользы и способствует резистентности.
Антибиотики становятся необходимыми, когда у пациентов наблюдается системное вовлечение. Температура, недомогание, лимфаденопатия или распространяющийся целлюлит указывают на бактериальную нагрузку, превышающую локальное сдерживание. Иммунокомпрометированные пациенты могут нуждаться в более раннем начале антибиотиков. Когда стоматологи не могут провести немедленный контроль источника из-за проблем с доступом пациента, антибиотики служат временными мостами к окончательному лечению.
Сколько времени занимает лечение зубной инфекции?
Дренаж острого абсцесса обеспечивает немедленное облегчение. Лечение корневого канала требует 1-3 визитов в течение 1-2 недель. Удаление зуба заживает за 1-2 недели. Курсы антибиотиков длятся 5-7 дней.
Продолжительность лечения зависит от тяжести инфекции и выбранного подхода. Простое дренирование абсцесса занимает 30 минут в стоматологическом кабинете. Боль улучшается в течение нескольких часов. Однако пациент должен вернуться для окончательного лечения зуба в течение нескольких дней, чтобы предотвратить рецидив.
Лечение корневого канала обычно включает два визита. Первый визит удаляет инфицированную пульпу и вводит антибактериальное средство. Второй визит, через 1-2 недели, заполняет и герметизирует каналы. Третий визит ставит постоянную коронку через 2-4 недели. Общее время лечения: 4-8 недель для полного восстановления.
Удаление зуба обеспечивает самое быстрое окончательное решение. Процедура занимает 20-40 минут. Мягкие ткани заживают за 1-2 недели. Если планируется замена импланта, срок увеличивается на 3-6 месяцев для заживления кости перед установкой импланта.
Курсы антибиотиков остаются короткими. Пяти- или семидневного курса достаточно для зубных инфекций, в отличие от длительных курсов, необходимых для инфекций глубоких тканей или костей. Пациенты должны завершить полный курс, даже если симптомы улучшаются раньше, чтобы предотвратить рецидив и резистентность.
Могут ли стоматологические инфекции заживать самостоятельно?
Нет. Стоматологические инфекции требуют профессионального вмешательства. Организм не может устранить источники инфекции внутри зубов или в полостях абсцессов. Задержка лечения увеличивает риск осложнений.
Иногда абсцесс разрывается спонтанно, выделяя гной и временно снимая давление. Пациенты могут интерпретировать это как "заживление". Однако источник инфекции, некротическая пульпа, глубокий кариес или пародонтальный карман, остаются. Бактерии вновь размножаются. Абсцесс рецидивирует, часто с более устойчивыми организмами.
Закрытая среда корня зуба или полости абсцесса препятствует доступу иммунной системы. Нейтрофилы и антитела не могут эффективно проникать в некротическую ткань или густой гной. Антибиотики, циркулирующие в крови, не могут достичь бактерий в этих аваскулярных пространствах. Только механическое удаление, дренирование, лечение корневых каналов или экстракция устраняют инфекцию.
Редко хронические инфекции низкой степени сохраняются в течение месяцев без острых симптомов. Эти "тихие" инфекции все равно разрушают кость и выделяют воспалительные медиаторы в кровоток. Они способствуют системным проблемам со здоровьем, не вызывая заметной боли. Регулярные стоматологические рентгеновские снимки выявляют эти скрытые инфекции.
Когда следует обратиться за неотложной помощью при стоматологической инфекции?
Обратитесь за неотложной помощью при затруднении дыхания или глотания, быстро распространяющемся отеке лица, температуре выше 39°C (102°F), спутанности сознания или вовлечении глаза при инфекциях верхних зубов.
Предупредительные знаки неотложной помощи указывают на угрожающее жизни течение. Угроза дыхательных путей из-за отека поднижнечелюстной области или дна рта требует немедленной оценки в отделении неотложной помощи. Пациенты, которые не могут проглотить собственную слюну, у которых развивается шумное дыхание (стридор) или которые чувствуют, что их горло закрывается, нуждаются в неотложном управлении дыхательными путями.
Быстро распространяющийся целлюлит, отек, который заметно увеличивается в течение нескольких часов, указывает на агрессивный бактериальный штамм или ослабленный иммунитет. Необходимы внутривенные антибиотики и возможное хирургическое дренирование. Отек лица, пересекающий среднюю линию или затрагивающий обе стороны, указывает на двустороннее распространение.
Системная токсичность сигнализирует о сепсисе. Высокая температура, учащенное сердцебиение (более 100 ударов в минуту), учащенное дыхание (более 20 вдохов в минуту) и измененное психическое состояние требуют неотложной помощи. Эти пациенты нуждаются в посевах крови, внутривенных жидкостях и антибиотиках широкого спектра в условиях интенсивной терапии.
Вовлечение глаза при инфекциях верхних зубов угрожает зрению. Отек вокруг глаза, двоение в глазах или невозможность двигать глазом указывают на орбитальный целлюлит. Это осложнение, возникающее из-за инфекций верхнечелюстных зубов, распространяющихся через тонкую кость в орбиту, требует неотложной консультации офтальмолога и ЛОР-врача.
Симптом | Необходимое действие | Срок |
Зубная боль с легким отеком | Стоматологический прием | В течение 24-48 часов |
Отек лица, лихорадка | Неотложная стоматологическая или медицинская помощь | В тот же день |
Трудности с дыханием/глотанием | Отделение неотложной помощи | Немедленно |
Отек глаза, изменения зрения | Отделение неотложной помощи | Немедленно |
Смущение, высокая температура, учащенное сердцебиение | Отделение неотложной помощи/911 | Немедленно |
Заключение: Почему ранние действия спасают зубы и жизни
Стоматологические инфекции требуют немедленного контроля источника через дренирование, лечение корневых каналов или удаление. Антибиотики играют вспомогательную роль при системном распространении. Профилактика через регулярный уход предотвращает боль, затраты и опасность продвинутых инфекций.
Лечение инфекций зубов основывается на четких принципах. Устраните источник инфекции. Дренируйте гной и некротические ткани. Сохраняйте естественные зубы, когда это возможно. Удаляйте, когда это необходимо. Используйте антибиотики разумно, только при системном вовлечении или когда процедуры необходимо отложить.
Доказательства в значительной степени поддерживают этот подход. Антибиотики одни неэффективны, потому что они не могут достичь бактерий в некротических камерах пульпы и абсцессах. Организмы, защищенные биопленкой, сопротивляются проникновению препаратов. Только механическое удаление инфицированных тканей приводит к выздоровлению.
Ранняя диагностика предотвращает осложнения. Небольшая периапикальная поражение на рентгене предупреждает о надвигающемся абсцессе. Глубокий пародонтальный карман сигнализирует о риске абсцесса. Лечение этих состояний до появления острых симптомов сохраняет зубы, деньги и здоровье.
Сбалансированное использование антибиотиков защищает отдельных пациентов и общественное здоровье. Каждый ненужный рецепт способствует устойчивости. Стоматологи, следуя принципам управления, назначают антибиотики только в указанных случаях, выбирая узкоспектровые препараты первого ряда и ограничивая продолжительность, сохраняют эффективность антибиотиков для будущих поколений.
Интеграция клинического лечения и профилактики обеспечивает наилучшие результаты. Пациенты, которые сочетают регулярные визиты к стоматологу с ежедневным уходом за полостью рта, редко развивают инфекции. Когда инфекции возникают, они быстро обращаются за помощью, а не терпят боль или надеются на спонтанное разрешение.
Будущее лечения инфекций зубов выглядит многообещающе. Терапии, нацеленные на биопленку, регенеративные техники и подходы персонализированной медицины улучшат результаты, снижая зависимость от антибиотиков. Однако основополагающий принцип остается неизменным: определить источник, устранить инфекцию и восстановить здоровье.
Ссылки
Cope, Anwen L., et al. "Использование антибиотиков в стоматологической практике: систематический обзор." Британский стоматологический журнал, т. 216, № 9, 2014, с. 523-30.
Galler, Kerstin M., et al. "Регенеративные эндодонтические процедуры для лечения некроза пульпы у незрелых постоянных зубов: систематический обзор." Журнал эндодонтии, т. 47, № 8, 2021, с. 1193-202.
Lockhart, Peter B., et al. "Плохое здоровье полости рта как хроническое, потенциально инфекционное и воспалительное состояние." Журнал стоматологических исследований, т. 98, № 10, 2019, с. 1073-80.
Matthews, David C., et al. "Антибиотики для острых стоматологических абсцессов: систематический обзор." Журнал антимикробной химиотерапии, т. 71, № 3, 2016, с. 564-71.
Moore, R. Andrew, et al. "Нестероидные противовоспалительные препараты для острого стоматологического болевого синдрома." Кохрейновская база данных систематических обзоров, № 12, 2015, CD004978.
Ng, Yuan-Ling, et al. "Результаты первичного лечения корневых каналов: систематический обзор литературы." Международный журнал эндодонтии, т. 44, № 7, 2011, с. 597-612.
Пател, Шанон и др. "Конусно-лучевая компьютерная томография в эндодонтии." Международный эндодонтологический журнал, т. 52, № 9, 2019, с. 1248-64.
Петерсен, Пуль Эрик. "Глобальная политика Всемирной организации здравоохранения по улучшению орального здоровья." Международный стоматологический журнал, т. 72, № 4, 2022, с. 302-07.
Сеневиратне, Чаминда Дж. и др. "Биопленка зубного налета: архетипическая биопленка." Периодонтология 2000, т. 75, № 1, 2017, с. 34-44.